THESE
PRESENTEE ET PUBLIQUEMENT SOUTENUE DEVANT LA FACULTE DE PHARMACIE DE MARSEILLE
LE 22 SEPTEMBRE 2017
PAR
Mademoiselle Audrey LELORIEUX
Née le 18 décembre 1991 à Chartres (28)
EN VUE D’OBTENIR
LE DIPLOME D’ETAT DE DOCTEUR EN PHARMACIE
« ETRE SPORTIF AVEC UN DIABETE DE TYPE 1 »
JURY :
Président : Mme le Maître de conférences Carole DI GIORGIO Membres : M. le Docteur Thierry AUGIER, Directeur de Thèse
Mme le Docteur Elisabeth GUIBOURGE M. le Docteur Denis LAPLANE
REMERCIEMENTS
A mon Papy, ma bonne étoile.
A ma Mamie, pour ton écoute attentionnée, ta bienveillance et ton amour.
A mon Papa, mon Papou, pour tout ton amour, ton soutien à chaque instant, pour ton exigence, pour la valeur du travail et la force que tu me transmets.
A ma Maman, pour ton amour, ton soutien, ton estime de moi, pour tout ce qui fait la personne que je suis devenue.
A ma Grande sœur, pour ton amour, pour notre complicité inconditionnelle et pour ton soutien infaillible chaque jour.
A ma Famille, pour votre présence, votre générosité, votre bienveillance et pour ces liens si forts qui nous unissent.
A mon professeur Mr Thierry AUGIER, pour ces cours passionnants de diabétologie qui m’ont permis de pouvoir présenter aujourd’hui ce sujet de thèse. Pour le soutien après l’insuccès au concours de l’internat et pour m’avoir ouvert les portes à l’exercice officinal.
A Danièle et Denis LAPLANE, pour la recherche de ce sujet ainsi que pour toute l’aide apportée durant ces longs mois d’écriture. Pour votre présence et votre bienveillance.
A mon binôme Arnaud BOCQUET, pour ces années de faculté passées ensemble, pour ces fous rires en TP, pour nos quelques engueulades aussi, pour ces nombreuses et belles années d’amitiés et celles à venir. Pour cette belle famille que vous construisez à deux.
A Aurore MERCIER, pour toutes ces relectures et corrections souvent très tardives qui ont permis d’embellir ma thèse. Pour tous ces merveilleux moments d’amitiés passés ensemble et ceux à venir.
A Mathilde RAVEL, pour notre amitié et notre belle complicité qui restent intacte années après années.
A mes Carabins : Angélique, Anthony, Mary, Vincent, Sarah et Jean-Camille, pour ses nombreuses parties de baby-foot Médecins VS Pharmaciens, pour toutes ces places gardées et ces longues heures à la BU, pour tous ces moments passés ensemble et ceux à venir. Mes docteurs le meilleur vous attend.
A Aline WENZ, pour ces journées interminables de mise en page, pour ta présence et ta gentillesse sans faille.
A Ninon MAURICE et Axel SCHIETSE, pour cette belle amitié qui nous unie. A Giulia MIZOULE, pour le soutien après la non-réussite de l’internat, le semestre de 6ème année officine et nos deux DU, à l’avenir professionnel qui s’ouvre enfin à nous.
A Florence DIEZ et Danièle LAPLANE, pour le soutien après ce changement d’avenir vers l’exercice officinal et pour la confiance que vous m’accordez au jour le jour.
A l’ensemble de mes collègues : Alexandra, Carole, Florence, Soizic, pour ces nombreuses heures de travail à vos côtés, pour l’aide et l’apprentissage quotidien.
A Michèle, pour ta rigueur et ton amour du travail bien fait.
A l’ensemble de mes Membres du Jury, (Mr Thierry AUGIER, Mme Carole DI GIORGIO, Mme Elisabeth GUIBOURGE, Mme Danièle LAPLANE, Mr Denis LAPLANE), pour avoir répondu positivement et avec enthousiasme à ma demande et d’être présent aujourd’hui.
A Madame La doyenne Françoise DIGNAT GEORGE, pour votre implication et tous ces changements à la faculté qui ont rendu ces années meilleures.
A la Faculté de Pharmacie de Marseille et à tous ses professeurs, pour le riche apprentissage.
A tous ceux que je n’ai pas pu citer, mais qui sont présent dans mon cœur chaque jour.
TABLE DES MATIERES
REMERCIEMENTS ... 8
TABLE DES MATIERES ... 10
LISTE DES FIGURES ... 14
PARTIE 1 - LE DIABETE DE TYPE 1 INTRODUCTION ... 16 1 DEFINITIONS ... 17 2 HISTORIQUE ... 20 3 EPIDEMIOLOGIE ... 22 4 ETIOLOGIE ... 25 4.1 FACTEURSAUTO-IMMUNS ... 25 4.2 PREDISPOSITIONGENETIQUE ... 25 4.3 HEREDITE ... 26 4.4 FACTEURSENVIRONNEMENTAUX ... 27 5 PHYSIOPATHOLOGIE ... 28 5.1 LEPANCREAS ... 28 5.2 L’INSULINE ... 30 5.3 MECANISMESPATHOLOGIQUES ... 32 6 DIAGNOSTIC ... 33 6.1 SIGNESCLINIQUES ... 33 6.2 BILANBIOLOGIQUE ... 33 6.3 IMMUNOGENETIQUE ... 34
6.4 MESUREDUPEPTIDECBASAL ... 35
6.5 TESTDESTIMULATIONAUGLUCAGON ... 36
7 SIGNES CLINIQUES ... 37
8 COMPLICATIONS ... 38
8.1 COMPLICATIONSAIGUES ... 38
8.1.2 HYPERGLYCEMIE ET ACIDOCETOSE ... 40
8.2 COMPLICATIONSCHRONIQUES ... 42
8.2.1 MICROANGIOPATHIES ... 42
8.2.1.1 LES ATTEINTES OCULAIRES ... 42
8.2.1.2 LES ATTEINTES RENALES ... 43
8.2.1.3 LES ATTEINTES NEUROLOGIQUES ... 44
8.2.2 MACROANGIOPATHIES ... 46
8.2.2.1 LES ATTEINTES CARDIAQUES ... 47
8.2.2.2 LES ATTEINTES ARTERIELLES ... 48
8.2.3 SENSIBILITE AUX INFECTIONS ... 49
8.2.4 LES AUTRES COMPLICATIONS ... 50
9 CONCLUSION ... 53
PARTIE 2 - TRAITEMENTS ET SUIVIS 1 TRAITEMENTS ... 54 1.1 OBJECTIFS ... 54 1.2 BILANINITIAL ... 55 1.3 REGLESHYGIENO-DIETETIQUES ... 55 1.3.1 REGIME ALIMENTAIRE ... 55 1.3.2 ACTIVITE PHYSIQUE ... 57
1.3.3 REDUCTION DES FACTEURS DE RISQUE CARDIOVASCULAIRE ... 58
1.4 TRAITEMENTSINSULINIQUES ... 59
1.4.1 LES INSULINES ... 59
1.4.2 MODE D’ADMINISTRATION ... 61
1.4.3 EFFETS INDESIRABLES/CONTRE-INDICATIONS ... 62
1.4.4 SCHEMAS INSULINIQUES ... 63
1.4.5 ADAPTATION DES DOSES D’INSULINE ... 68
1.5 EDUCATIONTHERAPEUTIQUEDUPATIENTDIABETIQUE ... 69
1.5.1 HISTORIQUE ... 69
1.5.2 DEFINITIONS ... 69
1.5.3 BUTS DE L’EDUCATION THERAPEUTIQUE ... 70
1.5.4 LES PROGRAMMES ... 70
1.6 MESURESASSOCIEES ... 71
1.7.1 LA RECHERCHE DANS LE DOMAINE DU DIABETE ... 72
1.7.2 LA GREFFE ... 72
1.7.3 LE PANCREAS ARTIFICIEL ... 74
1.7.4 « UN VACCIN CONTRE LE DIABETE DE TYPE 1 ? » ... 74
2 SURVEILLANCE GLYCEMIQUE ... 75
2.1 METHODES ... 75
2.1.1 BIOLOGIQUE : L’HEMOGLOBINE GLYQUEE (HbA1c) ... 75
2.1.2 AUTO SURVEILLANCE GLYCEMIQUE ... 76
2.2 LECTEURSDEGLYCEMIE ... 78
2.2.1 LES LECTEURS ... 78
2.2.2 LES AUTOPIQUEURS ET LEURS LANCETTES ... 79
2.2.3 LES BANDELETTES ... 79
2.2.4 LES COLLECTEURS DE DECHETS ... 80
2.2.5 LES CARNETS DE SURVEILLANCE ... 80
2.3 INNOVATIONS ... 81
2.3.1 LE SYSTEME FLASH D’AUTOSURVEILLANCE ... 81
3 CONCLUSION ... 83
PARTIE 3 - "COMMENT CONJUGUER SPORT ET DIABETE INSULINODEPENDANT ?" 1 L’ACTIVTIE PHYSIQUE ... 85
1.1 DEFINITION ... 85
1.2 BESOINSENERGETIQUES ... 85
1.3 PHYSIOLOGIEGENERALE ... 87
1.4 PHYSIOLOGIECHEZLEPATIENTDIABETIQUE ... 89
2 RECOMMANDATIONS ... 91
2.1 RECOMMANDATIONSGENERALESDEL’ISPAD ... 91
2.2 RECOMMANDATIONSAL’ECOLE ... 92
3 QUELS SPORTS ? ... 93
4 LA PLACE DU SPORT CHEZ LE DIABETIQUE DE TYPE 1 ... 94
4.2 FREINS ... 95
5 COMPLICATIONS SPORTIVES PROPRE AUX DIABETIQUE DE TYPE 1 ... 96
5.1 HYPOGLYCEMIE ... 96
5.1.1 MECANISMES PHYSIOLOGIQUES DE L’HYPOGLYCEMIE ... 96
5.1.2 RECOMMANDATIONS (INSULINE/ALIMENTATION) ... 98
5.2 HYPERGLYCEMIE ... 99
5.2.1 MECANISMES PHYSIOLOGIQUES DE L’HYPERGLYCEMIE ... 99
5.2.2 RECOMMANDATIONS (INSULINE/ALIMENTATION) ... 100
6 SURVEILLANCE GLYCEMIQUE ... 101
7 ADAPTATION DU TRAITEMENT ... 102
7.1 AJUSTEMENTDEL’INSULINE ... 102
7.2 ADAPTATIONALIMENTAIRE ... 103
7.2.1 LORS D’UNE COMPETITION ... 105
7.2.2 CAS PARTICULIERS : LA POMPE A INSULINE ... 108
8 CONSEILS A L’OFFICINE ... 109
9 VECU DE SPORTIFS DE DIABETE DE TYPE 1 ... 109
9.1 INTERVIEWD’UNSPORTIFAMATEUR... 109
9.2 PEUT-ONÊTREUNSPORTIFDEHAUTNIVEAU ? ... 112
10 CONCLUSION ... 113
CONCLUSION GENERALE ... 115
ANNEXE ... 117
LISTE DES FIGURES
Figure 1 : Seuils de glycémie et états physiopathologiques corrélés ... 18
Figure 2 : Incidence annuelle du diabète de type 1 (0 – 14 ans) dans différents pays3 ... 23
Figure 3 : Le Pancréas14 ... 28
Figure 4 : Représentation de la molécule d’insuline humaine13 ... 30
Figure 5 : Modélisation des différentes étapes et mécanismes pathologiques du diabète11 ... 32
Figure 6 : Exemples de signes cliniques de l'hypoglycémie ... 38
Figure 7 : Type d’aliment permettant un resucrage efficace39 ... 40
Figure 8 : Divergences entre microalbuminurie et macroalbuminurie... 44
Figure 9 : Evolution de l’athérosclérose au cours du temps39 ... 47
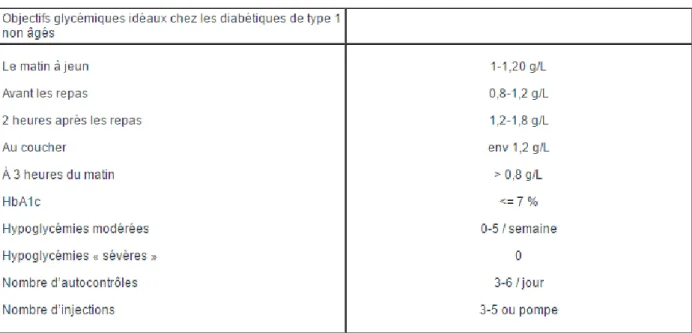
Figure 10 : Objectifs glycémiques idéaux chez un diabétique de type 1 (Non âgé)7 ... 54
Figure 11 : Caractéristiques spécifiques des insulines rapides19 ... 60
Figure 12 : Caractéristiques spécifiques des analogues rapides de l’insuline19 ... 60
Figure 13 : Caractéristiques spécifiques des insulines de durée d’action intermédiaire 19 ... 60
Figure 14 : Caractéristiques spécifiques des analogues lents de l’insuline19 ... 61
Figure 15 : Site d’injection en fonction de l’insuline à administrer ... 62
Figure 16 : Schéma de la sécrétion physiologique de l’insuline31 ... 63
Figure 17 : Exemple de calcul des différentes doses d’insulines pour un enfant de 30 Kg lors d’un schéma insulinique conventionnel ... 64
Figure 18 : Exemple de calcul des différentes doses d’insulines pour un adolescent ... 65
Figure 19 : Exemples de schémas insuliniques avec la technique à 3 injections ... 66
Figure 20 : Exemples de schémas insuliniques avec la technique à 2 injections ... 67
Figure 21 : Tableau de correspondance entre l’HbA1c et la glycémie ... 76
Figure 22 : Erreurs et risques possibles lors de la réalisation d’un autocontrôle glycémique2577 Figure 23 : Dessin représentant les conteneurs D.A.S.R.I 45... 80
Figure 24 : Tableau représentant les différentes classes d’intensités sportives53 ... 86
Figure 25 : Schéma explicatif des différentes étapes de la glycolyse54... 87
Figure 26 : Schéma explicatif de la ... 88
Figure 27 : Schéma représentant le cycle de KREBS et le bilan énergétique associé54... 88
Figure 28 : Schéma explicatif des besoins en glucose lors de la contraction musculaire ... 98
Figure 29 : Tableau reliant l’intensité et la durée d’une activité physique à la diminution de dose d’insuline3 ... 103
Figure 30 : Tableau récapitulatif de la dépense énergétique et de son équivalent en sucre pour différents sports55 ... 104
Figure 31 : Exemple d’adaptation alimentaire en fonction du type d’effort55 ... 105
INTRODUCTION
« Bill TALBERT, le légendaire champion des doubles, a réussi à défier les plus grands tennismans mais aussi le Diabète. Diagnostiqué à l'âge de 10 ans, il est alors mis en garde contre la pratique d’une activité sportive… quelques années plus tard, son palmarès parle de lui-même avec 33 titres nationaux répartis sur plus d’une dizaine d’années. »
Depuis les prouesses de ce tennisman émérite dans les années 50, plusieurs sportifs de haut niveau ont démontré que l’association d’une l’activité physique tout en étant diabétique est réalisable. Cette révolution nous permet de nous poser la question :
« Le diabète et l’activité physique, un partenariat possible ? »
Par la suite, l’univers de la diabétologie s’est alors penché sur cette question afin de permettre aux patients de pouvoir se rapprocher au plus près de la vie quotidienne d’un individu non atteint.
Les différentes recherches et publications parues ont permis au sport, de devenir un traitement à part entière, au même titre que les injections d’insuline ou l’adaptation du régime alimentaire. De nos jours, l’activité physique fait même partie de ces traitements qui, sur le plan psychologique, aide le patient à effectuer un vrai travail sur lui (estime et connaissance de soi) et lui permet de se sentir « normal » au même titre que les autres.
Ainsi, cet écrit s’axera autour de trois parties :
La première ciblera le diabète, sa définition clinique et physiopathologique, ainsi que les complications engendrées.
La deuxième sera plus spécifique aux différents traitements que l’on peut proposer aux patients et les surveillances associées.
La dernière partie ouvrira les portes de la possible conjugaison entre la pratique d’une activité sportive et la pathologie qu’est le diabète ; ses complications particulières mais aussi l’ensemble de ses effets bénéfiques sur la santé physique et psychique du patient.
PARTIE 1 - LE DIABETE DE TYPE 1
1 DEFINITIONS
Selon l’Organisation Mondiale de la Santé (O.M.S) :
« Le diabète est une maladie chronique qui survient lorsque le pancréas ne produit pas assez d'insuline ou lorsque l'organisme n'est pas capable d'utiliser efficacement l'insuline qu'il produit. »1
Le diabète est un trouble de l’assimilation, de l’utilisation et du stockage des sucres. L’insuline étant la seule hormone diminuant la concentration de sucre dans le sang, il en résulte une concentration accrue de glucose dans le sang, appelée hyperglycémie. Cette dernière, conduit, au fil des années, à des complications graves atteignant tous les systèmes de l’organisme.1
Le diabète se définit précisément par une glycémie à jeun (généralement matinale) supérieure à 1.26 g/L sur 2 dosages consécutifs, ou par une Hyperglycémie Provoquée (HGPO = dosage de la glycémie 2 heures après une absorption orale de 75g de glucose) supérieure à 2 g/L, ou encore par une glycémie supérieure à 2 g/L à n’importe quel moment de la journée.2
1 : Site Internet de l’OMS – thème de santé, Diabète
http://www.who.int/topics/diabetes_mellitus/fr/ consulté le 09/09/2016
2 : Site Internet de la Fédération Française des Diabétiques – Qu’est-ce que le diabète ?
HYPOGLYCEMIE Inférieur à 0.60 g/L Inférieur à 3.3 mmol/L GLYCEMIE NORMALE A jeun : inférieur à 1.10 g/L inférieur à 6.1 mmol/L HGPO: inférieur à 1.40 g/L inférieur à 7.8 mmol/L
Glycémie aléatoire : inférieur à 1.40 g/L inférieur à 7.8 mmol/L
INTOLERANCE AU GLUCOSE
A jeun : entre 1.10 g/L et 1.26 g/L entre 6,1 mmol/L et 6.9 mmol/L
HGPO : entre 1.40 g/L et 2 g/L
entre 7.8 mmol/L et 11.1 mmol/L
Glycémie aléatoire : entre 1.40 g/L et 2 g/L entre 7.8 mmol/L et 11.1 mmol/L DIABETE A jeun : supérieur à 1.26 g/L supérieur à 7 mmol/L HGPO : supérieur à 2 g/L supérieur à 11.1 mmol/L
Glycémie aléatoire : supérieur à 2 g/L supérieur à 11.1 mmol/L
Il existe 4 classes de diabète :
- Diabète de type 1 ou Diabète InsulinoDépendant (DID) - Diabète de type 2 ou Diabète NonInsulinoDépendant (DNID) - Diabète gestationnel
- Et des diabètes secondaires :3
Défauts génétiques de fonction des cellules β :
Chromosome 20 (MODY 1), Chromosome 7 glucokinase (MODY 2), Chromosome 12 HNF α (MODY 3), Chromosome 13 facteur promoteur de l’insuline (1PF-1 ; MODY 4), Chromosome 17nHNF-1β (MODY 5), Chromosome 2 Neuro D1 (MODY 6), Chromosome 7 KCNJ11 (Kir 6.2), Mutation de l’ADN mitochondrial
Défauts génétiques de l’action de l’insuline : Résistance à l’insuline de type A, Diabète lipoatrophique …
Maladie pancréatique exocrine :
Pancréatite, Traumatismes/Pancréatectomie, Hémochromatose… Maladie endocrinienne :
Acromégalie, Syndrome de Cushing… Infectieux :
Rubéole congénitale, Cytomégalovirus …
Association du diabète à d’autres pathologies d’origine immunitaire, appelées aussi « Polyendocrinopathies auto-immunes » : hypothyroïdie, vitiligo, insuffisance surrénalienne, intolérance au gluten.
Cet écrit ciblera précisément le diabète de type 1 : ses spécificités, ses traitements et son suivi et plus particulièrement ses synergies avec l’activité physique dans la dernière partie.
3 : International Society for Pediatric and Adolescent Diabete (ISPAD). 2009.
Le diabète de type 1 (connu auparavant sous le nom de Diabète InsulinoDépendant (DID) ou diabète juvénile) se caractérise par une production d'insuline insuffisante, voire nulle, exigeant une administration quotidienne de cette dernière. Ce déficit de production est dû à une destruction progressive des cellules béta des îlots de Langerhans du pancréas, par le système immunitaire et plus particulièrement les lymphocytes T. Cette pathologie est, de ce fait, une Maladie Auto-Immune (MAI). Ces MAI sont définies « comme une agression contre l’organisme par son propre système immunitaire », expliquant l’attaque contre les cellules béta pancréatiques propre à l’organisme.2
2 HISTORIQUE
La première description d’une maladie se rapprochant du diabète remonte à l’antiquité égyptienne. C’est le Papyrus de Thèbes datant de 1 550 avant Jésus-Christ qui en est le témoin.
Au IIème siècle après Jésus-Christ, le Médecin Arétée de Cappadoce décrit à nouveau cette
pathologie : « Le diabète est une affection grave, peu fréquente, qui se caractérise par une fonte musculaire importante des membres dans l’urine. Le patient n’arrête pas d’uriner et ce flux est incessant comme un aqueduc qui se vide. La vie est courte, désagréable et douloureuse, la soif est inextinguible [...]. Les patients sont en proie à des nausées, un état d’agitation, une soif dévorante, et en peu de temps ils meurent.»63
Au XIème siècle après Jésus-Christ, c’est le médecin Avicenne qui ajoute au tableau clinique déjà décrit des complications telles que la gangrène et la perte des fonctions sexuelles.
Au XVIIème siècle après Jésus-Christ, Thomas Willis, le médecin du roi Charles II d’Angleterre, fait de nouveau parler du diabète en faisant à son tour état du goût sucré de l’urine des diabétiques.
__________________________
63 : Site internet Suisse, Le Fait Médical, « Petite Histoire du Diabète »,
http://www.lefaitmedical.ch/fr/articles/petite-histoire-du-diabete-11-46, consulté le 03/09/2017
Au XIXème siècle après Jésus-Christ, « le fameux chercheur français Claude Bernard montre
que le sucre sanguin, le glucose, peut être stocké dans le foie sous forme de glycogène. Le rôle du pancréas est mis en évidence par les Allemands Oskar Minkowski et Josef von Mering, suite à l’ablation de cet organe chez le chien, celui-ci meurt peu après de diabète. »63
Quelques dates clés des époques suivantes :
« 1869 : découverte des îlots de Langerhans par l’étudiant allemand Paul Langherhans.
1889 : lien établi entre le pancréas et le diabète par les Allemands Oskar Minkowski et Josef
Von Mering.
1921 : découverte de l’insuline par Frederick Grant Banting et Charles Best.
1922 : première injection d’insuline (extraite du pancréas de porc) sauvant un enfant de 14
ans.
1923 : prix Nobel décerné à Frederick Grant Banting pour cette grande avancée.
Début de la production industrielle et commercialisation d’insuline par des laboratoires à partir du pancréas de bœuf et de porc.
1955 : Frederick Sanger décrit la structure chimique de l’insuline humaine.
1978-1982 : grâce aux progrès des technologies, l’insuline est produite par génie
génétique. »62
__________________________
62 : site Internet DinnoSanté – « Historique du Diabète »,
https://www.dinnosante.fr/fre/17/histoire-du-diabete?mobile_bloc=comprendre_diabete, consulté le 03/09/2017
3 EPIDEMIOLOGIE
Le diabète est la plus fréquente des maladies endocriniennes de l’homme. Concernant le diabète de type 1, il représente environ 10% des cas de diabète dans le monde.4
La prévalence en France est de 13.5 cas pour 100 000 enfants de moins de 15 ans5 et plus généralement de 200 000 (soit 15 % de diabétiques de type 1).7. Au niveau européen ce chiffre varie d’un pays à un autre avec un gradient Nord-Sud, marqué par une prévalence plus élevée au Nord (Finlande = 65 cas pour 100 000 habitants). Une seule exception la Sardaigne (pays du sud), fait partie des pays les plus touchés par cette pathologie. Cette particularité reste encore inexpliquée à ce jour.5
4 : T.R HARRISON, Principes de Médecine Interne - « Partie 12 : Endocrinologie et
Métabolisme, Section 1 : Endocrinologie, Diabète sucré et Hypoglycémie » par Daniel W. FOSTER et Arthur H. YOUNG
5 : Site Internet de l’INSERM – Diabète de type 1 (DID)
http://www.inserm.fr/thematiques/physiopathologie-metabolisme-nutrition/dossiers-d-information/diabete-de-type-1-did consulté le 09/09/2016
Le diabète de type 1 est défini lors d’études d’incidence par la date à laquelle a eu lieu la première injection d’insuline. En effet, le délai entre le début des symptômes et le véritable diagnostic peut être très variable.3 Actuellement en France, l’incidence est égale à 3,5 pour 100 000 enfants de moins de 15 ans5 et plus généralement à 7,8 pour 100 000 par an. Il représente 90% des diabètes de l’enfant. On estime à environ 12 000, les enfants diabétiques en France, soit 0,1% des enfants âgés de 0 à 15 ans.9
De plus, on visualise depuis une vingtaine d’années une augmentation de l’incidence de 3-4% par an, surtout avant l’âge de 5 ans, suggérant des facteurs environnementaux propices. En effet, on observe dans certaines populations, une augmentation de la proportion des personnes possédant des génotypes HLA à faible risque.7,3
Le diabète de type 1 représente 6 % de patients parmi l’ensemble des diabétiques.6
Cette pathologie survient habituellement avant 35 ans (pic à l’adolescence : 18 – 20 ans), mais peut être diagnostiquée à tout âge7. Dans la plupart des pays occidentaux, le diabète de type 1 équivaut à 90% des diabètes de l’enfant et de l’adolescent, cependant moins de la moitié des personnes qui ont un diabète de type 1 sont diagnostiqué avant l’âge de 15 ans.3
Par ailleurs, une variation saisonnière des nouveaux cas a été décrite avec un pic en hiver.3
Le sex-ratio est de 1.8 On observe une égalité d’apparition de cette maladie entre les hommes
et les femmes. Cependant, dans de rare cas et seulement dans certaines populations quelques différences d’incidences selon le sexe ont été mises en évidence.3
6 : Site Internet de la Fédération Française des Diabétiques – Evolution des chiffres du diabète
en France
http://www.afd.asso.fr/diabete consulté le 09/09/2016
7 : Site Internet de la Société Française d’Endocrinologie – ITEM 233 A, Diabète sucré de
type 1
http://www.sfendocrino.org/article.php?id=392#I consulté le 09/09/2016
8 : Pharma-mémo 2011, Biochimie clinique - Diabète de type 1 ou DID, V.HADDAD et R.
MAS
9 : Pédiatrie, 6e Edition, ELSEVIER-MASSON, 2014. Collège national des pédiatres
4 ETIOLOGIE
Dans le cas du diabète de type 1, pour des raisons encore énigmatiques, le patient fabrique des lymphocytes T qui attaquent ses propres cellules béta pancréatiques et plus particulièrement celles qui produisent l’insuline. Les signes cliniques de décompensation apparaissent lorsque 90% des îlots sont détruits, laissant le diagnostic du diabète de type 1 plus ou moins aisé.3
Les marqueurs sérologiques du processus auto-immuns sont au nombre de 4 : - Anticorps anti-îlots de Langerhans
- Anticorps anti-insuline
- Anticorps anti-glutamate décarboxylase (GAD) - Anticorps anti-IA2 (Islet Antigen 2)
Les facteurs auto-immuns étant plus ou moins spécifiques, l’association à d’autres maladies auto-immunes inflammatoires est fréquente, que ce soit de façon isolée ou dans le cadre d’une polyendocrinopathie auto-immune de type 2 (Hashimoto, Basedow, Insuffisance ovarienne primitive, ISL précoce …).8
Même si le mécanisme d’induction de cette pathologie reste encore inexpliqué, il existe une prédisposition génétique oligogénique (environ une vingtaine de loci identifiés) qui est toujours présente, permettant de définir des facteurs de risque et des facteurs protecteurs : 7
- Facteurs de risque :
o Complexe Majeur d’Histocompatibilité (CMH) de classe I, Human Leucocyte Antigene (HLA) B8, B15 et B18 avec un risque relatif compris entre 2 et 3.8
o CMH de classe II, HLA DR3 et DR4 avec un risque relatif compris entre 3 et
o il existe aussi, en plus des CMH : 7
des éléments variables au sein du gène de l’insuline. Les VNTR (Variable Number Tandem Repeat), sont responsables d’une sous-expression de l’insuline au niveau des cellules épithéliales thymiques.
un gène codant la molécule CTLA-4 (récepteur lié au phénomène d’immunomodulation des lymphocytes T) entrainant la dérégulation du système immunitaire envers ces propres cellules.
une protéine (PTP-N22) codant pour une tyrosine phosphatase, qui module l’activation du récepteur T (mutation retrouvée dans la plupart des maladies auto-immunes).
- Facteurs protecteurs : CMH HLA DR2, DQ, B7, W1/W2.8
A l’inverse des prédispositions génétiques, le rôle de l’hérédité n’est pas déterminant.
En effet, dans 85% des nouveaux cas, on ne retrouve aucun antécédent familiaux de diabète de type 1.7
Risques de développer un diabète de type 1 : - 35% pour le jumeau d’un diabétique8
- 7% pour un frère ou une sœur8
- 2-3% pour l’enfant d’1 seul parent diabétique8
- 30% pour l’enfant de 2 parents diabétiques7
- 7% pour les sujets ayant un typage HLA DR3 ou DR48
- 16 % pour un frère ou une sœur avec identité HLA et HLA-DR3 ou DR47
- 2 à 3 fois plus fréquent chez les enfants d’un père diabétique que ceux issu d’une mère diabétique.3
Les facteurs environnementaux sont encore, à l’heure actuelle hypothétiques : théorie hygiéniste7, facteurs infectieux (CytoMégaloVirus, virus ourliens, rubéole, myxovirus, paramyxovirus, hépatite virale, Epstein Barr Virus8, coxsackies B4 = Prévalence du diabète de type 1 de 20% en cas de rubéole congénitale11…) et facteurs alimentaires (introduction
précoce du lait de vache et plus précisément de l’albumine sérique bovine via la séquence peptidique ABBOS10) jouerait un rôle dans le déclenchement de cette maladie auto-immune
sans en être non plus la cause spécifique.
Physiologiquement, on l’expliquerait par une dérégulation du rôle de filtre de l’organisme suite à ces « agressions », provoquant une inflammation et une production d’anticorps qui se retourneraient après, contre son propre organisme.
Cependant, il ne faut pas confondre les facteurs environnementaux avec les facteurs précipitants (grippe, stress psychologique, choc émotionnel…).7
Les facteurs précipitants sont les seuls déclencheurs de la décompensation de la maladie et, entrainent donc, le passage de l’état de pré-diabète à l’état pathologique.
Ces nombreuses hypothèses étiologiques, montrent l’extrême complexité de cette pathologie qu’est le diabète de type 1. Cela permettra d’expliquer, par la suite, toutes les difficultés auxquelles, l’ensemble du corps médical et le patient feront face lorsqu’il faudra le traiter et retarder ses complications.
__________________________
10 : Diabète et Maladie métabolique, 4e Edition, MASSON, 2003. L. PERLEMUTER, J.-L.
SELAM, G. COLLIN DE L’HORTET – Diabète de type 1 (Insuinodépendant)
11 : Site Internet Mémo-Bio, préparation au concours de l’Internat en Pharmacie – Biochimie
5 PHYSIOPATHOLOGIE
Figure 3 : Le Pancréas14
Le pancréas est un organe glandulaire ou viscère qui fait partie du système endocrinien. Il est situé dans l’abdomen au-dessous et en arrière de l’estomac. Son rôle est la sécrétion du suc pancréatique déversé dans l’intestin pour la digestion, ainsi que l’excrétion dans le sang de deux hormones : l’insuline et le glucagon, qui serviront à la régulation du métabolisme du glucose.12
__________________________
12 : Site Internet de la Société Nationale Française de Gastro-Entérologie – Partie I : Les
organes, Chapitre 7 : Pancréas
http://www.snfge.org/sites/default/files/SNFGE/Formation/chap-7_fondamentaux-pathologie-digestive_octobre-2014.pdf, consulté le 16/09/2016
La sécrétion du suc pancréatique correspond à la fonction exocrine de l’organe. Elle répond aux besoins de l’organisme lors de la digestion en produisant le liquide pancréatique contenant de nombreuses enzymes :
- L’Amylase pour la digestion des sucres - La Lipase pour la digestion des graisses - La Trypsine pour la digestion des protéines
Il existe, en plus, des mécanismes de protection qui empêchent l’autodigestion du pancréas : - La synthèse des enzymes se fait sous forme de pro-enzymes inactives
(trypsinogène, procolipase) qui s’auto-activeront ou seront activées par d’autres enzymes dans la lumière duodénal,
- La présence d’un gradient de pression qui empêche la stagnation du suc pancréatique dans son canal,
- « La présence d’inhibiteurs physiologiques des enzymes dans le suc pancréatique (ex : inhibiteur de Kazal de type 1 qui inhibe la trypsine) »12 …
Le pancréas a aussi une fonction endocrine car il excrète des hormones (principalement l’insuline et le glucagon). Ces dernières sont fabriquées par des cellules pancréatiques spécialisées (les cellules béta pour l’insuline et les cellules alpha pour le glucagon), regroupées en petits îlots qui sont disséminés dans le pancréas : appelés îlots de Langerhans. Cette fonction permet de réguler, entre autre, l’homéostasie du glucose, grâce à la production de ces 2 hormones.
- L’insuline, hypoglycémiante, qui permet l’augmentation de l’utilisation périphérique du glucose mais qui inhibe aussi la production hépatique (via l’inhibition de la glycogénolyse et la néoglucogénèse).
- Le glucagon, hyperglycémiant, qui stimule la production hépatique de glucose.
En effet chez le diabétique, le défaut de production d’insuline n’est pas le seul responsable de l’hyperglycémie, le glucagon joue aussi un rôle primordial, expliquant les difficultés d’équilibration de cette pathologie.12
Figure 4 : Représentation de la molécule d’insuline humaine13
L’insuline est, comme décrit précédemment, une hormone excrétée naturellement par le pancréas endocrine. Elle permet la diminution de la glycémie sanguine en faisant entrer le glucose dans les cellules, ce qui permet de l’utiliser comme énergie ou de la réserver pour une utilisation ultérieure. Elle a de ce fait, un effet hypoglycémiant en favorisant le retour de la glycémie à sa valeur basale.15
__________________________
13 : Site Internet de Sciences physique, Montpellier – Inuline et Insuline
http://sciences-physiques.ac-montpellier.fr/ABCDORGA/Famille4/INULINEF.htm, consulté le 16/09/2016
15 : Site internet Diabète – Québec, « Qu’est ce que l’insuline »
http://www.diabete.qc.ca/fr/vivre-avec-le-diabete/soins-et-traitements/medicaments-et-insuline/linsuline, consulté le 30/09/2016
Structurellement, l’insuline est composée de 2 chaines d’acides aminés (chaine A de 21 acides aminés et chaine B de 30 acides aminés) reliées par 3 liaisons disulfidiques13. Sa demi-vie est de 5 minutes13 et sa masse moléculaire est de 5800 Daltons17.
Cette hormone est sécrétée de façon continue (basale) et sous forme de pic (bolus) chez une personne non pathologique. Elle est produite en fonction des besoins de l’organisme, des aliments consommés et de ce fait des sucres absorbés.16
Chez un diabétique de type 1, le pancréas ne produit plus assez, voir ne produit plus du tout d’insuline. Pour pallier à cela, les patients doivent s’injecter plusieurs fois par jour, selon leur glycémie, de l’insuline pour imiter et rétablir le fonctionnement normal du pancréas. Cette manipulation évite ainsi, l’apparition de complications dues à l’hyperglycémie provoquée par cette carence insulinique15.
__________________________
16 : Site Internet de l’association française des diabétiques, « L’insuline, le traitement du
diabète par l’insulinothérapie » - http://www.afd.asso.fr/node/69, consulté le 30/09/2016
17 : Site Internet de la société chimique de France, « Insuline »,
Figure 5 : Modélisation des différentes étapes et mécanismes pathologiques du diabète11
Pour des raisons encore non élucidées, le système immunitaire, via les lymphocytes T cytotoxique et les cytokines macrophagiques, s’attaque au pancréas en détruisant ses propres cellules béta pancréatiques7. L’activation de ce processus auto-immun, mis en évidence par l’apparition d’auto-anticorps dans le sang (Anticorps îlots de Langerhans, Anticorps anti-insuline, Anticorps anti-glutamate décarboxylase, Anticorps anti-IA2 (Islet Antigen 2)) est suivie d’une phase de pré-diabète11. Cette dernière correspond à une destruction progressive et
asymptomatique des cellules béta des îlots de Langerhans sur environ 5-10 ans.11
A l’issue de ses années de pré-diabète, lorsque qu’il ne reste que 20% de cellules qui fonctionnent et que les lésions pancréatiques, appelées « insulite »18 sont trop nombreuses,
l’insulinémie devient insuffisante pour maintenir la glycémie dans ses valeurs normales et la symptomatologie clinique apparait.11
__________________________
18 : Site internet de la faculté de medecine Pierre et Marie CURIE, Diabétologie,
6 DIAGNOSTIC
Comme décrit ci-après, les signes cliniques étant souvent soudains et violents, elle est un élément majeur dans le diagnostic. L’hyperglycémie et la triade « maigreur, cétose, âge inférieur à 35 ans », sont les symptômes les plus dépister lors du diagnostic clinique d’un diabète de type 1.7
Sur le plan biologique, on réalise un dosage de la glycémie sur plasma veineux. Si la glycémie est supérieure à 2g/L ou 11,1 mmol/L le diagnostic de diabète peut être posé.19 Il est
néanmoins recommandé d’effectuer au moins 2 dosages avant d’affirmer le diagnostic.8
Le bilan biologique ne se limite pas à la seule glycémie veineuse. D’autres paramètres sont à prendre en compte pour suivre l’évolution de cette décompensation révélatrice du diabète tels que :
- L’ionogramme sanguin et urinaire avec dosage du sodium, du potassium, des chlorures, de l’hématocrite et de la protidémie pour rechercher les signes de déshydratation8
- Les gaz du sang pour rechercher les signes d’acidose8
La recherche dans les urines, à l’aide de bandelettes urinaires, d’une glycosurie et d’une cétonurie massive (suite à la carence insulinique)20 doit, obligatoirement, être réalisée pour diagnostiquer une acidocétose diabétique.19
__________________________
19 : Vidal Recos 2016, 6e éditions, sous la direction du Pr Charles Caulin, « diabète de type
1 », éditions diffusions Flammarion, septembre 2015, 2799 p.
20 : PDF du DESU MAD Marseille 2016, « le diabétique à domicile : Insulinothérapie,
surveillance et matériels », Dr Thierry AUGIER, laboratoire de biochime fondamentale, moléculaire et clinique, Faculté de Pharmacie de Marseille, 89 p.
Les dosages immunologiques sont généralement réalisés une fois que le cap aigu est passé19, et seulement en cas de doute sur l’étiologie.11 Cependant, ils peuvent également être utilisés pour le diagnostic de la phase de pré-diabète chez les enfants ou sur la fratrie d’un diabétique de type 1, afin de permettre une prise en charge plus précoce. On les réalise aussi chez les sujets jeunes présentant une glycémie à jeun entre 1,10 et 1,26g/l.11
Un typage HLA est notamment nécessaire pour connaitre les prédispositions familiales.8
Comme décrit dans la partie « 4. Etiologie », les paramètres immunogénétiques sont les auto-anticorps dirigés contre nos propres cellules béta pancréatiques :
- Anticorps anti-glutamate décarboxylase : bons marqueurs de dépistage (prévalence : ≈ 80% des diabétiques de type 1).
- Anticorps anti-IA2 (Islet Antigen 2) : marqueurs d’évolution rapide vers un diabète.
Ces 2 anticorps sont les plus demandés pour le diagnostic étiologique d’un diabète ou pour diagnostiquer la phase pré-diabétique.
- Anticorps anti-insuline : marqueurs généralement utilisés chez l’enfant de moins de 4ans, leur prévalence est inversement proportionnelle à l’âge du patient.
- Anticorps anti-îlots de Langerhans : généralement dosés en cas de discordance du bilan auto-immun par immunofluorescence indirecte sur coupe de pancréas.11
- Anticorps anti Trans-glutaminase : à la recherche d’une maladie cœliaque.
Si les marqueurs s’avèrent négatifs, l’élimination d’un diagnostic de diabète de type 1 est normale. Cependant les diabètes secondaires, type pancréatite chronique, alcoolisme ou encore hémochromatose sont eux, possible.7
Le peptide C est un polypeptide de connexion contenant 31 acides aminés et ayant une masse moléculaire de 3021 Daltons. Lors de la biosynthèse de l’insuline, le clivage protéolytique du précurseur de l’insuline (Pro-Insuline) donne la molécule d’insuline et le peptide C. Ces derniers sont, après stockage dans les granules de sécrétions de l’appareil de Gogi des cellules béta pancréatiques, sécrétés en quantité équimolaire dans le sang.
Les rôles de ce peptide sont multiples, mais il est surtout un marqueur de la sécrétion insulinique.
En ce qui concerne sa mesure, elle s’effectue à la suite d’une prise de sang. Les résultats sont rendus 1 à 2 jours maximum suivant celle-ci. Ce test se réalise seulement en cas de doute lors des cas cités ci-dessous :
- Différencier un diabète de type 1 d'un diabète de type 2 et ainsi évaluer la fonction résiduelle des cellules béta pancréatiques dans le diabète de type 1.
- Faire un choix parmi les différentes thérapeutiques proposées. - Vérifier le succès d’une greffe.
- Surveiller après une pancréatectomie.
Les valeurs normales du peptide C sont comprises entre 0,37 et 1,47 nmol/L. Une diminution de celles-ci diagnostiquerait un diabète de type 1 lié au fait que le pancréas est incapable de produire de l’insuline, tandis qu’une normalité ou une augmentation du taux serait en faveur d’un diabète de type 2.
La mesure du peptide C basal est préférée à la mesure du taux d’insuline car la concentration du peptide est moins variable dans le temps et n'est pas perturbée par la présence d'anticorps anti-insuline.21
__________________________
21 : Site Internet du Centre Hospitalier Universitaire de Liège, Référentiel des examens
Biologie Clinique – Génétique – Anatomie et Cytologie Pathologique, C-PEPTIDE http://www.chu.ulg.ac.be/jcms/c_351697/c-peptide, consulté le 05/10/2016
Le Glucagon est une hormone sécrétée par les cellules alpha pancréatiques qui se compose de 29 acides aminés et pesant 3,5 kDa22. Celui-ci permet d’augmenter la glycémie (par induction de la glycogénolyse et de la néoglucogenèse) il s’agit donc, d’une hormone polypeptidique hyperglycémiante.22
Le test de stimulation au glucagon est réalisé à la suite d’une prise de sang dosant : glycémie, insulinémie, pro-insuline, peptide C et βOH butyrate23. L’injection de glucagon qui
suit, permet de stimuler la sécrétion de peptide C, qui voit ses valeurs augmenter de 1,5 à 2 fois le taux de base dans un cas non pathologique. 24
Dans le diabète de type 1, le taux de base est bas et il n’augmente guère après stimulation par le glucagon. Par ailleurs, il peut exister une sécrétion résiduelle au début de la maladie, qui permet d’observer la non destruction de toutes les cellules bêta. Ce test a pour objectif de témoigner de la « non capacité » de l’organisme à contrôler naturellement sa glycémie.24
__________________________
22 : PDF de A. GRIMALDI, « Glucagon » - http://www.lab-cerba.com/pdf/0262F.pdf,
consulté le 05/10/2016
23 : Site Internet du Centre Hospitalier de Pau, « Tests dynamiques Endocriniens », Test au
Glucagon, http://www.ch-pau.fr/Labo/Niveau1/Tests-dynamiques-endocriniens.pdf, consulté le 05/10/2016
24 : PDF de O. GAILLARD, « Le peptide C » - http://www.lab-cerba.com/pdf/0388F.pdf,
7 SIGNES CLINIQUES
Les signes cliniques évocateurs de cette pathologie sont généralement explosifs, brutaux (« le coup de tonnerre dans un ciel calme »)7 et provoquent dans la majorité des cas une décompensation soudaine de l’organisme.
Cette décompensation peut provenir de :
- Repas avec ingestion massive de sucrerie surtout chez le jeune enfant, - Choc émotionnel et stress,
- Episode infectieux dans les semaines précédentes (virus type grippe/rubéole congénitale/coxsackie B4) car ils sont responsables de la sécrétion de cytokines favorisant le développement de la réaction auto-immune pancréatique18 …).19
On retrouve chez un jeune sujet (< 20 ans généralement)11, un syndrome cardinal comprenant une asthénie8, une polyuro-polydipsie7 (certains enfant recommençant même à
uriner au lit, ou veulent boire l’eau de leur bain19) mais aussi un amaigrissement malgré une
polyphagie7. Cependant, une augmentation de l’obésité dans les sociétés industrialisées actuelles peut entrainer une absence de la maigreur.7
L’examen clinique associe généralement : - Déshydratation19
- Haleine sentant plus ou moins l’acétone19
- Légère fonte musculaire7
- Exceptionnelle hépatomégalie par stéatose possible8
- Dyspnée de Kusmall, diagnostic d’acidose (inspiration profonde, suivie d’une courte pause en inspiration forcée et d’une expiration brève et gémissante, à laquelle succède une nouvelle pause)7
- Troubles visuels transitoire (anomalies de la réfraction constatées surtout dans les jours suivant la normalisation glycémique après l’introduction de l’insuline)7
Par ailleurs, il faut quand même noter que cette sémiologie très classique ne résume pas tous les modes d’entrée dans la maladie, tels que l’hyperglycémie de découverte fortuite, le diabète gestationnel ou le bilan familial.7
8 COMPLICATIONS
8.1.1 HYPOGLYCEMIE ET COMA HYPOGLYCEMIQUE
L’hypoglycémie est définie par une diminution du taux de sucre dans le sang26 (inférieur à
0.60 g/L ou 3,3 mmol/L) liée à une inadaptation momentanée entre le traitement et la situation du patient39. Ainsi chez le diabétique de type 1, elle « constitue le prix à payer pour l’obtention d’un bon contrôle glycémique global mais est, aussi, l’obstacle majeur à l’obtention de ce bon contrôle ».10
Il existent différentes causes : psychologiques voire psychiatriques, mauvaise perception des hypoglycémies, repas insuffisants ou sautés, exercice physique non programmé avec mauvaise adaptation de l’insulinothérapie, erreurs dans la réalisation de l’injection d’insuline, objectifs glycémiques trop ambitieux par rapport à la prise en charge globale, adaptation des doses insuliniques trop brutale, prise de médicaments potentialisant les hypoglycémies (IEC, anticalciques, fibrates, β bloquant non cardio-sélectifs).10
Signes cliniques :
- Les signes dysautomiques : sueurs, palpitations, tremblements, faim.
- Les signes neuroglucopéniques : troubles de la concentration, difficultés à parler, incoordination motrice, sensation d’ébriété.
- Les signes non spécifiques : fatigue brutale, céphalées, nausées, paresthésies péri buccales, diplopie.
- Les autres signes : nervosité, irritabilité, sensation de froid, angoisse, agressivité, accès d’émotion (euphorie/tristesse), somnolence détectable par l’entourage, pâleurs, regard dans le vide/fixe, amorphe.
Figure 6 : Exemples de signes cliniques de l'hypoglycémie
Lorsque les hypoglycémies sont trop fréquentes ces symptômes s’estompent, entrainant la diminution des signaux d’alertes lancés par l’organisme, les rendant même indétectables par le patient. Il est donc fondamental, même en l’absence de signes cliniques, de s’inquiéter des valeurs glycémiques inférieures à 0,6g/L.26
« Tout symptôme, toute manifestation rapide ou brutale chez un diabétique de type 1 doit être considéré a priori comme une hypoglycémie ».10
Une hypoglycémie non traitée peut évoluer en coma hypoglycémique d’installation rapide, cliniquement agité avec tachycardie, sueurs, crise convulsive et manifestation focalisées. Le stéréotype du coma hypoglycémiques est toujours semblable pour un même individu.10 Le traitement se fait alors par voie parentéral à l’aide de perfusions de glucose ou dans un cas de plus grande urgence, par injection de glucagon.39
La confirmation diagnostique fait suite à une glycémie capillaire réalisée par le patient lui-même ou par une personne de l’entourage en fonction de son état de santé. Dans la majorité des cas, même sans traitement, les hypoglycémies du diabétique sont réversibles et sans séquelles. Il est donc fondamental que les patients n’aient pas d’appréhension face à l’hypoglycémie car celle-ci entraverait la possibilité d’un bon contrôle glycémique global.10
Le traitement de l’hypoglycémie s’appelle un « resucrage »39, il comporte 3 étapes : - Mesurer sa glycémie,
- Absorber sans délai 15 grammes de glucides (fonction du poids de la personne = 0,3 grammes de glucide par kilo de poids corporel),
Figure 7 : Type d’aliment permettant un resucrage efficace39
8.1.2 HYPERGLYCEMIE ET ACIDOCETOSE
Toute valeur dépassant 6 mmol/L peut être qualifiée d’hyperglycémie. Il est donc important pour le diabétique de type 1, de déterminer des valeurs cibles lui permettant de réduire au maximum ses phases néfastes d’hyperglycémiques.26
Ces objectifs sont définis avec le médecin et sont fonction de l’âge du patient, de la présence ou non de complications et/ou d’une autre pathologie.
Par exemple, un adulte de 25 ans atteint d’un type 1 sans complication et sans autre maladie aura un objectif glycémique :
- 0,80 à 1,20 g/L, avant les repas
- < à 1,40 g/L, 2 heures après les repas.39
Les risques de l’hyperglycémie : 39
- Si les hyperglycémies sont modérées et ponctuelles, il n’y a pas de risque pour la santé.
- Si une glycémie reste très élevée pendant un laps de temps important, il y a un risque de complication aiguë (décompensation hyperglycémique).
- Si le nombre d’hyperglycémie au cours du temps est trop élevé, le diabète n’est pas bien équilibré et l’hémoglobine glyquée est trop élevée. Il y a, de ce fait, une augmentation du risque de développer des complications chroniques.
Différents facteurs peuvent être mis en cause lors d’une hyperglycémie : le manque d’insuline (ajustement insuffisant ou omission de doses), un apport excessif de glucides ou du « grignotage », le stress psychologique (par production d’adrénaline et de cortisol qui ont un effet hyperglycémiant) ou physique (infections) et/ou tout simplement, la peur de l’hypoglycémie faisant souvent suite à une mauvaise expérience lors d’un épisode hypoglycémique sévère.26
Le traitement de l’hyperglycémie se réalise par l’ajout d’une dose d’insuline rapide (10% de la dose totale journalière d’insuline). Suite à cela on réalise une nouvelle glycémie capillaire ainsi qu’une bandelette urinaire, permettant de vérifier le taux d’acétone urinaire. Ce taux permet de connaitre les répercussions métaboliques dues à l’hyperglycémie sur l’organisme.26
Ces possibles répercussions apparaissent lorsque l’organisme en déficit d’insuline ne peut plus utiliser le glucose sanguin et puise dans ses réserves graisseuses comme seconde source d’énergie. La dégradation de ses cellules graisseuses provoque alors une production importante de déchets appelés : corps cétoniques. L’accumulation de ces derniers entraine une acidification du sang et c’est l’acidose diabétique.26
Cette acidose a pour conséquence des vomissements associés à une production importante d’urine, entrainant de ce fait, un état de déshydratation (bouche sèche, yeux creusés et peau moins élastique allant jusqu’à l’altération de la conscience).
Chez l’enfant et l’adolescent, les causes d’acidose sont souvent plus complexes. Elles permettent la découverte fortuite du diabète dans 25 à 50 % des cas, mais chez ce type de population elle est souvent dû à une omission de dose d’insuline : soit par refus d’accepter la maladie, soit par désir de perdre du poids (plus souvent chez l’adolescent) ou encore, suite à une mauvaise supervision du jeune diabétique par son entourage (autonomisation trop rapide d’un enfant).26
Il est important de noter qu’une infection étant une source de stress, elle peut provoquer une résistance à l’insuline. Il est cependant rare qu’une infection seule entraine une acidose. Elle fait dans la majorité des cas suite à un mauvais contrôle du diabète au départ.26
8.2.1 MICROANGIOPATHIES
Les microangiopathies regroupent l’ensemble des lésions de la membrane basale constatées sur les petits vaisseaux (artères, veines et capillaires de diamètre inférieur à 30 µm).10
Elles sont la conséquence de 4 phénomènes :
- La glycation (liée à l’hyperglycémie chronique), - La prolifération de facteurs de croissance tissulaires,
- Le stress oxydatif par accumulation de produit de dégradation (résidus carbonyles) causé par l’augmentation de radicaux libres,
- Les voies parallèles du métabolisme du glucose (type voie des polyalcools) par accumulation de sorbitol et de fructose provoquant une hyper tonicité et un déséquilibre électrolytique des cellules.10
8.2.1.1 LES ATTEINTES OCULAIRES
La complication majeure concernant le territoire oculaire est la Rétinopathie diabétique. Elle représente la première cause de cécité dans les pays industrialisés.
Elle est définie par une ischémie rétinienne (par vasodilatation chronique avec altération des parois des vaisseaux, ainsi qu’une modification des constituants de plasma) suivie d’une réparation aberrante de la rétine (développement de néovaisseaux fins et fragiles puis de l’apparition de tissu glial entrainant une rétractation et un décollement de la rétine).
Le développement de cette pathologie est causé par deux facteurs principaux :
- l’ancienneté du diabète (avec une prévalence allant jusqu’à 70% si le diabète a plus de vingt ans)
- le bon contrôle glycémique (fréquence et sévérité augmentées si le diabète est mal contrôlé).
Elle se manifeste le plus souvent par une plainte du patient sur une baisse de son acuité visuelle accompagnée de perceptions visuelles anormales (brouillard, fumée, taches…). Il est alors indispensable et urgent de réaliser un bilan ophtalmologique (examen du fond d’œil et angiographie à la fluorescéine).
Pour le traitement, « Seul le bon contrôle glycémique est capable d’empêcher ou de retarder l’apparition de la rétinopathie »10. A un stade évolué de la pathologie, il est possible de faire
de la photocoagulation pan-rétinienne (empêchant les néovaisseaux de saigner) ou une virectomie.
Il est donc recommandé à tous les diabétiques de réaliser un bilan ophtalmologique annuel.10
8.2.1.2 LES ATTEINTES RENALES
La néphropathie diabétique est la complication la plus courante au niveau rénal chez le diabétique de type 1. Elle est visible dans 40 à 50% des cas après plus d’une vingtaine d’année de diabète.
Physio-pathologiquement, l’hyperglycémie chronique entraine une dilatation des capillaires glomérulaires, favorisant la filtration glomérulaire et augmentant, ainsi, le passage d’albumine dans l’urine primitive. Par la suite, le nombre de glomérules fonctionnels diminuent, engendrant une protéinurie encore plus importante, elle-même augmentant la tension artérielle. Le cercle vicieux de la néphropathie est alors en place.
En référence à la physiopathologie, le diagnostic de cette complication se fait par la présence de protéines dans les urines (albumine). Il se réalise à l’aide de bandelettes urinaires adaptées.
L’attitude thérapeutique sera différente s’il s’agit d’une microalbuminurie ou d’une macroalbuminurie.10
Microalbuminurie Macroalbuminurie / ! \ Seule période où l’on peut freiner ou
stopper l’évolution.
- Objectif prioritaire : bon contrôle glycémique (HbA1c < à 7 % ou 7,5 %). - Régime pauvre en protéine.
- Traitement anti-hypertensif pour éviter la progression de l’atteinte rénale (exercice physique, restriction sodée, IEC, antagonistes calciques +/- diurétiques, β bloquants)
Cas de la microalbuminurie sans hypertension : IEC avec augmentation des doses jusqu’à disparition de l’albumine urinaire.
- Rester exigeant sur le bon contrôle glycémique, car même si l’efficacité sur la macroalbuminurie n’est pas prouvée, il reste très important pour la non-évolution
des autres complications
microangiopatiques.
- Traitement anti-hypertensif identique. - Traitement substitutif dès que l’on atteint
le stade d’insuffisance rénale terminale avec une clairance de la créatinine < à 20 mL/min (hémodialyse ou dialyse péritonéale ambulatoire continue voir transplantation rénale).
Figure 8 : Divergences entre microalbuminurie et macroalbuminurie
8.2.1.3 LES ATTEINTES NEUROLOGIQUES
L’atteinte principalement observée chez les diabétiques est la Neuropathie diabétique. Elle est présente dans 7,5 % chez les diabétiques nouvellement découvert, ce qui rend sa prévalence égale à 50 % après plus de vingt-cinq années de diabète.
Anatomiquement, on retrouve une démyélinisation d’origine métabolique (hyperglycémie chronique) entrainant un ralentissement de la conduction nerveuse. Elle rassemble par définition, toutes les atteintes neurologiques en rapport avec le diabète qui s’étendent de l’encéphale aux muscles :
- La polyneuropathie = douleurs et atteintes de la sensibilité profonde.
- Multi/Mononévrite(s) = symptomatologies motrices (force musculaire), sensitives (douleurs vives, nocturnes avec un caractère migratoire) et des réflexes (diminution voir abolition sur le territoire atteint).
- Neuropathie motrice proximale = unilatérale et concernant particulièrement le membre inférieur au commencement avec atteinte globale (motrice, sensitive, végétative)
- Autres : amyotrophie diabétique, mal perforant plantaire.
Plusieurs examens peuvent être demandés pour une identification plus précise (mesure de la vitesse de la conduction nerveuse, altération des paramètres du réflexe d’Hoffman, ponction lombaire, biopsie nerveuse), mais l’examen clinique du patient reste systématique.
Concernant le traitement, la prévention par un bon contrôle glycémique et une insulinothérapie optimisée constituent un point majeur. Lorsqu’une neuropathie finie par se déclarer, le traitement de la douleur par AINS, antidépresseurs tricycliques, antiépileptiques, neuroleptiques, voir même par application locale de capsicine, à une part importante dans l’arsenal thérapeutique. Quelques traitements spécifiques sont apparus mais n’ont pas encore prouvé leur efficacité (vitaminothérapie, inhibiteurs de l’aldose réductase, inhibiteurs des radicaux libres).10
8.2.2 MACROANGIOPATHIES
Les macroangiopathies regroupent l’ensemble des pathologies touchant les grosses et moyennes artères. Elles sont le plus important facteur de mortalité chez les diabétiques.10 Les plus fréquentes sont :
- La maladie coronarienne, - L’insuffisance cardiaque, - L’hypertension artérielle,
- L’arthérite des membres inférieurs.10
Physio-pathologiquement, on retrouve une athérosclérose prématurée à localisation multiples et de gravité évolutive (faisant suite aux hyperglycémies, aux microprotéinuries et à des anomalies des lipoprotéines).10
L’athérosclérose est définit par l’OMS (1954) comme « une association variable de remaniement de l’intima des artères de gros et moyen calibre consistant en une accumulation locale de lipides, de glucides complexes, de sang et de produits sanguins, de tissus fibreux et de dépôt de calcaires », cette définition expliquant ainsi la gravité des complications entrainées.48
Le diabète n’est pas le seul facteur entrainant cette athérosclérose ; le tabac, l’excès de cholestérol, l’hypertension artérielle, la sédentarité ou encore l’obésité font parties intégrantes du risque cardiovasculaire.39
__________________________
Figure 9 : Evolution de l’athérosclérose au cours du temps39
8.2.2.1 LES ATTEINTES CARDIAQUES
La FIGURE 9 explique parfaitement les 2 pathologies engendrées sur le plan cardiaque par l’athérosclérose :
- l’Angor : l’intérieur de l’artère est rétréci par une plaque de cholestérol, - l’Infarctus du myocarde : l’artère est entièrement bouchée.
On parle d’insuffisance cardiaque à la suite d’un infarctus étendu, lorsque le cœur ne peut plus jouer son rôle de « pompe ».
Cliniquement, le patient ressent une douleur dans la poitrine pouvant irradier dans la mâchoire et le bras gauche. Chez le diabétique atteint de complications neurologiques, ces symptômes peuvent ne pas être ressentis et l’on découvre alors l’angor ou l’infarctus (selon le stade) sur les bilans biologiques.
Les examens permettant le diagnostic sont fonction de la situation (ECG d’effort, scintigraphie myocardique, échographie d’effort, coronoscanner) mais le seul pouvant montrer « l’état » à l’instant T des artères est la coronographie.
Concernant le traitement, il est impératif de suivre les règles de prévention : - Bonne hygiène de vie,
- Contrôle du diabète, de la tension artérielle et du cholestérol, - Arrêter la consommation de tabac,
- Réaliser son contrôle annuel chez le cardiologue avec électrocardiogramme.
Lorsque les artères sont bouchées, et comme il n’est pas encore possible de faire régresser l’athérosclérose, on réalisera une angioplastie avec pose de stent ou un pontage cardiaque pour permettre la revascularisation des artères. Ces interventions seront suivies d’un traitement médicamenteux essentiel pour éviter la récidive appelé : BASIC.
(B = Bétabloquant, A = Aspirine faible dose, S = Statine, I = Inhibiteurs de l’enzyme de conversion, C = Contrôles des autres facteurs de risques cardiovasculaires).39
8.2.2.2 LES ATTEINTES ARTERIELLES
Comme expliqué précédemment l’athérosclérose est un processus qui atteint les artères du cœur mais également celles du cerveau et des jambes.
En effet, au niveau cérébral, le manque de flux sanguin entraine une carence en oxygène qui favorise le risque d’Attaque Ischémique Transitoire voir même d’Accident Vasculaire Cérébral. Ce dernier pouvant aller jusqu’à la paralysie complète ou le décès du patient si le territoire neuronal atteint touche une fonction vitale de l’organisme.
Au niveau des membres inférieurs, la clinique évoquée par les patients est plutôt à type de « crampes à l’effort », appelées aussi claudication intermittente, qui s’estompent à l’arrêt de l’effort. A cette étape, l’artère concernée n’est que partiellement obstruée. Lorsque que celle-ci se bouche complètement on observe alors des ulcères des bords des pieds ou des jambes (différents des ulcères veineux).
Pour éviter ses complications, le personnel médical effectue au moindre signe ou en prévention selon l’historique du patient, un écho-doppler artériel. A la suite de cet examen et si les résultats sont en faveur d’artères obstruées, un angioscanner ou une artériographie seront réalisés.
Concernant le traitement, il est similaire à celui réalisé lors d’atteintes cardiaques (stents, pontages), tout comme les éléments préventifs (facteurs de risques cardiovasculaires).
Cas particuliers : Les atteintes des pieds
L’association de la neuropathie (décrit précédemment) et de l’atteinte artérielle sont responsable d’une pathologie appelée : Pied diabétique. Cette dernière peut aller jusqu’à l’amputation.
Le dépistage de cette complication se réalise par « le test au monofilament » : le médecin pose sur la plante du pied du patient un filament calibré.
- Si le patient ressent ce filament, la neuropathie n’est pas extrêmement développée et le risque de mal perforant plantaire est moindre.
- A contrario, si le patient n’a aucune sensation, il est impératif pour ce dernier de vérifier ses pieds quotidiennement ! 39
8.2.3 SENSIBILITE AUX INFECTIONS
Lorsque l’hémoglobine glyquée est dans les normes (inférieur à 7 %), le risque infectieux est le même que celui de la population générale. En revanche, lorsque le contrôle glycémique n’est pas suffisant, l’ensemble des défenses de l’organisme (globules blancs, anticorps) est impacté par ce surplus de sucre. Leur présence et leur efficacité étant diminuées, cela favorise alors, l’entrée de micro-organismes (Bactérie = otites, abcès dentaire, furoncles / Virus = rhume, grippe, gastro-entérite / Champignons = mycoses des plis, orteils, ongles).
La prévention reste la partie la plus importante dans cette lutte face aux infections. Elle se regroupe autour de 4 grands piliers :
- S’assurer du meilleur équilibre glycémique possible
- Respecter les règles de base de l’hygiène (mains, corporelle, buccal, alimentaire et l’entretien du logement)
- Retrouver une bonne hygiène de vie (alimentation équilibrée, sommeil suffisant, exercice physique régulier, éviction du tabac)
- Mise à jour des vaccinations !
Il faut noter également que les infections déséquilibrent le diabète par action sur les hormones hyperglycémiantes en augmentant le besoin en insuline.
Dans ce cas, le contrôle glycémique doit être d’autant plus rigoureux et régulier pour éviter l’hyperglycémie majeure voir même l’acidocétose. Certains signes cliniques (comme la perturbation de l’appétit, le vomissement, la diarrhée) sont des situations que les parents et/ou l’enfant doivent savoir gérer très précautionneusement car le risque de décompensation grave est important. 39
8.2.4 LES AUTRES COMPLICATIONS
Les atteintes bucco-dentaires :
Bouche sèche : L’augmentation de sucre dans la salive entraine une diminution de production de celle-ci, pouvant engendrer des mycoses buccales, des ulcères voir même des caries.
Maladies parodontales : L’augmentation du risque d’infections facilite le développement de gingivites et de parodontites puisqu’elles sont causées par la formation de plaque dentaire et la présence de bactérie.
Attention au cercle vicieux : problème bucco-dentaire/équilibre glycémique, qui s’installent beaucoup plus rapidement chez le diabétique que chez les autres individus. Il est alors important d’inculquer aux enfants, dès leur plus jeune âge, l’importance d’une bonne hygiène buccale. 39