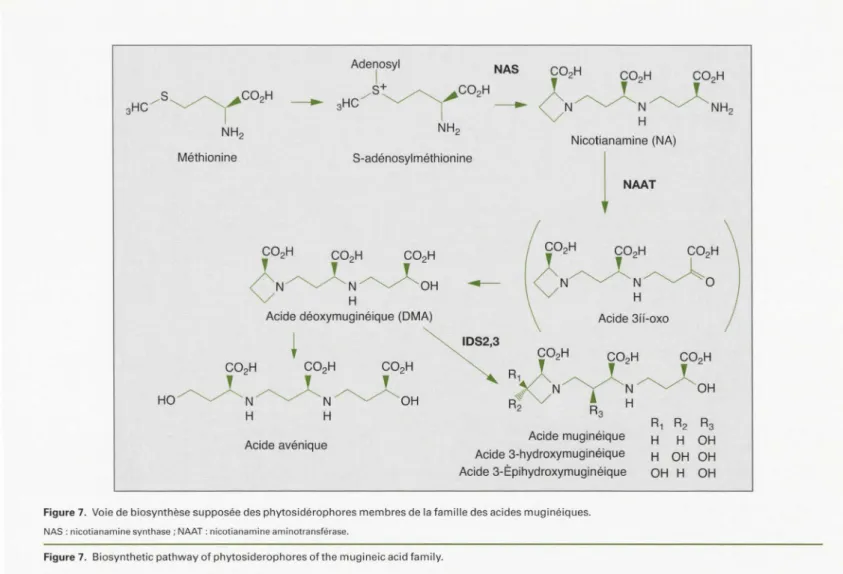
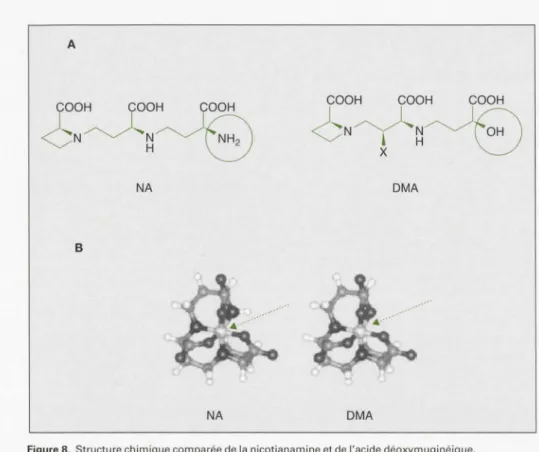
Synthèse
Acquisition et gestion du fer par les plantes
Jean-
Fr
anço
i
s
Briat
Grégory Vert
Biochimie et physiologie moléculaire
des plantes,
Centre national de la recherche scientifique (UMR 5004),
Université Montpellier-11,
Institut national de la recherche agronomique et École nationale supérieure d'agronomie,
Place Viala,
F-34060 Montpellier cedex 1
<briat@ensam.inra.fr>
lirés à part : J.-F. Briat
Résumé
L'homéostasie du fer doit être conLrôlée tant au niveau cellulaire que de l'organisme entier pour fournir suffisamment de ·e métal essentiel à la croissance et au développement des
plantes, tout en évitant un excès qui pourrait être toxique. La carence en fer conduit à la chlorose chez les plantes, caractérisée par un jaunissement interne1vaire. Ce phénotype
révèle l'impact du manque de fer sur le conLenu des feuilles en chlorophylle et en
caroLénoïcles. La diminution de l'abondance en pigments photosynthétiques corrèle avec
la perte des capacités photochimiques des chloroplastes. La carence en fer altère également la respiration miLochonclriale et la fixalion de l'azote atmosphérique clans les
nodules des légumineuses. Ces perturbations méLaboliques sont étroitemenL liées au fait que le fer est un métal de transition indispensable comme cofacteur de nombreuses
réactions reclox cellulaires. Pour assurer l'acquisition du fer à partir du sol, sa distribution
aux différents organes et tissus d'une plante, et sa distribution intracellulaire entre les
différents organites, plusieurs membranes doivent être traversées par ce métal. De
nombreux transp rteurs impliqués clans ces fonctions ont été caractérisé au niveau moléculaire ces dix dernières années. La nécessité d'une régulation inLégrée de ces
différents systèmes de transpon requis pour la circulation du fer clans la plante entière est évidente, et plusieurs mutants altérés clans ces processus de signalisation ont été décrits.
À
l'inverse, les plantes se trouvant confrontéesà
un excès de fer mettent en place despossibilités de stockage de ce métal pour contrôler sa réactiviLé toxique avec l'oxygène.
À
ce titre, l'apoplasme, les vacuoles et les ferritines des plastes jouent un rôle important.
Mots clés
: Pr
oductions végétales; métabolisme.Summary
Iron homeostasis in plants
Iron homeostasis at cellular level and in the whole organism must be balanced in orcler to supply enough iron for the plant growth and development, and to avoicl excessive, toxic
levels. Iron cleficiency in plants leads to the chlorosis syndrom, characterized by a leaf
inte1veinal yellowing. Such a phenotype reveals the impact of iron deficiency on
chloropbyll and carotenoid concentrations. This clecrease in pbotosynthetic pigment
abunclance correlates with a I wering of the chloroplast photochemical capacities. Iron cleficiency also alters mitochondrial respiration and nitrogen fixation in the nodule of legumes. These defects are mainly due to the fact that iron is a major cofactor in many cellular reclox processes. In order to perform iron uptake from the environment, iron distribution to various organs and tissues, and iron intracellular compartmentalization, various membranes must be crossed by this metal. Many transporters involved in these
functions have been characterized at molecular level this last decacle. An integrated regulation of these transport systems required for iron t:rafficking in the whole organism is
therefore necessary, and various mutants affected in these signaling processes have already been characterized. On the opposite, in case of iron excess iron must be bufferecl
because of its high reactivity with oxygen. This is achieved through its storage in the apoplasm and vacuoles and by way of the iron storage protein ferritin founcl within the
plastids.
Key
worcls:
Vegetal productions; metabolism.D
f
un
point
d
e v
u
e a
nthropo
-m
o
rphjqu
e,
l
'
im
portance
bi
o-l
og
i
q
u
e
du f
e
r
est
assoc
i
ée
aux
pat
h
o
l
og
i
es
diverses dont
so
u
ffrent
l
es
ê
tr
es
hum
a
in
s
poss
é
dant un m
é
tabol
i
sme
d
u
f
e
r
ano
rm
a
l.
Pa
rmj
ces
pat
h
o
l
og
i
es,
l'
aném
i
e
li
ée à
l
a ca
r
e
n
ce e
n f
e
r
co
n
s
titue
l
e
problème
nutriti
o
nnel
J
e
p
lu
s co
ur
a
nt
,
affecta
nt
quatre
à c
inq
mi
lli
a
rd
s
d
'
êt
r
es
humains
,
dont
un
e
grande partie
d
a
n
s
l
es
pays
du
Sud
. L
a
prin
c
ip
a
l
e so
ur
ce
de
f
e
r
clans
l
es
r
ég
im
es
a
lim
enta
ir
es
d
es
pay
s e
n
déve
l
oppeme
nt
p
r
ov
i
ent
d
es végé
t
a
u
x.
La
co
mpr
é
h
e
n
s
i
o
n d
es
m
éca
ni
s
m
es
assu-ra
nt l
a
r
ég
ul
a
ti
o
n d
e
l
'
hom
éostas
i
e
du
f
e
r
c
h
ez
l
es
p
l
a
n
tes
apparaît
a
in
s
i indi
spe
n
sa
-ble
, n
on se
ul
e
m
e
nt
à
l
'a
m
é
li
oratio
n
de
l
a
productivité de
ce
LJ
es-c
i
,
mai
s a
u
ss
i
à
l
a
sa
nt
é
des
ê
tr
es
humain
s
.
Rôles métaboliques
du fer
chez les végétaux
L
e
fer
co
n
st
i
tue
l
e q
u
at
ri
è
m
e é
l
émen
t
l
e
plus
abo
nd
ant à
l
a s
urfa
ce
de notre p
l
a-n
ète.
Ma
l
g
r
é cette
r
e
l
ative abondance
a
u
ni
vea
u
des
r
oc
h
es co
n
s
titu
a
nt
l
a c
r
o
Cite
terrest
r
e
,
l
e
f
e
r n
'es
t pr
ése
nt
qu
'
e
n
fa
ibl
e
quantité
d
a
n
s
l
a
mati
è
r
e v
i
va
nt
e (de 50 à
1
00
p
g.g-
1de
m
at
i
è
r
e sèc
h
e
cl
a
n
s
l
es
feuilles
,
par
exe
mpl
e
(11.
Cependant
,
l
e
f
e
r demeur
e
un
é
l
é
ment
essent
iel
partici-pant
à
de
n
o
mbr
e
u
x
p
r
ocess
u
s
m
é
t
abo
li
-ques
indi
s
p
e
n
sab
l
es à
l
a vie
d
e
l
a p
l
a
nt
e
.
L'imp
o
rt
a
n
ce
m
é
t
abo
liqu
e
d
e
l'
é
l
é
m
e
nt
fer
pro
v
i
e
n
t
d
e ses
propr
i
é
t
és c
himiqu
es.
Il
peut
fo
rm
e
r ju
sq
u
'à six
li
aisons
d
e
coo
rdin
a
ti
o
n
e
n
accep
t
a
nt un
e
paire
d
'
é
l
ectro
n
s s
ur
chacune
d
e ses six
o
rbital
es
ato
miqu
es.
D
es
é
l
é
m
e
nt
s
é
l
ec
tron
éga
tif
s co
mm
e
l
'
oxygène,
l
'azote
e
t
l
e so
ufr
e
auront
l
a
ca
pacit
é
d
e se
li
e
r
avec
l
e
f
e
r.
Ce
tt
e
propr
i
é
t
é
fondamenta
l
e
permet
a
u
fe
r
de
s
'
assoc
ier
à
des
pr
otéi-n
es.
Sa
natur
e
de méta
l
d
e
transition
lui
co
nf
è
r
e
l
a capac
it
é
cl
'exjs
t
e
r
so
u
s
cieux
fo
rm
es,
l
'
un
e
r
éd
uit
e (Fe
2+,
J
e
fer ferre
u
x),
l'
a
utr
e oxy
d
ée
(Fej+,J
e
fer fe
rri
que).
Ce
tt
e
ca
pa
c
it
é
d
e
p
o
uv
o
ir
accepte
r
o
u
don
n
e
r
alternativement
un
é
l
ec
tron
,
fait
du
f
e
r J
e
cofac
t
e
ur d
e c
h
oix
de
n
o
mbr
e
u
ses
r
éac-tions
enzy
m
atiq
u
es
d
'
oxydo
r
éd
u
c
ti
o
n
. E
n
association avec
des protéines
,
l
e
fer
es
t
ainsi
impliqu
é
clan de nombreuses
r
éac-ti
ons
de transfert d
'
é
l
ectro
n
s
clans
l
a
plante.
Les protéines
à
fer
L
es
prot
é
in
es
à
f
e
r
p
e
u
ve
nt
ê
tr
e
r
egro
u
-p
ées e
n tr
o
i
s
classes
, co
rr
es
p
o
ndant
à
l
a
façon
d
o
nt
l
e
m
é
tal
es
t
coo
rd
on
n
é
a
u
x
pr
o
t
é
in
es
:
l
es protéi
n
es
f
e
r
-so
ufr
e
,
l
es
prot
é
in
es à
h
ème
e
t
l
es
prot
é
in
es
cl
a
n
s
l
esq
u
e
ll
es
l
e
fer
est d
ir
ecte
m
e
nt
li
é à
l
a
c
h
aî
n
e
protéique.
Les protéines à centre fer-soufre
Ce type
d
e
protéine
s co
n
tie
n
t
ce
qu
e
l
'
o
n
appe
ll
e
un
ce
ntre
(ou
cluster)
fer
-so
ufr
e
,
Cys
s
2-\
s
2
-co
n
st
i
tué d
'un
e assoc
iation
e
n
s
t
œc
hi
o-m
ét
ri
e
var
i
a
bl
e e
ntr
e
des
a
tom
es
d
e
f
e
r
e
t
d
e so
ufr
e
[
2).
Ces ce
ntr
es
fer-s
o
ufr
e
so
nt
associés
à
l
a
pr
o
t
é
in
e
par
l
'
int
e
rm
éd
iair
e
de
gro
up
ement thio
l
d
e
ce
rt
ains
r
és
idu
s
cys
t
é
in
e.
L
e
nombr
e
d
'
atomes
d
e
f
e
r
clans
l
es ce
ntre
s
fer-
so
ufr
e va
ri
e
de
un
à
q
u
atre
,
l
es ce
ntr
es
(
2Fe-2S)
e
t (
4Fe
-
4S) éta
nt
l
es
plu
s
r
é
p
a
ndu
s
(figure 1).
Au sein de
ces
s
tru
c
tur
es,
l
a va
l
e
n
ce
du fer p
e
ut
va
ri
e
r
,
p
e
rm
e
ttant
aux
ce
ntr
es
f
e
r
-so
ufr
e e
t
a
u
x
prot
é
in
es
co
rr
es
p
o
nd
a
nt
es
de former
un
\
Cys [2Fe-2S] Cys'
CysI
'
Cys [4Fe-4S]Figure 1. Représentation schématique des centres fer-soufre [2Fe-2S] et [4Fe-4S].
Les atomes de soufre de résidus cystéine sont représentés en vert clair et ceux impliqués dans la formation du centre
fer-soufre en vert foncé. Les deux types de centres fer-soufre sont unis à la protéine par liaison avec les groupements thiols de certains résidus cystéine de la protéine (d'après 13]).
Figure 1. Schematic representation of iron-sulfur clusters [2Fe-2S] and [4Fe-4S].
A Espace intermembranaire (Fe-S)--+---11,.__
t
FMNMatrice
NADH
Complexe IB
+
Fe Complexe Ill 2e-Succinate (FADH2) 10mm Complexe IlFigure 2. Importance du fer pour la structure et la fonction respiratoire des mitochondries.
Complexe IV
- Fe
A) Organisation des éléments de la chaine de transport d'électrons dans la membrane mitochondriale interne. La chaine respiratoire est formée de quatre complexes de transporteurs
d'électrons et de deux transporteurs (l'ubiquinone et le cytochrome c) dont la localisation est indépendante.
Fe-S: protéine à centre fer-soufre; cyt: cytochrome (d'après 131).
B) Images de microscopie électronique de mitochondries de feuilles de plantes de tabac cultivées en présence I+ Fe) où en absence 1-Fe) de fer. La flèche sur l'image -Fe indique des
inclusions denses aux électrons fréquemment observées dans les mitochondries de plantes carencées en fer. Figure 2. Iron requirements for the structure and respiratory function of mitochondria.
couple
d
'oxy
dorédu
c
tion. L
'e
n
v
ironn
e-m
e
nt d
es
prot
é
ine
s
à ce
ntr
e
f
e
r-s
o
ufr
e
leur
co
nfèr
e
une
gamme
d
e
p
o
t
e
nti
e
l
s
redo
x
trè
s é
t
e
ndue.
Du
fa
it
d
es
propriétés
citées
pr
écé
d
e
m-m
e
nt
,
le
s
protéines
à ce
ntr
e
fer-soufre
so
nt
un cons
tituant
ma
jeur de
s c
haînes de
tr
a
n
s
p
o
rt d
'
élec
tron
s
,
e
n p
a
r
t
in
il
ier
a
u
niv
ea
u d
e la
mit
oc
hondri
e.
De n
o
mbr
eu-ses
prot
é
in
es
à ce
ntr
e
f
e
r
-so
ufr
e o
nt
é
t
é
id
e
ntifi
ées
au
ni
vea
u d
e
l
a
m
e
mbran
e
inte
rn
e
d
e
la
mit
oc
hondrie (figure
2).
Ainsi
,
le co
mpl
exe
I
c
h
ez
les
animaux
co
nti
e
nt
a
u moin
s quau·e
pr
o
t
é
in
es à ce
n-tr
e
fer-
so
ufr
e (N
-1
à N
-
4), e
t
le complexe
II
a
u m
o
in
s
troi
s
(S
l
à 53).
L
e co
mpl
exe
IV
Cahiers Agricultures 2004
;
13
:
183-201
renf
e
rm
e
une
protéin
e
à ce
ntre f
er-so
ufr
e : la
prot
é
in
e
d
e
Ri
es
k
e.
L
es
m
ê
m
es
raisons ex
pliqu
e
nt la pr
ése
n
ce
d
e
protéi-nes
à
ce
ntr
e
f
e
r
-so
ufr
e a
u niv
eau
d
e
la
c
haîn
e de
u·
a
n
s
p
o
rt
d
'
é
lectro
n
s
ph
otosy
n-th
é
tiqu
es
d
es c
hl
orop
l
astes (figure
3)
Ces
prot
éines
à ce
ntr
e
f
e
r-
soufre
u
·o
uv
ées a
u
ni
vea
u
de
la
m
e
mb
ra
n
e
des
th
y
lakoïd
es
A
B
+
Fe - FeFigure 3. Importance du fer pour la structure et la fonction photosynthétique des chloroplastes.
A) Organisation de la chaîne photosynthétique de transport d'électrons.
Trois complexes membranaires sont représentés: le photosystème Il, le complexe cytochrome b6f, et le photosystème l. Le chemin suivi par les électrons est indiqué par la flèche verte. b559 : cytochrome b559 ; PO: plastoquinone; PQH2: plastoquinol; RFe-S: protéine de Rieske; b6: cytochrome b6 ; f: cytochrome f; PC: plastocyanine; Fx. accepteur X; FA: accepteur A;
Fe: accepteur B; Fdx: ferredoxine; FNR: ferredoxin-NAD+ reductase. Les protéines de Rieske, Fx, FA, Fe, et Fdx contiennent un centre Fe-S. (d'après 11491). B) Images de microscopie électronique de chloroplastes de feuilles de plantes de tabac cultivées en présence(+ Fe) ou en absence (-Fe) de fer.
Figure 3. Iron requirements for the structure and photosynthetic function of chloroplasts.
![Figure 1. Représentation schématique des centres fer-soufre [2Fe-2S] et [4Fe-4S]](https://thumb-eu.123doks.com/thumbv2/123doknet/2311992.27019/2.873.193.837.123.981/figure-representation-schematique-centres-fer-soufre-fe-fe.webp)