Solutions techniques pour l’atténuation des impacts
environnementaux liés à l’activité minière et étude
de facteurs aggravants
Thèse
Nicolas KAGAMBEGA
Doctorat en génie des eaux
Philosophiæ Doctor (Ph. D.)
Québec, Canada
Solutions techniques pour l’atténuation des impacts
environnementaux liés à l’activité minière et étude
de facteurs aggravants
Thèse
Nicolas KAGAMBEGA
Sous la direction de :
Rosa GALVEZ, directrice de recherche
Abibata OUATTARA, codirectrice de recherche
iii
Résumé
L’activité minière est source de profits économiques pour les états, les populations, contribue pour une part importante à la lutte contre la pauvreté et à la création d’emplois directs et indirects. Cependant, l’industrie minière peut être préjudiciable à l’environnement et durant toutes ses phases (exploration, développement, production et fermeture) à travers les rejets miniers générés.
Lorsque ces rejets miniers générés par l’activité minière contiennent des minéraux sulfurés, leur exposition à l’oxygène, à l’eau ou à certains microorganismes entraine leur oxydation qui peut produire un effluent acide (drainage minier acide ou DMA) susceptible de solubiliser les métaux qui ont des impacts négatifs sur l’environnement et la santé humaine.
Ces différents impacts sur l’environnement sont susceptibles d’être amplifiés à travers l’utilisation de sels de déglaçage comme fondants pendant l’hiver. En effet, dans des régions comme le Québec où la saison hivernale dure plusieurs mois, on fait généralement recours aux fondants routiers pour dégager la neige des routes et empêcher l’arrêt des travaux dans les mines durant cette période.
L’objectif de ce travail est de développer des méthodes pour la gestion des résidus miniers dans une perspective de développement durable et de protection de l’environnement à travers: la lixiviation des résidus miniers avec les acides organiques commerciaux (acide citrique, gluconique et oxalique); la neutralisation de drainage minier acide fortement contaminé par l’utilisation de la dolomie de haute pureté; l’étude des échanges chimiques entre les métaux et le chlorure de sodium dans le relargage des métaux.
Des essais en jar test suivis d’essais en colonnes ont été réalisés pour la lixiviation (avec les acides organiques commerciaux ou le sel de déglaçage et pour la neutralisation des drainages miniers acides).
Les résultats obtenus montrent que la solubilisation des métaux se fait sous l’effet uniquement des acides organiques et non sous l’influence d’enzymes extracellulaire. La lixiviation des résidus miniers par l’acide citrique à 5.10-2 g/l offre la possibilité de récupération des métaux contenus dans les résidus miniers rejetés par l’industrie minière à des concentrations commercialement intéressantes. La solubilisation des métaux étant fonction du type d’acide ou du mélange d’acide, de la concentration, des métaux et du temps. L’acide citrique qui est un acide tricarboxylique possédant trois groupes fonctionnels auxquels peuvent être associés les métaux présente les plus fortes teneurs de solubilisation. Il forme également des complexes plus stables avec des métaux
iv
comme le cuivre, le zinc et le plomb. Les mécanismes mis en jeu sont l’acidification et la complexation. Les tests d’analyses de variances montrent qu’en général, il n’existe pas de différences statistiques significatives quel que soit l’acide ou le mélange d’acides utilisé pour la lixiviation. Les essais d’extraction séquentielle sélective effectués montrent que les métaux contenus dans les résidus miniers sont d’origines litho-géniques et que ceux solubilisés appartiennent essentiellement aux fractions géochimiques échangeable, carbonatée ou à celle des oxydes et hydroxydes.
L’analyse technico-économique montre que la lixiviation des métaux contenus dans les résidus miniers serait techniquement et économiquement rentable. Elle permet par conséquent de valoriser ces résidus miniers et de préserver également l’environnement.
La dolomie pure, composée à 96% de dolomite, permet la neutralisation des effluents acides même fortement contaminés. Elle permet de tamponner des effluents acides fortement contaminés générés par des mines de cuivre ou de zinc. Toutefois, son pouvoir de neutralisation est faible pour les drainages miniers acides issus d’anciennes mines de pyrite ou fortement contaminés en fer.
Enfin, les sels de déglaçage amplifient de cinq à douze fois la solubilisation des métaux comme le zinc et le plomb. Les phénomènes mis en jeu dans la mobilisation des métaux par les sels de déglaçage sont la solubilisation des métaux consécutive à l’acidification (échanges d’ions); la chloro-complexation ; et l’association des ions sulfates avec les métaux.
v
Abstract
The mining industry is a source of economic profits for states and populations, and contributes significantly to the fight against poverty and to the creation of direct and indirect jobs. However, the activities of the mining industry can be detrimental to the environment and during all phases (exploration, development, production and closure) through the mining discharges generated. When these tailings generated by mining activity contain sulphide minerals, their exposure to oxygen, water or certain microorganisms causes their oxidation, which can produce an acidic effluent (acid mine drainage or AMD) likely to solubilize metals that have negative impacts on the environment and human health.
These different impacts on the environment are likely to be amplified through the use of de-icing salts as fondants during the winter. In regions such as Quebec, where the winter season lasts for several months, road fondants are generally used to clear snow from roads and prevent work stoppages in mines during this period.
The objective of this work is to develop methods for the management of mine tailings in a perspective of sustainable development and environmental protection through (i) leaching of tailings residues with commercial organic acids (citric acid, gluconic acid and oxalic acid); (ii) The neutralization of acid mine drainage heavily contaminated by the use of high purity dolomite; (iii) The study of chemical exchanges between metals and sodium chloride in the release of metals.
Batch tests followed by column tests were carried out for leaching (with commercial organic acids or de-icing salt and for the neutralization of acid mine drainage).
The results obtained show that the solubilization of the metals is carried out by the effect of organic acids and not under the influence of extracellular enzymes. The leaching of tailings by citric acid at 5.10-2 g/l offers the possibility of recovering the metals contained in the tailings released by the mining industry at commercially attractive concentrations. The solubilization of metals depends on the type of acid or acid mixture, concentration, metals and time. Citric acid which is a tricarboxylic acid having three functional groups to which the metals may be associated have the highest solubilization contents. It also forms more stable complexes with metals such as copper, zinc and lead. The mechanisms involved are acidification and complexation. Testing of variance analyzes shows that, in general, there are no statistically significant differences regardless of the acid or mixture of acids used for leaching. The selective sequential extraction tests carried out show that the
vi
metals contained in the tailings are of lithogenic origin and that those solubilized essentially belong to the exchangeable, carbonated or oxide/hydroxide geochemical fractions.
The technical-economic analysis shows that the leaching of the metals contained in the tailings would be technically and economically profitable. It therefore allows to value these tailings and also to preserve the environment.
Pure dolomite, composed of 96% dolomite, allows the neutralization of even highly contaminated acid effluents. It makes it possible to buffer heavily contaminated acid effluents generated by copper or zinc mines. However, its neutralizing power is low for acid mine drainage from old iron or pyrite mines.
Finally, de-icing salts amplify the solubilization of metals such as zinc and lead five to twelve times. The phenomena involved in the mobilization of metals by de-icing salts are the solubilization of metals following acidification (ion exchange); chloro-complexation; and the association of sulfate ions with metals.
vii
Table des matières
Résumé ... iii
Abstract ... v
Table des matières ... vii
Liste des tableaux ... x
Liste des figures ... xii
Liste des annexes ... xv
Liste des abréviations et sigles ... xvi
Remerciements ... xix
Chapitre I : Introduction ... 1
Chapitre II : Problématiques et objectifs ... 10
II.1. Problématiques ... 11
II.2. But et objectifs ... 16
II.3. Organisation de la thèse ... 18
Chapitre III : Revue de la littérature ... 19
III.1. Résidus miniers (RM) ... 20
III.1.1. Définitions ... 20
III.1.2. Conséquences liées aux résidus miniers ... 23
III.2. Drainage minier acide (DMA) ... 25
III.2.1. Définition ... 25
III.2.2. Formation du DMA ... 26
III.2.3. Rôle catalyseur des microorganismes ... 28
III.2.4. Impacts du DMA ... 29
III.2.5. Toxicité des métaux ... 31
III.2.7. Prévention et contrôle du DMA ... 34
III.2.8. La neutralisation du DMA ... 35
III.3. Valorisation des résidus miniers ... 37
III.3.1. Phyto-extraction ... 37
III.3.2. Gestion intégrée des résidus miniers ... 37
III.3.3. La biolixiviation ... 40
III.4. La complexation ... 42
III.5. Législation et normes environnementales au Québec ... 44
III.5.1. Loi sur les mines (L.R.Q., M-13.1) ... 44
viii
III.5.3. Règlement sur les effluents des mines de métaux (REMM) ... 46
III.6. Hypothèses de recherche ... 46
Chapitre IV : Approche méthodologique ... 47
IV.1. Matériaux ... 49
IV.2. Caractérisation des matériaux ... 51
IV.2.1. Mesures du pH et du pE ... 52
IV.2.2. Teneur en Eau (w) ... 53
IV.2.3. Pourcentage de matière organique ... 53
IV.2.4. Porosité ... 54
IV.2.5. Perméabilité ... 54
IV.2.6. Débits ... 55
IV.2.7. Granulométrie ... 56
IV.2.8. Pouvoir tampon ... 57
IV.2.9. Capacité d’Échange Cationique (CEC) ... 57
IV.2.10. Composition minéralogique par spectrométrie de diffractions aux RX et microscopie électronique à balayage (MEB) ... 58
IV.2.11. Les sulfates ... 59
IV.2.12. Concentrations totales des métaux par spectrophotométrie d’absorption atomique (SAA). ... 60
IV.2.13. Distributions géochimiques des métaux par extraction séquentielle sélective (ESS) . 61 IV.3. Lixiviation des résidus miniers par des acides organiques ... 62
IV.4. Neutralisation du DMA par la dolomie ... 63
IV.5. Influence du chlorure de sodium dans la mobilisation des métaux ... 64
Chapitre V : Résultats et discussions ... 67
V.1. Caractérisation des résidus miniers ... 69
V.1.1. Paramètres géotechniques des résidus miniers ... 69
V.1.2. Caractéristiques minéralogiques des résidus miniers ... 73
V.1.3. Paramètres physico-chimiques des résidus miniers... 75
V.1.4. Distribution géochimique des métaux lourds dans les résidus miniers ... 81
V.1.5. Caractérisation physico-chimique du drainage minier acide ... 84
V.1.6. Caractérisation de la dolomie ... 85
V.1.7. Les acides organiques commerciaux utilisés ... 91
V.1.8. Caractérisation du sel de déglaçage ... 93
V-2 : Lixiviation des résidus miniers par les acides organiques ... 96
V.2.1. Solubilisation des métaux en fonction du type d’acide ... 96
V.2.2. Solubilisation des métaux en fonction de la concentration de l’acide ... 110
ix
V.2.4. Évolution de la teneur de solubilisation des métaux en fonction du temps ... 127
V.2.5. Solubilisation des métaux par fraction géochimique ... 140
V.2.6. Effet de la température sur la lixiviation ... 148
V.2.7. Les essais en colonnes ... 149
V.2.8. Bilan de masse ... 155
V.2.9. Principaux facteurs influençant la solubilisation des métaux ... 156
V.2.10. Comparaison de la lixiviation par les acides organiques commerciaux avec la lixiviation fongique (Ouattara, 2008) ... 159
V.2.11. Analyse technico-économique de la lixiviation par l’acide citrique ... 164
V.2.12. Conclusion partielle ... 171
V-3 : Neutralisation du drainage minier acide par de la dolomie de haute pureté ... 174
V.3.1. Essais préliminaires de neutralisation en jar test ... 174
V.3.2. Essais en colonnes ... 177
V.3.3. Analyse minéralogique de la dolomie à l’issue des essais de neutralisation ... 188
V.3.4. Différents paramètres influençant l’efficacité de la dolomie ... 195
V.3.5. Conclusion partielle ... 197
V-4 : Relargage des métaux par le sel de déglaçage ... 199
V.4.1. Essais préliminaires en "jar test" ... 199
V.4.2. Paramètres suivis ... 200
V.4.3. Extraction séquentielle sélective (ESS) ... 213
V.4.4. Essais en colonnes ... 216
V.4.5. Bilan de masse ... 226
V.4.6. Comparaison de la solubilisation des métaux avec les acides organiques commerciaux et celle avec le sel déglaçage ... 227
Chapitre VI : Conclusions et perspectives ... 231
VI.1. Lixiviation des résidus miniers par les acides organiques commerciaux ... 234
VI. 2. Neutralisation des drainages miniers fortement contaminés par de la dolomie de haute pureté ... 236
VI. 3. Mobilisation des métaux par le sel de déglaçage ... 238
VI. 4. Contributions scientifiques ... 240
VI. 5. Perspectives ... 243
Bibliographie ... 245
x
Liste des tableaux
Tableau 1: Les impacts environnementaux de l’extraction minière (Winfield et al., 2002) ... 24
Tableau 2: Principales bactéries et archéobactéries associées à l’oxydation des sulfures et du fer que l’on peut retrouver dans les rejets miniers générateurs d’acide.* ... 29
Tableau 3: Principaux effets sur la santé humaine des métaux observés dans le drainage minier acide (Collon, 2003) ... 33
Tableau 4: Minéraux neutralisants dits acidivores (Aubertin et al., 2002) ... 36
Tableau 5: Modes alternatifs de gestion des résidus miniers (MEND, 2014) ... 38
Tableau 6: Tableau comparatif de la méthode de gestion intégrée et celle conventionnelle des résidus miniers (MEND, 2014) ... 39
Tableau 7: Composition du sel de déglaçage ... 49
Tableau 8: Paramètres et méthodes de caractérisation des matériaux ... 52
Tableau 9: Caractéristiques granulométriques des résidus miniers ... 70
Tableau 10: Paramètres physico-chimiques et teneurs en métaux totaux des résidus miniers ... 75
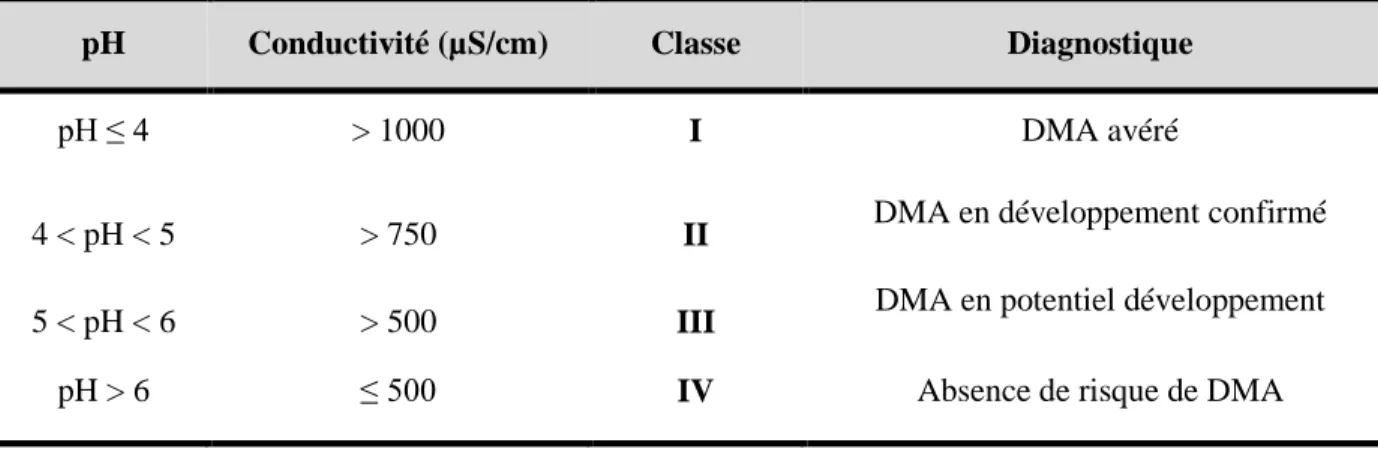
Tableau 11: Risque potentiel de génération de DMA à partir du pH et de la conductivité (Brunet et Coste, 2000) ... 76
Tableau 12: Capacité d’échange cationique des résidus miniers ... 78
Tableau 13: Teneurs en métaux totaux des résidus miniers ... 79
Tableau 14: Grille des critères génériques pour les sols tirée de la politique de protection des sols et de réhabilitation des terrains contaminés (MDDEFP, 2013)... 80
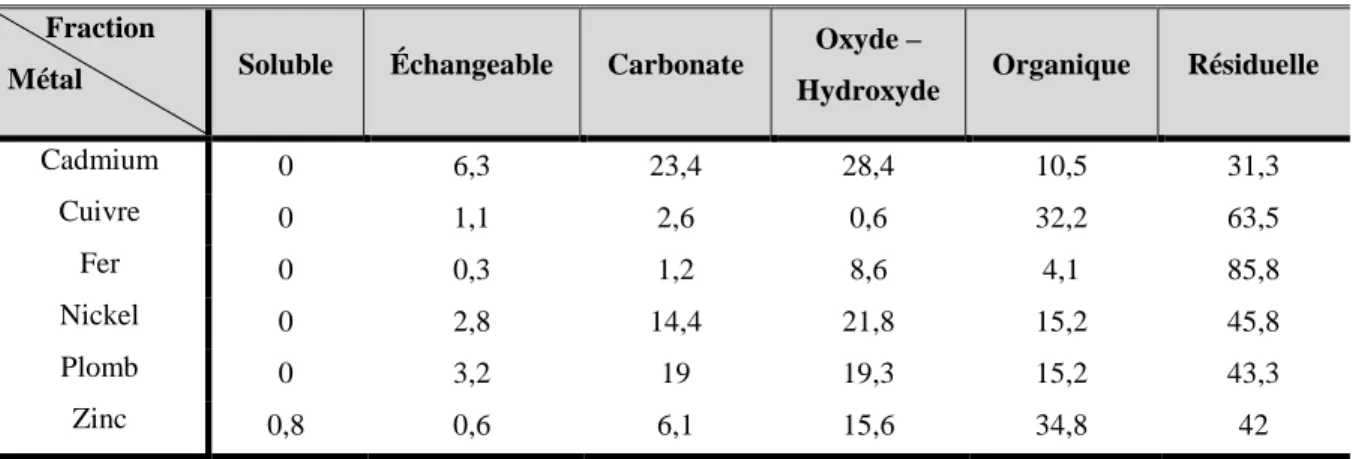
Tableau 15: Pourcentage de rétention des métaux lourds par fraction géochimique ... 82
Tableau 16: Séquence de rétention des métaux lourds dans les différentes fractions géochimiques 83 Tableau 17: Séquence de sélectivité des métaux ... 83
Tableau 18: Paramètres physico-chimiques du drainage minier acide ... 84
Tableau 19: Caractéristiques granulométriques de la dolomie... 86
Tableau 20: Exigences pour le sel de déglaçage des routes (source : norme MTQ, 2011) ... 94
Tableau 21: Quelques paramètres physico-chimiques du sel de déglaçage ... 94
Tableau 22: Matrice de corrélation entre métaux pour les acides utilisés individuellement à la concentration de 10-2 g/l ... 99
Tableau 23: Matrice de corrélation entre métaux pour les acides utilisés individuellement à la concentration de 3.10-2 g/l ... 99
Tableau 24: Matrice de corrélation entre métaux pour les acides utilisés individuellement à la concentration de 5.10-2 g/l ... 99
Tableau 25: Test d’homogénéité des variances ... 100
Tableau 26: ANOVA à 1 facteur ... 100
Tableau 27: Sous-ensembles homogènes ... 101
Tableau 28: Matrice de corrélation entre métaux pour le mélange des acides deux à deux à la concentration de 10-2g/l ... 104
Tableau 29: Matrice de corrélation entre métaux pour le mélange des acides deux à deux à la concentration de 3.10-2g/l ... 104
Tableau 30: Matrice de corrélation entre métaux pour le mélange des acides deux à deux à la concentration de 5.10-2g/l ... 104
Tableau 31: Test d’homogénéité des variances ... 105
Tableau 32: ANOVA à 1 facteur ... 106
Tableau 33: Sous-ensembles homogènes ... 106
Tableau 34: Matrice de corrélation entre métaux pour le mélange des trois acides (citrique, gluconique et oxalique) ... 109
Tableau 35: ANOVA à 1 facteur ... 109
xi
Tableau 37: Pourcentage de solubilisation des métaux par fraction géochimique à 10-2 g/l avec les
acides organiques individuels ... 142
Tableau 38: Pourcentage de solubilisation des métaux par fraction géochimique à 3.10-2 g/l avec les acides organiques individuels ... 142
Tableau 39: Pourcentage de solubilisation des métaux par fraction géochimique à 5.10-2 g/l avec les acides organiques individuels ... 144
Tableau 40: Pourcentage de solubilisation des métaux par fraction géochimique avec le mélange des acides organiques deux à deux et à 10-2 g/l ... 144
Tableau 41: Pourcentage de solubilisation des métaux par fraction géochimique avec le mélange des acides organiques deux à deux et à 3.10-2 g/l ... 145
Tableau 42: Pourcentage de solubilisation des métaux par fraction géochimique avec le mélange des acides organiques deux à deux et à 5.10-2 g/l ... 145
Tableau 43: Pourcentage de solubilisation des métaux par fraction géochimique avec le mélange des trois acides organiques ... 147
Tableau 44 : Taux massiques relatifs de solubilisation des différents métaux ... 155
Tableau 45: pK des acides organiques à 25 °C (Evangelou, 1998) ... 156
Tableau 46: Paramètres influençant la sélectivité de rétention des métaux lourds (Dubé, 1997) ... 157
Tableau 47: Séquence de rétention des métaux lourds comparée à celle des résidus miniers du Nouveau-Brunswick (NB) et de la Nouvelle-Calédonie (NC) tirée de Ouattara, 2008 ... 159
Tableau 48: Séquence préférentielle théorique de sélectivité et d’affinité (Dubé, 1997; Ouattara, 2008) ... 161
Tableau 49: Séquences de solubilisation des métaux par la lixiviation avec les acides organiques commerciaux comparée à celles de la lixiviation fongique (Ouattara, 2008) ... 162
Tableau 50: Coûts de production proposés par Mulligan (1999) actualisés... 165
Tableau 51: Exemples de procédés de séparation des métaux ... 166
Tableau 52 : Comparaison des prix des différents métaux par rapport aux coûts de production .... 167
Tableau 53: Variation de la valeur présente nette du cuivre par kilogramme en fonction des différents paramètres ... 168
Tableau 54: Variation de la valeur présente nette du nickel par kilogramme en fonction des différents paramètres ... 168
Tableau 55: Variation de la valeur présente nette du plomb par kilogramme en fonction des différents paramètres ... 168
Tableau 56: Variation de la valeur présente nette du zinc par kilogramme en fonction des différents paramètres ... 169
Tableau 57: Proportion des métaux précipités (Val-d’Or) ... 185
Tableau 58: Proportion des métaux précipités (Eustis) ... 185
Tableau 59: Principales caractéristiques des DMA après 15 jours d’essais de neutralisation ... 187
Tableau 60: Teneurs des métaux solubilisés (mg/l) dans le témoin (résidus miniers et eau dé-ionisée) ... 208
Tableau 61: Teneurs des métaux solubilisés (mg/l) dans le sel de déglaçage à 2 g/l ... 208
Tableau 62: Teneurs des métaux solubilisés (mg/l) dans le sel de déglaçage à 18 g/l ... 209
Tableau 63: Teneurs des métaux solubilisés (mg/l) dans le sel de déglaçage à 35 g/l ... 209
Tableau 64: Séquence de solubilisation des métaux lourds en fonction de la concentration en sel de déglaçage après 24 heures ... 211
Tableau 65: Solubilisation des métaux lourds avec la solution de sel de déglaçage à 2g/l par fraction géochimique (en pourcentage) ... 214
Tableau 66: Séquence de solubilisation des métaux lourds avec le sel de déglaçage dans les différentes fractions géochimiques ... 215
Tableau 67: Séquence de sélectivité des métaux lourds avec le sel de déglaçage ... 216
xii
Liste des figures
Figure 1: Évolution des droits miniers au Québec en millions de dollars (Source : Compte public du
Québec et Ministère des Finances du Québec) ... 12
Figure 2: Retombées fiscales liées aux activités minières au Québec en million de dollars (Gouvernement du Québec, 2012) ... 12
Figure 3: Valeurs des expéditions minières du Québec de 2001 à 2015 en milliards de dollars (tiré de MERN, 2016). ... 13
Figure 4: Schéma d’une mine à ciel ouvert (source : Commission Européenne, 2009)... 21
Figure 5: Schéma d’une mine souterraine (source : Commission Européenne, 2009)... 21
Figure 6 : Différentes étapes de l’extraction et de gestion des résidus miniers (source : Environnement Canada : Inventaire National des Rejets de Polluants: INRP, 2009) ... 22
Figure 7: Illustration schématique de la formation d'eau de drainage minier en fonction de l'interaction entre les résidus ou les stériles de l'installation et l'atmosphère (Source : Eriksson, 2002 dans "Commission Européenne", 2009) ... 27
Figure 8: Schéma des interactions entre les métaux lourds et les constituants du sol (Galvez-Cloutier, 1995) ... 32
Figure 9: Schéma méthodologique ... 48
Figure 10: Dolomie grossière de la carrière "OMYA St-Armand" de Québec ... 50
Figure 11: Drainages miniers acides d'Eustis (A et B) et de Val-d’Or (C et D). ... 51
Figure 12: Schéma du dispositif utilisé dans les essais en conditions anoxiques (Genty et al., 2008) ... 64
Figure 13: Exemple de montage de l'essai en jar test ... 65
Figure 14: Courbe granulométrique des résidus miniers ... 69
Figure 15: Résultats de l'analyse au MEB des résidus miniers ... 73
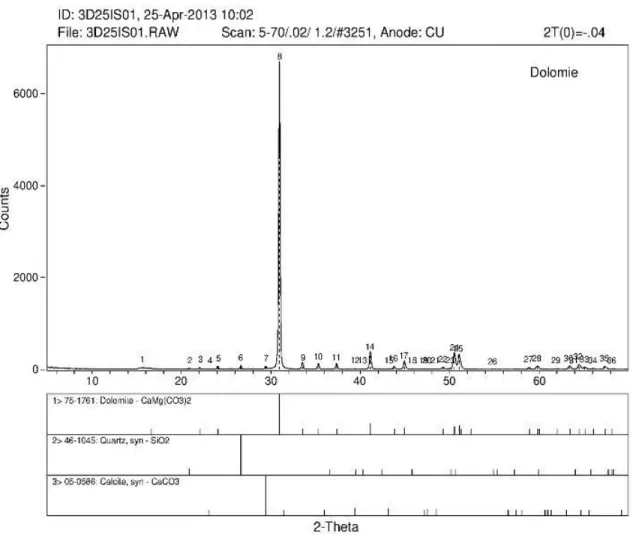
Figure 16: Spectres d'analyse à la diffraction aux RX des résidus miniers ... 75
Figure 17: Pouvoir tampon des résidus miniers ... 77
Figure 18: Distribution des métaux par fraction géochimique ... 82
Figure 19: Courbe granulométrique de la dolomie ... 86
Figure 20: Résultats de l'analyse au MEB de la dolomie ... 88
Figure 21: Spectre d'analyse à la diffraction aux RX de la dolomie ... 89
Figure 22: Pouvoir tampon de la dolomie ... 90
Figure 23: Structure de l’acide citrique ... 92
Figure 24: Structure de l’acide gluconique ... 92
Figure 25: Structure de l’acide oxalique ... 93
Figure 26: Teneurs des métaux solubilisés à partir des acides organiques individuels ... 98
Figure 27: Teneurs des métaux solubilisés à partir du mélange des acides organiques deux à deux ... 103
Figure 28: Teneurs des métaux solubilisés à partir du mélange des trois acides organiques ... 108
Figure 29: Teneurs des métaux solubilisés à partir des acides organiques individuels en fonction de la concentration ... 112
Figure 30: Teneurs des métaux solubilisés à partir du mélange des acides organiques deux à deux en fonction de la concentration ... 114
Figure 31: Teneurs des métaux solubilisés à partir du mélange des trois acides organiques en fonction de la concentration ... 115
Figure 32: Proportions des métaux solubilisés à partir des acides organiques individuels ... 117
Figure 33: Proportions des métaux solubilisés à partir du mélange des acides organiques deux à deux ... 119
xiii
Figure 35: Proportions des métaux solubilisés à partir des acides organiques individuels en fonction
de la concentration ... 123
Figure 36: Proportions des métaux solubilisés à partir du mélange des acides organiques deux à deux en fonction de la concentration ... 125
Figure 37: Proportions des métaux solubilisés à partir du mélange des trois acides organiques en fonction de la concentration ... 126
Figure 38: Évolution de la teneur de solubilisation des métaux en fonction du temps avec l’acide citrique... 128
Figure 39: Évolution de la teneur de solubilisation des métaux en fonction du temps avec l’acide gluconique ... 130
Figure 40: Évolution de la teneur de solubilisation des métaux en fonction du temps avec l’acide oxalique ... 132
Figure 41: Évolution de la teneur de solubilisation des métaux en fonction du temps avec le mélange acide citrique et acide gluconique ... 134
Figure 42: Évolution de la teneur de solubilisation des métaux en fonction du temps avec le mélange acide citrique et acide oxalique ... 136
Figure 43: Évolution de la teneur de solubilisation des métaux en fonction du temps avec le mélange acide oxalique et acide gluconique ... 138
Figure 44: Évolution de la teneur de solubilisation des métaux en fonction du temps avec le mélange des trois acides ... 139
Figure 45: Teneurs des métaux en fonction de la température de lixiviation ... 148
Figure 46: Montage expérimental des essais en colonnes ... 150
Figure 47: Évolution du pH en fonction du temps ... 151
Figure 48: Évolution de la conductivité en fonction du temps ... 152
Figure 49: Évolution de la teneur des métaux en fonction du temps ... 153
Figure 50: Diagramme comparatif des teneurs des différents métaux solubilisés ... 154
Figure 51: Analyse des coûts de récupération des métaux par kilogramme ... 170
Figure 52: Essai de neutralisation en béchers des drainages miniers acides par la dolomie ... 174
Figure 53: Évolution du pH en fonction du temps ... 176
Figure 54: Évolution de la teneur en sulfate en fonction du temps ... 177
Figure 55: Montage expérimental des essais en colonnes ... 178
Figure 56: Évolution du pH des DMA après deux semaines de test de neutralisation... 179
Figure 57: Évolution des teneurs en sulfate dans les DMA après deux semaines de test de neutralisation ... 180
Figure 58: Évolution des teneurs des métaux précipités ... 183
Figure 59: Évolution de la teneur en métaux précipités (suite) ... 184
Figure 60: Proportions comparées des métaux précipités après neutralisation des deux DMA par la dolomie ... 186
Figure 61: Aspects de la dolomie après les essais de neutralisation en béchers ... 189
Figure 62: Résultats de l'analyse au MEB de la dolomie utilisée avec le DMA d'Eustis (A : anoxique; B : oxique) ... 190
Figure 63: Résultats de l'analyse au MEB de la dolomie utilisée avec le DMA de Val-d’Or (A : anoxique; B : oxique) ... 190
Figure 64: Spectre d'analyse à la diffraction aux RX de la dolomie utilisée avec le DMA d'Eustis (conditions anoxiques) ... 192
Figure 65: Spectre d'analyse à la diffraction aux RX de la dolomie utilisée avec le DMA d'Eustis (conditions oxiques) ... 193
Figure 66: Spectre d'analyse à la diffraction aux RX de la dolomie utilisée avec le DMA de Val-d’Or (conditions anoxiques) ... 194
Figure 67: Spectre d'analyse à la diffraction aux RX de la dolomie utilisée avec le DMA de Val-d’Or (conditions oxiques)... 195
xiv
Figure 68: Montage expérimental des essais préliminaires en jar test ... 199
Figure 69: Évolution du pH en fonction du temps ... 201
Figure 70: Évolution de la conductivité en fonction du temps ... 202
Figure 71: Évolution du potentiel redox en fonction du temps ... 203
Figure 72: Évolution de la teneur en sulfate en fonction du temps ... 205
Figure 73: Évolution de la teneur en chlorure en fonction du temps ... 206
Figure 74: Comparaison des teneurs de métaux solubilisés en fonction de la concentration en sel de déglaçage ... 210
Figure 75: Comparaison des teneurs de métaux solubilisés dans la colonne alimentée par la solution de sel de déglaçage à 2g/l et la colonne témoin ... 210
Figure 76: Teneurs des métaux solubilisés en fonction des fractions géochimiques ... 215
Figure 77: Montage expérimental des essais en colonne ... 217
Figure 78: Évolution du pH en fonction du temps ... 218
Figure 79: Évolution de la conductivité en fonction du temps ... 219
Figure 80: Évolution de la teneur en chlorure en fonction du temps ... 220
Figure 81: Évolution de la teneur en sulfate en fonction du temps ... 221
Figure 82: Évolution de la teneur des métaux en fonction du temps ... 223
Figure 83: Principaux mécanismes de remobilisation des métaux par NaCl (Suaire et al. 2013) .. 226
Figure 84: Comparaison de la teneur des métaux solubilisés entre la solution de sel de déglaçage et la colonne témoin ... 229
xv
Liste des annexes
Annexe A: Diffractogrammes des résidus miniers ... 255 Annexe B: Diffractogramme de la dolomie ... 258 Annexe C: Principales étapes de récupération sélective des métaux ... 259 Annexe D: Grille des critères génériques pour les sols (tirée de la politique de protection des sols et de réhabilitation des terrains contaminés. ... 260 Annexe E: Relation entre la température et la quantité de sel de voirie nécessaire pour faire fondre la glace. ... 262 Annexe F: Représentation graphique de la relation entre la température et la quantité de sel de voirie nécessaire pour faire fondre la glace. ... 262 Annexe G: Répartition du nombre de jours de précipitations de pluie et de neige de 1981 à 2010 mesurée à station météorologique de l'Aéroport Montréal-Trudeau (Québec). ... 263
xvi
Liste des abréviations et sigles
ADN Acide désoxyribonucléique
ANOVA "Analyse of variance"
ASTM "American society for testing materials"
BSR Bactéries sulfato-réductrices
CaCO3 Calcaire
[CaMg(CO3)2] Dolomie
CEAEQ Centre d’expertise en analyse environnementale du Québec
CEBC Couvertures avec effets de barrière capillaire
CEC Capacité d’échange cationique
Cl Chlore
Cmol / Kg Centi-mole par kilogramme
DAC Drains anoxiques calcaires
DF "Dilution factor"
DMA Drainage minier acide
DMN Drainage minier neutre
DNC Drainage minier neutre contaminé
DOC Drains oxiques calcaires
DRX Diffraction aux rayons X
ESS Extraction séquentielle sélective
Fe2+ Fer ferreux
Fe3+ Fer ferrique
g/l gramme par litre
GCB Géo-composites benthoniques
GCL "Geosynthetic clay liners"
xvii
HPLC "High-performance liquid chromatography"
INRP Inventaire national des rejets de polluants
MDDEFP Ministère du Développement Durable de l’Environnement de la Faune et des Parcs
MDDELCC Ministère du Développement Durable de l’Environnement et Lutte Contre les Changements Climatiques
MDDEP Ministère du Développement Durable de l’Environnement et des Parcs
MEB Microscope électronique à balayage
MEND "Mine environment neutral drainage"
MERN Ministère de l’énergie et des ressources naturelles
MES Matières en suspension
mg/l Milligramme par litre
MNRF Ministère des Ressources naturelles et de la Faune
MTQ Ministère des Transports du Québec
MV Millivolts
µS / cm Microsiemens par centimètre
NaCl Chlorure de sodium
NEDEM Neutralisation des eaux de drainage dans l’environnement minier ORP "Oxidation Reduction Potential"
PAF Perte au feu
pE Potentiel d’oxydoréduction
pH Potentiel d’hydrogène
RATS Résidus acides en transformation et stabilisation
RPM Rotations par minute
S2O3
Sulfosels
TOC Tranchées ouvertes calcaires
xviii
Dédicaces
Je dédie ce travail à mon épouse Hortense et à mes adorables princesses
Dorine et Lyne Wendy.
Merci pour votre compréhension, votre patience et votre indulgence malgré
mes absences récurrentes et prolongées.
xix
Remerciements
À la fin de cette aventure parsemée de questionnements, je voudrais tout d’abord remercier Professeure Rosa Galvez directrice du Département de Génie – Civil et Génie des eaux et ma Directrice de thèse qui m’a accompagné tout au long de ce projet et dont la supervision, l’expérience, la disponibilité et les qualités humaines et sociales ont surtout été des sources de motivations constantes pour l’atteinte des différents objectifs.
Je tiens également à remercier Docteure Abibata Ouattara, ma codirectrice de thèse pour ses précieux conseils qui m’ont guidé tout au long de ce travail. Son sens de l’écoute et du travail bien fait m’ont été d’un apport inestimable.
Tous mes remerciements au Professeur Marcel Laflamme, Directeur de programme au département de Génie des mines qui m’a aidé pour l’obtention des résidus miniers sans lesquels ce travail ne pouvait pas se faire. Merci pour les conseils et contributions diverses. Je remercie le Programme Canadien des Bourses de la Francophonie (PCBF) pour le soutien financier sans lequel, ce projet n’aurait pas été réalité.
Je voudrais également remercier le Professeur Lompo Martin, Chargé de Mission du Centre Universitaire Polytechnique de Fada N’Gourma (CUP-Fada) et Directeur de l’École Nationale Supérieure d’Ingénieurs de Fada N’Gourma (ENSI-F) pour les différents soutiens et encouragements.
Toute ma reconnaissance à Monsieur Michel Bisping du laboratoire d’environnement pour sa disponibilité et ses encouragements tout au long de ce travail.
À Christian Juneau du laboratoire de géotechnique, André Ferland du Laboratoire de microanalyse et Jean Frenette du laboratoire de diffraction-X pour les différentes analyses.
À Ana pour les logiciels qui ont facilité le traitement de mes données et ces différentes contributions, conseils et encouragements.
xx
Toutes mes reconnaissances à l’équipe de Rosa Galvez et aux stagiaires qui ont participé à ce projet.
À tous mes collègues et collaborateurs de l’École Nationale Supérieure d’Ingénieurs de Fada N’gourma (ENSI-F).
Enfin, si ce projet est arrivé à terme, je le dois à mon épouse Hortense, à mes filles Dorine et Lyne Wendy : votre soutien, votre patience et votre compréhension : tout ce temps d’absence et ce préjudice affectif.
À mon père décédé au début de cette aventure, à ma mère, mes frères et sœurs : enfin terminées ces études qui n’en finissent pas !
1
2
L’activité minière est source de profits économiques pour les états, les populations et contribue pour une part importante à la lutte contre la pauvreté particulièrement dans les pays en développement. La croissance démographique, l’urbanisation, les développements technologiques et les fortes demandes par les pays émergents (Chine, Indonésie, Inde, Brésil, Afrique du Sud) compte tenu de leur industrialisation accélérée ont pour conséquences des besoins en minéraux et métaux sans cesse croissants. L’industrie minière occupe donc une place de choix dans l’économie des pays producteurs ou exportateurs de minéraux et de métaux.
Au Québec, les contributions du secteur minier au titre des droits miniers sont estimées à 304 millions de dollars en 2010 – 2011, ce qui est nettement supérieur à la somme des droits miniers versés au cours des dix années précédentes par les compagnies minières au gouvernement du Québec (Direction générale de la géologie du Québec, 2012). À cette date, le territoire québécois comptait 25 mines actives avec également 249 116 titres miniers actifs couvrant 11 463 198 ha, soit une hausse de 10,7% par rapport aux années antérieures. En 2010, les activités d’extraction minière ont généré environ 15109 emplois directs, et selon le Ministère des Ressources naturelles et de la Faune (MRNF), les emplois directs et indirects étaient estimés à 34 000 en 2011. Le Québec était la quatrième plus importante province canadienne en matière des valeurs d’expéditions minières en 2011, derrière l’Ontario, le Saskatchewan, la Colombie-Britannique, et premier producteur Canadien en ce qui concerne les minéraux métalliques (or, cuivre, zinc et fer) en 2009 et 2010 (Labrecque, 2012).
Si l’industrie minière est source de retombées économiques pour le Québec et créatrice d’emplois, elle peut cependant être préjudiciable à l’environnement durant les différentes phases (exploration, développement, production, fermeture). Elle présente des aspects négatifs (Aubertin et al., 2002) à savoir entre autres: des risques pour la santé humaine, des incidences sur l’environnement et sur l’utilisation du territoire, des conséquences d’ordre économique, politique et social. Ces effets se manifestent par les perturbations de l’esthétique des lieux, la contamination de l’eau, des sols et de l’air, des menaces à la flore et la faune.
3
En effet, l’exploitation et le traitement des minerais engendrent de grands volumes de rejets miniers (rejets de concentrateurs, stériles miniers) qui doivent être gérés de façon rationnelle et sécuritaire afin de protéger l’environnement (Aubertin et al., 2002). À titre d’exemple, selon Windfield et al. (2002), la production d’une paire d’alliances en or nécessiterait le traitement d’une quantité de minerai équivalent à un trou creusé dans le sol de 3 mètres de longueur, 1,8 mètre de largeur et 1,8 mètre de profondeur, soit 9,72 m3 de minerai. Cela est lié aux teneurs généralement faibles des minéralisations, ce qui conduit à des amoncellements de grandes quantités de rejets d’exploitation dans le paysage, constitués par le mort-terrain, les stériles et les résidus de traitement.
En plus, lorsque ces résidus miniers contiennent des minéraux sulfurés, leur exposition à l’oxygène, à l’eau ou à certains microorganismes entraîne leur oxydation qui peut produire un lixiviat acide (appelé drainage minier acide ou DMA) susceptible de solubiliser les métaux qui auront des impacts négatifs sur l’environnement. D’après Kalin et al. (2006), et par consensus général, le drainage minier acide (DMA) est le problème environnemental le plus critique lié à l'exploitation minière.
La génération du DMA est un processus complexe qui dépend de facteurs physiques, chimiques et biologiques. Les principaux composants requis pour la formation du DMA sont (Kawatra et Natarajan, 2001): des résidus contenant des sulfures réactifs incluant les minéraux sulfurés, du soufre élémentaire et des sulfures intermédiaires divers (sulfosels : S2O32-); de l’oxygène moléculaire et de l’eau. D’autres facteurs y interviennent en influençant la vitesse de production des acides. Il s’agit : de l’activité biologique, de la température, du pH, la présence d’oxydants alternatifs (Fe3+, Mn3+, Mn4+), la présence de minéraux tampons ou alcalins (la calcite ou les silicates). Étant donné que la minéralogie et les facteurs affectant la formation du DMA varient énormément d’un site à l’autre, la prédiction d’un potentiel DMA peut s’avérer extrêmement difficile et coûteuse (Akcil et Koldas, 2006). En outre, le choix d’une méthode dans le traitement du DMA est tributaire de plusieurs facteurs qui sont entre autres : le potentiel de génération d’acide et le potentiel de neutralisation acide des résidus miniers, la nature et les caractéristiques physiques des résidus, les conditions de terrain, le climat, la topographie, l'hydrologie des eaux de surface
4
et souterraines, la durée d'efficacité requise de la mesure de contrôle ainsi que la sensibilité du milieu récepteur face au DMA (Aubertin et al., 2002a).
Face aux problèmes liés à l’activité extractive industrielle et en particulier au DMA, des législations et des normes ont été adoptées pour amener les compagnies minières à réduire ces effets dans une perspective de développement durable (loi sur les mines, loi sur la qualité de l’environnement, la directive 019, le règlement sur les effluents des mines de métaux: REMM). Les compagnies minières ont également développé des pratiques visant à minimiser les impacts de l’industrie extractive sur l’environnement et les communautés. Ces pratiques intègrent des normes (norme CSA-ISO 31 000 – F10 relative aux principes et lignes directrices de la gestion du risque), des méthodes de gestion intégrée des résidus miniers, la construction de relations solides avec les communautés locales et particulièrement les peuples autochtones. Le cas le plus édifiant est celui du projet Manitou-Goldex qui est un partenariat MRNF-Mines Agnico Eagle (MAE). En effet, ce projet de partenariat innovateur, qui allie développement durable et visées économiques, avait pour objectif la restauration du site minier Manitou en utilisant les résidus de la mine Goldex afin de recouvrir et de neutraliser les résidus qui sont générateurs de DMA (MRNF, 2008). Pour ce faire, les résidus de la mine Goldex qui sont dépourvus de sulfure et de cyanure et dont le potentiel de neutralisation acide est très important sont acheminés sous forme de pulpe épaissie à 55 % solide, par un pipeline d’une longueur d’environ 24 km jusqu’au site Manitou. Ce projet a été financé à hauteur de 35 millions de dollars par le gouvernement du Québec et de 15 millions de dollars par la compagnie Agnico Eagle qui est propriétaire de la mine Goldex (Institut du Nouveau Monde, 2014).
Des méthodes de traitement du DMA et de restauration de sites abandonnés ont également été développées (méthodes chimiques, biologiques) à travers le monde, mais les différents travaux montrent que leur application et leur efficacité dépendent de nombreux facteurs (cités plus haut). Le principe des différentes méthodes consiste à réduire ou éliminer la présence de l’une des principales sources d’oxygène et/ou l’eau.
5
Pendant longtemps, le système de terrain marécageux, en particulier ceux contenant de la sphaigne (mousses de la famille des Sphagnaceae) a été utilisé (Hedin et al., 1994; Skousen et Ziemkiewicz, 1995; Aubertin et al., 2002). Ce système consiste à réduire de façon significative la concentration des solides en suspension, en sulfates et en métaux dissous et la hausse du pH lorsque le DMA circule dans ce terrain marécageux. Cependant, on assiste à une détérioration des zones marécageuses par l’acide à la suite d’une longue période d’exposition à l’air ambiant.
D’autres essais ont donc été envisagés. Les principaux visant à prévenir ou à contrôler le DMA sont (Aubertin et al., 2002):
les essais statiques et minéralogiques qui ont pour objectif d’établir la capacité d’un échantillon de résidus miniers à produire de l’acide et à le neutraliser. Ils consistent à établir une balance entre les minéraux potentiellement producteurs d’acide et ceux potentiellement neutralisateurs. Les essais cinétiques visant à prédire quand débuterait la génération du
lixiviat acide et aussi à caractériser l’évolution de la qualité de l’eau dans le temps. Autrement dit, d’évaluer des taux de réaction et le temps requis pour épuiser les réserves minérales (sulfures, minéraux acidivores tels que les carbonates, silicates, hydroxydes).
Les drains de pierres calcaires ou système de traitement passif où on fait circuler le DMA, ce qui a pour conséquences de générer de l’alcalinité et augmenter le pH. Il s’agit des drains anoxiques calcaires (DAC), les drains oxiques calcaires (DOC) et les tranchées ouvertes calcaires (TOC).
Les recouvrements aqueux qui sont basés sur le taux de solubilité et de diffusion de l’oxygène dans l’eau. Le taux de transport de l’oxygène à travers l’eau peut être suffisamment faible de sorte que la production d’acide soit insignifiante.
Les recouvrements étanches sont utilisés pour exclure tout apport en eau aux matériaux sulfurés. Ces barrières imperméables sont faites de sols à faible conductivité hydraulique ou de matériaux synthétiques peu perméables. On a les géomembranes, géocomposite (géocomposite bentonitique : GCB ou
6
géosynthétique bentonique : GSB, "Geosynthetic Clay Liners" : GCL) ou les recouvrements de type couvertures avec effets de barrière capillaire (CEBC) pour réduire le flux d’oxygène. Les matériaux utilisés dans ces barrières sont entre autres : les rejets des industries de pâte et papier, les enduits bitumineux, les ciments ou cendres volantes, les enduits de surface et les boues amendées.
La neutralisation qui utilise des minéraux calcaires, de la chaux hydratée, du carbonate de sodium, de la soude caustique, de l’ammoniac, du peroxyde de calcium, des cendres et de la dolomie.
Des méthodes dites biologiques comprenant des méthodes de traitement passif et des méthodes de traitement actif sont également utilisées. Les méthodes de traitement passif concernent les bactéries sulfato-réducteur (BSR) et la présence de sources de carbone organique. L’élimination de l’action bactérienne consiste en général à la création de conditions anoxiques afin d’inhiber l’action bactérienne ou d’améliorer les activités des bactéries sulfato-réductrices (BSR). En effet, la présence de certaines bactéries acidophiles hétérotrophes (Acidiphilicum spp., par exemple) dans le DMA inhibe les réactions d’oxydation (Kawatra et Natarajan, 2001). Les méthodes de traitement actif concernent également les bioréacteurs sulfurogènes et l’oxydation accélérée du fer avec de la biomasse immobilisée (Zagury et al., 2005).
D’autres méthodes ont également été développées pour la valorisation des résidus miniers afin d’augmenter les retombées économiques et de réduire leurs impacts sur l’environnement. La mise en valeur des résidus miniers est réalisée selon les sites et suivant divers procédés tout en respectant les normes et réglementations en vigueur. Il s’agit essentiellement des procédés d’extraction des métaux contenus dans les résidus miniers, le traitement par séparation physique n'utilisant aucun réactif chimique, la phyto-remédiation (Ali et al., 2013) qui est l'utilisation des plantes et des microbes du sol pour réduire les concentrations ou les effets toxiques de contaminants dans l'environnement, les pratiques de valorisation qui s’inscrivent dans une gestion intégrée des résidus miniers (remblais miniers souterrains, les remblais miniers cimentés en pâte, stabilisation des dépôts de
7
résidus miniers en pâte de surface, remblayage des fosses dans le cas des mines à ciel ouvert).
Compte tenu des problèmes posés par l’industrie extractive et particulièrement ceux liés au DMA, consécutifs à la demande de plus en plus croissante en matières premières minérales, les recherches sont de nos jours orientées vers la récupération des métaux des minerais faiblement riches (à faible teneur) et la valorisation des résidus miniers.
Par conséquent, des techniques de valorisation telles que la biolixiviation ont été développées (Mulligan et al., 1999; Ouattara, 2008). Le rôle des microorganismes que sont les bactéries et les champignons est de favoriser la récupération des métaux contenus dans les résidus solides, en les transformant en composés solubles et extractibles. La lixiviation bactérienne est utilisée pour récupérer les métaux dans les minerais à faible teneur ou pour une récupération secondaire des métaux contenus dans les résidus de traitement pour éviter une pollution de l’environnement. Cependant, la lixiviation bactérienne s’applique aux milieux acides et nécessite généralement la présence d’une source d’énergie. En général, les bactéries chimioautotrophes du genre Thiobacillus et Sulfolobus sont utilisés dans les milieux sulfurés pour l’extraction des métaux, contrairement aux bactéries hétérotrophes et les champignons qui sont utilisés aussi bien dans la lixiviation des minerais de métaux sulfurés que des minerais non sulfurés (Ouattara, 2008).
Les premiers travaux sur la lixiviation fongique (qui utilise les champignons) ont montré qu'elle permettait la récupération des métaux de valeur, à des concentrations commercialement attractives et représente une biotechnologie qui respecte l'environnement, mais pas économiquement rentable compte tenu du coût élevé du substrat utilisé (Bosshard et al., 1996; Gadd et al., 1998). Mulligan et al. (1999), ont suggéré l'utilisation de résidus alimentaires peu couteux et disponibles en grande quantité, comme source de substrat, pour la production des acides organiques.
En utilisant comme substrat, le perméat de lactosérum à la place du sucrose habituellement utilisé, et les champignons Aspergillus niger et Penicillium simplicissimum sur des résidus
8
de mines de zinc et de plomb (du Nouveau Brunswick) et de nickel (de la Nouvelle-Calédonie), Ouattara (2008) montre que la lixiviation fongique pouvait être rentable en fonction du type de résidus miniers et permettrait de protéger l’environnement dans une perspective de développement durable. Pour ce faire, la lixiviation fongique qui s’applique aux différents types de matériaux (acide, neutre, basique, présence ou pas de sulfures) apparaît comme une alternative aux problèmes de pollution de l’environnement liés au DMA.
Plusieurs études sur la biolixiviation ont montré qu’en dehors des acides organiques produits par les microorganismes, d’autres produits du métabolisme devraient être impliqués dans la solubilisation des métaux (Vachon et al., 1994; Castro et al., 2000). Selon Morley et al., 1996, les enzymes sécrétés par les champignons tels que les phosphatases seraient responsables de la solubilisation des phosphates métalliques. Pour Cameselle et al., 1995, la réduction enzymatique serait à l’origine de la transformation du fer ferrique (Fe3+
) en fer ferreux (Fe2+) au cours de la biolixiviation. Ten et Ting (2003) ont montré en utilisant Aspergillus niger pour la récupération des métaux contenus dans les résidus électroniques que la solubilisation des métaux n’était pas attribuable à des enzymes extracellulaires, mais principalement due à l’action des acides organiques. Les acides citrique, oxalique et gluconique produits par les champignons étaient responsables du processus de biolixiviation dans la récupération des métaux lourds.
Ten (2003) en dénaturant les enzymes par traitement thermique en autoclave montre que les résultats de lixiviation des métaux du substrat originel par Aspergillus niger et Penicillium
simplicissimum étaient identiques à ceux obtenus après dénaturation des enzymes. Ces
résultats confirment également que les enzymes extracellulaires n’étaient pas responsables de la solubilisation des métaux.
En outre, dans les pays où l’hiver dure plusieurs mois, on a recours aux sels de déglaçage utilisés comme fondants. Pour l’entretien hivernal du réseau routier au Québec, environ 1,5 million de tonnes de sels de voirie sont épandues annuellement. Or, ces sels ont des effets néfastes sur les nappes aquifères, le sol, la flore et la faune (Morin et Perchanok, 1999 cités
9
par le MTQ, 2010). Le sel de déglaçage le plus fréquemment utilisé dans beaucoup de pays est le chlorure de sodium (NaCl) (Norrström et Bergstedt, 2001).
Le maintien des conditions sécuritaires de circulation en période hivernale nécessite l’utilisation de ces sels de déglaçage. Le NaCl et les sels de déglaçage en général sont des substances qui pénètrent et migrent dans l’environnement sous forme d’ions dissociés et il n’existe pas de mécanismes d’élimination majeurs (volatilisation, dégradation, sorption ou oxydation) pour contribuer à l’élimination des sels dans les eaux de surface (Environnement Canada et Santé Canada, 2001, Lauzon, 2007). De plus la salinité consécutive à l’utilisation des sels de déglaçage augmenterait la mobilité des métaux dans les sols, et amplifierait par conséquent leur mobilisation (Bäckström et al. 2005; Norrström, 2005; Acosta et al. 2011). Pour cette raison, la percolation de ces sels à travers les stériles et les résidus miniers peut être à l’origine de la mobilisation des métaux et de leur relargage dans l’environnement augmentant ainsi les impacts sur l’environnement.
C’est dans ce contexte que se situe le présent projet de thèse qui vise le développement de méthodes pour la gestion des résidus miniers dans une perspective de développement durable et de protection de l’environnement. Il ambitionne : (1) la lixiviation des métaux à partir des résidus miniers par des acides organiques commerciaux; (2) la neutralisation du DMA par de la dolomie et (3) l’étude des échanges entre les métaux et les sels de déglaçage
10
11
II.1. Problématiques
Dans le secteur des mines, le Québec est l’un des leaders mondiaux. Son sous-sol regorge de nombreuses potentialités minières en plus des ressources pétrolières et gazières. Les premières exploitations minières ont commencé dès 1840, mais c’est au début des années 1920 que l’industrie minière prend son véritable envol au Québec (MERN - rapport sur les activités minières du Québec, 2014). Le Québec devient dès lors le principal pourvoyeur en minerais des régions les plus industrialisés d’Amérique du Nord. Cet état de fait se trouve alors amplifié compte tenu de la croissance de l’industrie minière et de l’importance de l’expansion industrielle. Les substances généralement exploitées sont les minéraux métalliques, les minéraux industriels et les matériaux de construction.
Selon ce même rapport sur les activités minières du Québec - MERN (2014), près de 200 mines, carrières et sablières peuvent être dénombrées sur l’ensemble du territoire, parmi lesquelles une vingtaine exploite des gisements métalliques dont plusieurs sont de classe mondiale : mine Raglan (nickel), et LaRonde (or, zinc, cuivre, argent). Les principales régions concernées sont l’Abitibi-Témiscamingue (or, argent, zinc, cuivre), la Côte-Nord (fer et ilménite) et Nord-du-Québec (nickel, or, zinc). Selon le Gouvernement du Québec (2012), les redevances minières ont représenté 42 millions de dollars par année de 2006-2007 à 2009-2010. Ce montant atteignait 365 millions de dollars en 2011-2012 et devrait dépasser 400 millions de dollars annuellement à partir de 2015-2016 (Figure 1). La contribution du secteur des mines à l’économie du Québec est alors très importante. En 2010 (Gouvernement du Québec, 2012), environ 43100 emplois étaient liés à l’industrie minière, soit près de 1,3% des emplois au Québec. Sa contribution au produit intérieur brut québécois (PIB) représentait 7 milliards de dollars, soit 2,8% de l’économie québécoise et 23,2% de l’ensemble des exportations du Québec.
12
Figure 1: Évolution des droits miniers au Québec en millions de dollars (Source : Compte
public du Québec et Ministère des Finances du Québec)
En 2010, les retombées fiscales liées aux activités minières sur l’ensemble du territoire du Québec étaient estimées à 617 millions de dollars (Figure 2). Elles sont évaluées à 6,1 milliards de dollars pour la période allant de 2012 à 2016 (gouvernement du Québec, 2012).
Figure 2: Retombées fiscales liées aux activités minières au Québec en million de dollars
13
Toutefois, 2015 a connu une baisse de la demande et une diminution du prix des substances minérales sur le plan mondial (MERN – rapport sur les activités minières du Québec, 2016). Ainsi donc, la valeur des expéditions du Québec au cours de cette année pour les minéraux métalliques et industriels est estimée à 7,7 milliards de dollars, soit une baisse de 9,5% par rapport à 2014 (8,5 milliards de dollars) (Figure 3).
Figure 3: Valeurs des expéditions minières du Québec de 2001 à 2015 en milliards de
dollars (tiré de MERN, 2016).
Cependant, si l’industrie minière est source de revenus, de retombées économiques et favorise la création d’emplois d’une part, d’autre part elle peut être préjudiciable à l’environnement. En effet, elle présente des impacts avec des importances très variables selon les différentes étapes du cycle de vie de la mine (exploration, développement, production, fermeture). Ces impacts sont ressentis sur les ressources en eaux, la biodiversité (flore et faune), le paysage, le sol et sur la qualité de l’air. Ces impacts diffèrent également selon le type d’exploitation, c’est-à-dire à ciel ouvert ou souterrain. Le choix du type d’exploitation étant fonction de plusieurs paramètres, dont la teneur du minerai, le coût unitaire de l'exploitation (coût/tonne), la sélectivité du minerai, et la sécurité. Toutefois, la géochimie complexe des minerais de métaux ainsi que l’utilisation de réactifs pour le traitement des minerais tendent à amplifier les effets de la pollution consécutive à l’exploitation minière.
La dégradation des écosystèmes aquatiques et des cours d’eau récepteurs, impliquant souvent des réductions substantielles dans la qualité de l’eau, fait partie des impacts les plus graves de l’extraction des métaux.
14
La pollution des cours d’eau résulte essentiellement de trois facteurs principaux : la sédimentation, le drainage minier acide et la solubilisation des métaux. L’érosion ou les eaux de ruissellement après de fortes pluies augmentent souvent la charge sédimentaire des cours d’eau situés à proximité. L’eau joue un rôle très important dans l’activité minière, car le traitement des minerais nécessite d’énormes quantités d’eau.
Les activités minières peuvent provoquer une contamination de l’eau à travers les résidus ou par d’autres contacts directs ou indirects, le mélange ou l’utilisation de l’eau dans le traitement des minerais. L’activité minière contribue également à la désorganisation et l’eutrophisation du réseau hydrographique de la région concernée, surtout dans le cas des mines à ciel ouvert.
La construction et l’entretien (par apport de sels de déglaçage) de routes d’accès, soit pour l’acheminement des équipements lourds et des produits sur le site ou pour l’expédition des métaux et des minerais traités, peuvent avoir des conséquences importantes sur l’environnement (destruction d’habitats fauniques, d’arbres, du sol).
L’impact le plus évident de l’exploitation minière sur la biodiversité est la disparition de la végétation, qui à son tour modifie la disponibilité de la nourriture et les habitats fauniques.
De façon naturelle, l’activité minière implique la production de grandes quantités de rejets miniers. Ces volumes dépendent du type de minerai exploité, du type d’exploitation, de la teneur ainsi que de la taille de la mine. La disposition de ces grands volumes de résidus miniers constitue des défis considérables pour l’industrie minière et peut avoir des impacts dévastateurs sur l’environnement. Ces effets sont souvent plus prononcés pour les mines à ciel ouvert que pour les mines souterraines. Les rejets qui sont en général sans valeur économique immédiate (Chevalier et Paquette, 1996) représentent la portion la plus importante du matériel extrait. Cette situation s’explique par les faibles teneurs de métaux contenus dans les roches et par les énormes volumes de roches qui doivent être extraits, traités et rejetés. Ils sont composés des rejets de découverture, des haldes à stériles et des résidus stockés dans les parcs à résidus. Si une infime partie des rejets est réutilisée (remblais ou matériau d’entretien ou de construction), la grande partie est entreposée.
15
Les résidus miniers demeurent le plus problématiques en raison de leur taille et des produits chimiques qu’ils peuvent contenir (cyanure par exemple). Ils sont composés de roches finement broyées et un pourcentage élevé de particules inférieures à 80 microns (Aubertin, 2002). Au Québec, les activités minières couvrent 280 km2 et génèrent des résidus miniers qui couvrent environ 150 km2 (MRNF, 2011). En plus de la perturbation esthétique, lorsqu’ils contiennent des métaux ou des minéraux sulfurés, ces résidus sont susceptibles de produire du drainage minier acide (DMA) et favoriser ainsi la mobilisation (la solubilisation) des métaux dans l’environnement. Toutefois, il convient de noter qu’une exploitation de minerais sulfurés peut ne pas engendrer des problèmes de DMA, car certains minéraux basiques présents au sein de la roche mère, telle que la calcite, la dolomite, l’ankérite, la chlorite, et l’épidote, sont des minéraux consommateurs d’acide et leur présence en une certaine quantité peut inhiber la formation du DMA. De plus, la formation de DMA est fonction du potentiel des résidus et des stériles à générer de l’acide.
Le DMA est caractérisé par sa coloration "rouge brique" ou jaunâtre, la présence d’un acide minéral comme l’acide sulfurique (H2SO4), de métaux lourds comme le cuivre, le fer, le plomb, le zinc et par une coloration rougeâtre typique compte tenu des fortes concentrations de fer ferrique (Fe3+) en solution tout en véhiculant d’importantes quantités d’aluminium, de magnésium, de calcium et de sulfates (Chevalier et Paquette, 1996). Ces effluents acides représentent des sources de pollution de l’environnement et particulièrement des effets néfastes pour les eaux de surface (lacs, rivières, fleuves), la vie aquatique (poissons en particulier) et la santé humaine.
Selon Aubertin (2002), le problème du DMA était connu depuis des centaines d’années (particulièrement en Europe), mais il a suscité beaucoup plus d’intérêt au cours des années 1980 et 1990 à travers ses différents aspects que sont : les incidences environnementales, les contrôles législatifs et les aspects techniques relatifs à la prédiction, la prévention et le contrôle. Le Canada, avec la participation du Québec, a beaucoup contribué à l’avancement des connaissances et la mise au point de solutions pratiques notamment à travers le programme de recherches NEDEM (Neutralisation des Eaux de Drainage dans
16
l’Environnement Minier) qui a succédé au programme RATS (Résidus Acides en Transformation et Stabilisation).
Face à ces problèmes, de nombreuses normes et lois ont été adoptées. L’évolution des techniques d’exploitation et de gestion des résidus miniers par les compagnies minières a permis également de réduire les impacts liés à l’activité minière au Québec. Toutefois, il n’en demeure pas moins que de nombreux passifs relatifs au lourd héritage des mines abandonnées existent. Ces sites laissés à l’abandon et sans propriétaire sont en général désignés par des termes tels que: abandonné, orphelin, rétrocédé, inactif, fermé et délaissé. Selon Bussière et al. (2005), "un site minier est considéré abandonné si on ne peut identifier de propriétaire solvable (autre que le gouvernement) pour les composantes de la mine (par exemple : le puits, les infrastructures, les aires d’entreposage) ou si les installations ont été rétrocédées à la Couronne". Au 31 mars 2012, 698 sites miniers étaient inscrits à l’inventaire du passif environnemental du gouvernement du Québec, pour un montant total de 891,6 M$ (Lafrance et al. 2012).
Par ailleurs, compte tenu de l’hiver qui dure plusieurs mois, on a généralement recours à des fondants routiers (comme le sel de déglaçage) pour dégager les routes. Ces sels une fois dans l’environnement peuvent aggraver la mobilisation des métaux contenus dans les rejets miniers, de même que ceux solubilisés dans le drainage minier acide. Lorsque ces rejets contiennent des métaux (liés par exemple aux sulfures), l’utilisation de ces fondants peut contribuer à la libération de ceux-ci entraînant ainsi la pollution de l’environnement.
C’est dans ce contexte que se situe ce projet de thèse qui ambitionne d’explorer des solutions techniques afin de réduire les impacts relatifs à l’activité minière et de contrôler les facteurs aggravants tels que l’utilisation de sels de déglaçage.
II.2. But et objectifs
Pour réduire les préjudices causés à l’environnement par l’exploitation minière, des techniques de valorisation des résidus miniers, telle que la biolixiviation (bactérienne ou
17
fongique), ont été développées. La biolixiviation fongique (qui utilise les champignons), contrairement à la biolixiviation bactérienne, ne nécessite pas de sources d’énergie et s’applique à tous les milieux (acide, basique ou neutre). En effet, ces deux dernières décennies ont connu plusieurs applications de la lixiviation fongique dans l’extraction des métaux (Vachon et al., 1994; Tzeferis et al., 1994; Bosshard et al., 1996; Mulligan et al., 1999; Torrès, 2000; Ouattara, 2008). Les travaux de Ouattara, 2008 montrent que cette méthode pourrait être économiquement rentable pour l’extraction des métaux et permettait de protéger l’environnement. Cependant, elle est tributaire du type de résidus miniers (sulfures et métaux en présence), du type de champignon (Aspergillus niger et Penicillium
simplicissimum) et du type de substrat de culture utilisé (perméat de lactosérum). Pour ce
faire, cette biotechnologie représenterait, un moyen d’extraction des métaux précieux et de métaux lourds qui peuvent occasionner des pollutions de l’environnement. Les acides organiques produits par les champignons et utilisés pour la lixiviation sont disponibles dans le commerce et à coût relativement abordable.
Compte tenu des découvertes de plus en plus nombreuses de gisements à faibles teneurs et des quantités énormes de résidus miniers issus de l’exploitation minière, la lixiviation par les acides organiques pourrait représenter une alternative par rapport aux méthodes traditionnelles déjà existantes et devrait permettre un respect, encore plus accru des normes environnementales.
Dans le traitement des sols contaminés aux métaux lourds, les ligands susceptibles de former des complexes sont parfois utilisés pour l’extraction des métaux (Yeung et Gu, 2012). L’extraction des métaux éviterait une éventuelle oxydation, et les résidus non acido-gènes pourraient être utilisés pour le remblayage ou dans la construction en fonction de leurs paramètres géotechniques.
D’autre part, face aux nombreux problèmes liés au DMA issu des mines en activité et de celles abandonnées, le traitement des effluents miniers permet de limiter ou d’enrayer leurs conséquences. Plusieurs méthodes de traitement ont été expérimentées, dont les plus importantes sont celles utilisant les calcaires et la chaux.