LE POTENTIEL DIDACTIQUE DU POTENTIEL CHIMIQUE
Paolo LUBINI
Alta Scuola Pedagogica, Locarno (Suisse)
MOTS-CLÉS : POTENTIEL CHIMIQUE – POUSSÉE – COURANT – RÉSISTANCE – ANALOGIES
RÉSUMÉ : L’explicite utilisation du concept de potentiel chimique (m) permet de décrire de façon cohérente, systémique et systématique les phénomènes qui impliquent des transformations de substances sans devoir recourir explicitement aux concepts d’énergie et d’entropie. Elle permet aussi de saisir de nombreuses analogies à un niveau structurel avec d’autres branches des sciences naturelles tels que l’hydraulique, la thermologie, l’électricité en termes de poussées, courants et résistances.
ABSTRACT : The explicit use of the concept of chemical potential allows to describe the phenomena related to the transformations of substances at a first and phenomenological level, as well as in a coherent, systemic, and systematic way without the need of the concepts of energy and entropy. Additionally, such an approach offers the opportunity to exploit the analogies with other branches of the natural sciences, such as hydraulics, thermodynamics, or electricity, in terms of driving forces, currents, and resistances.
1. INTRODUCTION
Le concept de potentiel chimique mi pour un corps pur, introduit par W. Gibbs à la fin du XIX
siècle, est d’habitude présenté dans les livres de thermodynamique comme la dérivée partielle de l’énergie libre (G) par rapport à la quantité de substance à pression et température constantes et comme telle a les dimensions de J mol-1 :
,,jiipTnGnµ∂=∂
C’est surtout à cette définition, bien que rigoureuse du point de vue formel, que le concept de potentiel chimique doit sa réputation de grandeur difficile et improposable dans un cours de chimie pour débutants. Il est toutefois possible d’utiliser le concept de potentiel chimique sans devoir connaître dans les détails les argumentations thermodynamiques qui ont amené à sa définition.
2. POTENTIEL CHIMIQUE ET POUSSÉE POUR UNE TRANSFORMATION
Ainsi qu’une différence de température peut être considérée comme la poussé qui est responsable du transfert de la chaleur (entropie) entre deux corps, ou ainsi qu’une différence du potentiel électrique peut être considérée comme la poussée qui est responsable du courant électrique dans un circuit, dans la même façon, par analogie, une différence du potentiel chimique peut être considérée comme la poussée pour un changement physico-chimique. Dit en d’autres termes, pour établir si, dans le contexte d’une réaction chimique, le passage d’un système donné d’une situation A à une nouvelle situation B est spontanément possible, il suffit de comparer la valeur du potentiel chimique de l’état initial avec celle de l’état final : si le potentiel chimique diminue, alors la transformation sera possible, si m reste inchangé, on aura une situation d’équilibre chimique, et si m augmente, la transformation, ainsi décrite, ne pourra pas avoir lieu spontanément (Figure 1). Dans ce dernier cas, pour réaliser la transformation il sera nécessaire de recourir à une intervention externe : à quelque chose qu’on pourrait bien appeler une « pompe chimique ».
L’utilisation de ce simple critère nous permet de répondre assez aisément à des questions du type : certaines espèces chimiques auront tendance à réagir chimiquement entre elles ? Dans quel état d’agrégation se présentera un corps pur dans des conditions de pression et température données ? Quelle tendance aura un corps pur à diffuser dans une certaine ambiance ?
Figure 1 - On considère une transformation quelconque. Pour déterminer si elle pourra ou non se réaliser spontanément, il suffira de comparer les potentiels chimiques des deux états. Dans le cas où les deux situations auront le même
potentiel chimique, on aura un état d’équilibre chimique.
L’idée de poussée (telle qu’une différence du potentiel) en tant que “moteur” pour un changement est un outil d’analyse très puissant pour la rationalisation des phénomènes naturels : en électricité on a en effet une différence du potentiel électrique comme poussée pour un courant électrique, en thermologie on a une différence du potentiel thermique (différence de température) en tant que poussée pour un courant de chaleur (entropie), en hydraulique on a une différence de pression en tant que poussée pour un courant d’un volume d’eau. Ces analogies ont été résumées dans le tableau 1.
Poussée Courant
Chimie Différence de potentiel chimique Courant chimique
Électricité Différence de potentiel électrique Courant électrique
Thermologie Différence de potentiel thermique Courant d’entropie
Hydraulique Différence de pression Courant d’eau
Tableau 1 - Un regard d’ensemble : pour chaque domaine sont indiquées les poussées (différences de potentiel) et les respectifs courants. Le terme Ix représente l’intensité du flux qui décrit l’échange de la respective grandeur extensive
(charge électrique, entropie, volume d’eau) entre l’intérieur du système considéré et l’environnement.
2.1. Les valeurs du potentiel chimique pour les corps simples
Ainsi que la température d’ébullition, la densité, la capacité thermique, la masse molaire et beaucoup d’autres propriétés des différentes substances peuvent être déterminées expérimentalement et ont étés rassemblées dans des tableaux, de la même façon les valeurs des potentiels chimiques des différents corps ont étés mesurées et mises dans des tables. Pour nous
introduire au concept de potentiel chimique, considérons quelques valeurs relatives à des corps simples (Tableau 2) [1].
Étant donné que dans les réactions qui se produisent habituellement, le nombre d’atomes de chaque élément se conserve, nous disposons pour la détermination des potentiels chimiques d’autant de degrés de liberté que d’éléments chimiques. Ainsi, par convention, on a décidé d’assigner la valeur de 0 kJ mol-1 au corps simple du respectif élément dans la forme allotropique plus stable à la température de 298 K et à la pression de 101 kPa. Le degré de liberté mis à disposition par l’élément Carbone, par exemple, et utilisé en assignant la valeur du potentiel chimique 0 kJ mol-1 à la graphite. Le diamant, une autre forme allotropique du Carbone, a, par contre, un potentiel chimique de + 3 kJ mol-1 : on peut ainsi immédiatement déduire que le diamant est soumis à une poussée pour se transformer en graphite.
Élément Corps simple Formule chimique µ [kJ mol-1]
Carbone Diamant C +3
Graphite C 0
Iode Diiode (solide) I2 0
Diiode (liquide) I2 +3
Diiode (gazeux) I2 +19
Oxygène Oxygène monoatomique O +232
Dioxygène O2 0
Ozone O3 +163
Tableau 2 - Comparaison entre les potentiels chimiques de quelques corps simples. Les valeurs se réfèrent aux corps purs respectifs à la température de 298 K et à la pression de 101 kPa. Les données correspondent aux valeurs de l’énergie libre molaire de formation (∆G°f) que l’on trouve habituellement dans les tables de thermodynamique.
2.2. Les valeurs du potentiel chimique pour les corps composés
On peut tirer d’autres considérations de caractère plus général en considérant les potentiels chimiques de quelques corps composés reportés dans le tableau 3. La plupart des corps composés a un potentiel chimique négatif. Cela signifie que ces corps composés, dans les conditions de température et pression indiquées, ne montrent aucune tendance à se décomposer dans les respectifs corps simples des éléments dont ils sont composés : eau, carbonate de calcium, quartz, comme on sait bien, peuvent être conservés dans une boîte fermée (Figure 2). D’autres corps composés, au contraire, ont un potentiel chimique positif. Cela signifie que ces corps composés ont une tendance à se décomposer dans les corps simples des respectifs éléments dont ils sont composés. À cette catégorie de corps composés appartient, par exemple, l’azoture de sodium, une substance, qui, entre
autre, trouve des intéressantes applications techniques dans les dispositifs d’airbag [2] (Figure 3).
Élément Formule chimique µ [kJ mol-1]
Marbre CaCO3 -1128 Quartz SiO2 -805 Sel NaCl -384 Sucre C12H22O11 -1544 Glucose C6H12O6 -2743 Éthanol C2H6O -175 Eau H2O -237 Dioxyde de carbone CO2 -394 Acétylène C2H2 +209
Azoture de sodium NaN3 +91
Tableau 3 - Potentiels chimiques de quelques corps composés. Les valeurs se
réfèrent aux corps purs respectifs à la température de 298 K et à la pression de
101 kPa.
Figure 2 - Un valeur négative du potentiel chimique indique que la substance considérée peut être produite à partir des corps simples des éléments qui la composent, respectivement que le corps composé ne montre aucune tendance à se
décomposer dans les corps simples des éléments qui le composent.
Figure 3 - Un valeur positive du potentiel chimique indique que la substance considérée ne peut pas être produite à partir des corps simples des éléments qui la composent sans une intervention externe, respectivement que le corps
composé montre une tendance à se décomposer dans les corps simples des éléments qui le composent.
Le tableau des potentiels chimiques peut aussi être utilisé pour prévoir si une transformation pourra ou non se dérouler dans une certaine direction. Par exemple, dans la figure 4 est reporté le calcul nécessaire pour établir si l’oxydation du glucose est spontanée ou pas.
3. RÉSISTANCE À LA TRANSFORMATION
Il y a beaucoup de substances qui sont plus ou moins stables même si d’après leurs potentiels chimiques elles devraient se transformer dans les corps simples des respectifs éléments dont elles sont composées. Malgré son potentiel chimique positif, le diamant ne se transforme pas en graphite. En plus, il y a de nombreuses réactions chimiques qui ne se déroulent pas, même si le potentiel chimique des produits est inférieur à celui des réactifs : le glucose, le bois, la plastique et … nous-mêmes devrions réagir avec le di-oxygène de l’air, mais cela n’est pas observé ! Jusqu’à présent, on n’a pas considéré la dimension temporelle : on n’a rien dit à propos de l’intensité du courant chimique d’une réaction, In(Réaction, ce qui caractérise la rapidité avec laquelle un processus se
vérifie. Cette intensité de courant n’est pas déterminée uniquement par la poussée (différence de potentiel chimique) mais aussi, et de manière décisive, par la résistance à la réaction. La figure 5 résume les facteurs qui contribuent à déterminer l’intensité du courant chimique avec laquelle une transformation a lieu.
Figure 5 - Représentation schématique des facteurs qui influencent l’intensité du
courant chimique avec laquelle une transformation chimique se réalise1[28].
Une description des transformations chimiques basée sur les concepts de courant (en tant que taux de transformation des substances), de poussée (due à une différence de potentiel chimique) et de résistance permet de saisir à un niveau structurel de nombreuses analogies avec les autres branches d’étude des phénomènes naturels, ce qui, par un développement habituel n’est pas nécessairement le cas (Figure 6).
1 Dans ce contexte il faut absolument souligner que entre différence de potentiel chimique et résistance de réaction il
n’y a aucune relation directe. Par exemple, si l’on sait qu’une transformation est décrite par une grande différence de potentiel chimique, cette information ne permet en aucun cas de tirer des conclusions par rapport à la valeur de la résistance chimique qui caractérise cette transformation. Dans d’autres mots, la seule connaissance de la différence de potentiel chimique ne permet de faire aucune prévision par rapport à la rapidité avec laquelle cette transformation aura lieu.
Figure 6 - Re ation entre les concepts de (intensité de) courant, poussée et résistance. On peut noter l’analogie avec l’électricité (courant électrique IQ, tension électrique Dj et résistance électrique Rélectrique), la thermologie (courant
d’entropie IS, différence de température DT et résistance thermique Rthermique) et l’hydraulique (courant du liquide IV,
différence de pression DP et résistance hydraulique Rhydraulique).
4. DÉPENDANCE DU POTENTIEL CHIMIQUE PAR RAPPORT À LA TEMPÉRATURE, À LA PRESSION ET À LA CONCENTRATION
Pour étendre l’utilisation du concept de potentiel chimique à des situations différentes de celles qui font référence à des conditions standards (température 298 K, pression 101 kPa, concentration 1,0 M), il faut pouvoir disposer d’une description de la variation de la valeur du potentiel chimique en fonction de la température, la pression et, dans le cas de solutions aqueuses, de la concentration. À ce propos, déjà avec une simple approximation « zéro », on peut obtenir des résultats très intéressants en réduisant au minimum la mathématique nécessaire. Il s’agit simplement d’assumer, pour le potentiel chimique, une dépendance linéaire par rapport au paramètre considéré dans les immédiats alentours des conditions relatives à l’état standard de référence. Cette approche, exemplifiée dans la figure 7 pour le cas de la dépendance du potentiel chimique par rapport à la température, permet d’obtenir des formules relativement simples et de facile compréhension2.
Dans une façon tout à fait analogue, on peut obtenir les formules reportées en figure 8 et qui décrivent, dans une approximation « zéro », la dépendance du potentiel chimique par rapport à la température, à la pression et à la concentration.
Figure 7 - Dépendance du potentiel chimique par rapport à la température pour
une substance hypothétique à l’état solide respectivement liquide dans l’approximation « zéro ». Le coefficient de
proportionnalité linéaire correspond, dans le cas de la température, à la valeur négative de l’entropie molaire de la
substance en question.
Figure 8 - Expressions de la dépendance du potentiel chimique par rapport à la
température, à la pression et à la concentration. On peut noter comment,
dans quelques cas, au lieu de l’approximation linéaire, on utilise une
approximation logarithmique. Cela permet d’étendre la validité de l’approximation sur un intervalle plus
grand.
4.1. Passages d’état à pression constante dus à des changements de température
Comme premier exemple d’application des relations exprimées dans la figure 8, on peut considérer la description du changement d’état de l’eau de liquide à solide à pression constante. Dans la figure 9, sont illustrés les passages qui permettent de calculer la température de fusion de l’eau en imposant que, dans les états de coexistence, le potentiel chimique de la phase liquide doit être égal à celui de la phase solide (situation d’équilibre).
Figure 9 - Calcul de la température de fusion de l’eau à la pression de 101 kPa et relative représentation graphique (données utilisées : T° = 298 K, P° = 1 bar, µ°C(graphite) = 0 kJmol-1, µ°C(diamant) = +2.9 kJmol-1, V°C(graphite) = 0.54 Jbar -1mol-1, = V°
4.2. Passages d’état à température constante dus à des changements de pression
Dans ce deuxième exemple, on veut calculer la pression à partir de laquelle, à température constante, la graphite peut se transformer spontanément en diamant. Comme dans le cas précédent, le calcul peut être formulé en imposant une condition d’équilibre entre les deux phases (Figure 10).
Figure 10 - Calcul de la pression nécessaire pour pouvoir transformer la graphite en diamant (on considère une température de 298 K) et relative représentation graphique (données utilisées : p° = 1 bar, µ°C(graphite) = 0 kJmol-1,
µ°C(diamant) = +2.9 kJmol-1, V°C(graphite) = 0.54 Jbar-1mol-1, = V°C(diamant) = 0.34 Jbar-1mol-1).
4.3. La tension de vapeur de l’éthanol
Comme dernier exemple, nous proposons une situation un peu plus complexe : celle relative à la tension de vapeur de l’éthanol. Dans ce cas, on doit considérer en même temps la dépendance du potentiel chimique par rapport à la température et à la pression. À remarquer, dans la figure 11, l’accord entre les valeurs expérimentales et celles calculées.
Figure 11 - La tension de vapeur de l’éthanol. Les valeurs calculées ont été obtenues à partir de l’équation ci-dessus. À remarquer l’accord entre les valeurs expérimentales et celles calculées.
4.4. Un regard d’ensemble
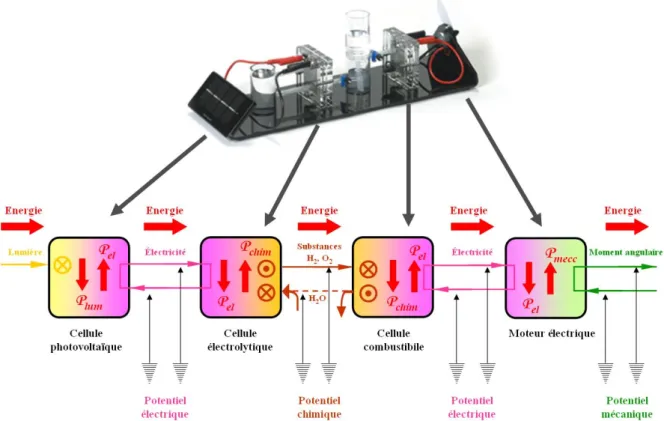
L’utilisation du potentiel chimique, respectivement de la différence du potentiel chimique comme poussée pour une réaction chimique, permet de décrire en termes de poussées, courants et résistances, les flux énergétiques à travers des dispositifs plus ou moins simples comme celui illustré dans la figure 12. Dans cette situation, on utilise des symboles et un cadre conceptuel de référence qui permet de saisir et valoriser les analogies entre les différents domaines des sciences naturelles.
Figure 12 - Description du flux énergétique dans un dispositif constitué par une cellule photovoltaïque, une cellule électrolytique, une cellule combustible et un moteur électrique raccordés en série. La schématisation proposée explicite
l’utilisation du concept de potentiel chimique. Dans le schéma, on suppose aussi un rendement du 100 %, c’est-à-dire qu’on suppose qu’il n’y ait pas de production d’entropie : les différentes puissances sont entièrement utilisées pour créer
des différences de potentiel (électrique, chimique ou mécanique).
5. CONCLUSION
L’explicite utilisation du concept de potentiel chimique (m) permet de décrire de façon cohérente, systémique et systématique les phénomènes qui impliquent des transformations de substances sans devoir recourir explicitement aux concepts d’énergie et d’entropie. Elle permet aussi de saisir de nombreuses analogies à un niveau structurel avec d’autres champs des sciences naturelles. Le potentiel chimique résulte ainsi être une grandeur centrale et transversale à toute la chimie et, plus
en général, à tous les champs d’étude confrontés avec des transformations de substances. En se référant au jeu des analogies, on pourrait même ajouter que renoncer à l’explicite utilisation du concept de potentiel chimique dans la présentation de la chimie, ça serait comme vouloir parler de thermologie sans discourir de température, ou traiter l’hydraulique sans considérer la pression, ou encore décrire l’électricité sans présenter le potentiel électrique …
BIBLIOGRAPHIE
Une récolte des valeurs des potentiels chimiques peut être repérée au site de la Job Stiftung : http://www.jobstiftung.de/de/page.php?Text=dat/index.php&Top=dat/top.php
MADLUNG A. (1996). J. Chem. Educ.73, 347-348.
JOB G. (1972). Neudarstellung der Wärmelehre. Frankfurt am Main : Akademische Verlagsgesellschaft.