Solubilité et cinétique de réaction de l'oxyde de nickel dans les conditions du circuit primaire d'un réacteur à eau sous pression
202
0
0
Texte intégral
Figure




+7
Outline
Calculs thermodynamiques
Influence d’un ligand sur la solubilité de NiO
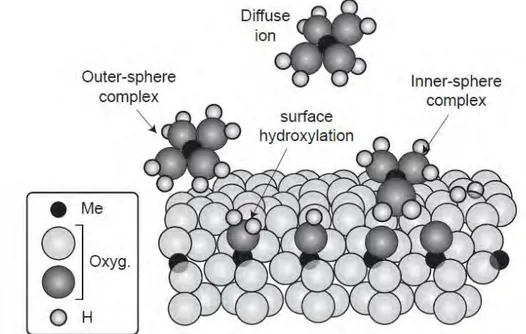
Mécanismes à l’interface solide/liquide
Modélisation des phénomènes de complexation de surface
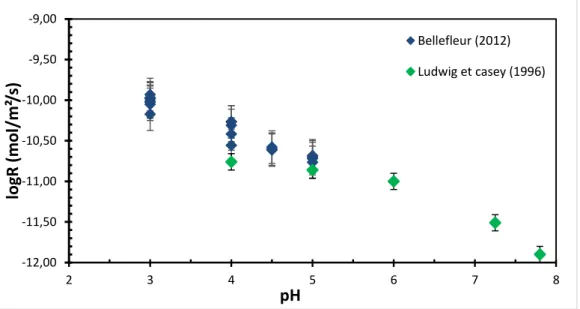
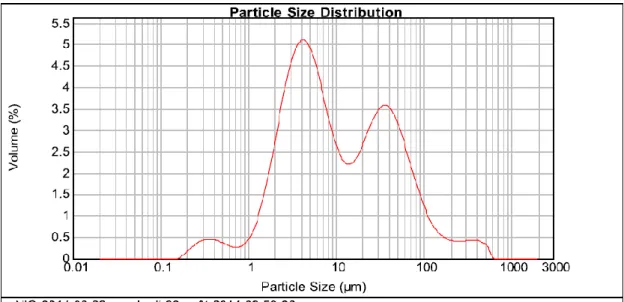
Mesures expérimentales des cinétiques de dissolution de NiO
Discussion
Définition des conditions de modélisation
Modélisation des résultats expérimentaux en milieu acide chlorhydrique
Modélisation des résultats en milieu bore lithium
Application des résultats au circuit primaire
Documents relatifs