UNIVERSITÉ MOHAMMED
Faculté des Sciences, 4 Avenue Ibn Battouta B.P. 1014 RP, Rabat Tel +212 (0) 37 77 18 34/35/38, Fax
Discipline
Spécialité
AIDE A LA DETECTION
PAR LES TECHNIQUES DE SEGMENTATION ET DE
CODAGE DE TEXTURES DES IMAGES
Soutenue Le : 04 juillet 2012
Devant le jury
Président :
M. E.H. Bouyakhf
Examinateurs :
Mme. F. Regragui
M. A. Touzani
M. A. Tamtaoui
M. E .H. Ibn el haj
M. M. N. Boujida
M. M. T. Alaoui
UNIVERSITÉ MOHAMMED V – AGDAL
FACULTÉ DES SCIENCES
Rabat
Faculté des Sciences, 4 Avenue Ibn Battouta B.P. 1014 RP, Rabat
Tel +212 (0) 37 77 18 34/35/38, Fax : +212 (0) 37 77 42 61, http://www.fsr.ac.ma
Numéro d’ordre
THÈSE DE DOCTORAT
Présentée par
Fatima EDDAOUDI
Discipline : Sciences de l’Ingénieur
Spécialité : Informatique
AIDE A LA DETECTION DES PATHOLOGIES DU SEIN
PAR LES TECHNIQUES DE SEGMENTATION ET DE
CODAGE DE TEXTURES DES IMAGES
MAMMOGRAPHIQUES
: 04 juillet 2012
Professeur à la Faculté des Sciences de Rabat.
Professeur à la Faculté des Sciences de Rabat. Professeur à l’Ecole Mohammedia d’Ingénieurs
Professeur à l’Institut National des Postes et des Télécommunications
Professeur à l’Institut National des Postes et des Télécommunications
Professeur à Institut National d'Oncologie, S.Med Ben Abdellah Docteur à l’Académie Hassan II des Sciences et Techniques
AGDAL
Faculté des Sciences, 4 Avenue Ibn Battouta B.P. 1014 RP, Rabat – Maroc : +212 (0) 37 77 42 61, http://www.fsr.ac.ma
Numéro d’ordre : 2584
DES PATHOLOGIES DU SEIN
PAR LES TECHNIQUES DE SEGMENTATION ET DE
CODAGE DE TEXTURES DES IMAGES
Rabat.
Rabat. Mohammedia d’Ingénieurs
Professeur à l’Institut National des Postes et des Télécommunications Professeur à l’Institut National des Postes et des Télécommunications
logie, S.Med Ben Abdellah es Sciences et Techniques
I
Avant propos
Les travaux présentés dans cette thèse ont été réalisés au sein de l’unité de Formation de Recherche: Laboratoire d’Informatique, Mathématiques Appliquées, Intelligence Artificielle et Reconnaissance de Forme du Département de Physique de la Faculté des Sciences de Rabat.
Je veux spécialement remercier mon directeur de recherche Madame F.REGRAGUI, Professeur à la Faculté des Sciences de Rabat et lui exprimer ma gratitude pour sa disponibilité et son soutien pendant ces années de recherche. Je la remercie également pour sa sympathie, son ouverture d’esprit et son sens critique. Qu’elle soit ici assurée de ma reconnaissance.
Je tiens à exprimer toute ma profonde gratitude à Monsieur E. H. BOUYAKHF, Professeur à la Faculté des Sciences de Rabat, pour m’avoir accueilli au sein du Laboratoire d’Informatique, Mathématiques Appliquées, Intelligence Artificielle et Reconnaissance de Forme. Je tiens à le remercier chaleureusement pour son aide et sa convivialité dans l’élaboration de ce travail. Je le remercie pour avoir accepté de présider mon jury.
Je remercie Monsieur A. TOUZANI, Professeur à l’école Mohammedia d’ingénieurs et directeur du CRASTE-LF (Centre Régional Africain des Sciences et Technologies de l’Espace en Langue Française) d’avoir accepter de participer à l’évaluation de mon travail. Je lui exprime ma gratitude pour sa disponibilité, pour sa sympathie. Qu’il soit ici assuré de ma reconnaissance.
Que Monsieur A. TAMTAOUI, Professeur à l’Institut National des Postes et des Télécommunications, trouve ici le témoignage de ma gratitude. Je lui exprime mes remerciements et ma reconnaissance pour avoir accepté d'être examinateur de ce manuscrit et pour les orientations scientifiques qu’il m’a suggérées et la grande disponibilité dont il a toujours fait preuve.
Je remercie Monsieur M. N. BOUJIDA, Professeur à Institut National d'Oncologie, Sidi Mouhamed Ben Abdellah de Rabat, pour m’avoir fait l’honneur de participer à mon jury de thèse.
II
Je tiens à remercier Monsieur E.H.IBN EL HAJ, Professeur à l’Institut National des Postes et des Télécommunications, pour me faire le grand plaisir d’accepter de joindre le jury de cette thèse.
Je remercie profondément Monsieur M. TAHIRI ALAOUI, Professeur à la Faculté des Sciences de Rabat, pour ses encouragements et pour avoir accepté de participer à mon jury.
Je remercie le Professeur M. HIMMI pour sa sympathie, sa courtoisie et ses encouragements durant ces années de thèse.
Je voudrais remercier mes amis et collègues : N. LAMOURI, A. MAHMOUDI,
M. HAMZAOUI et bien d’autres que je n’ai pas cités pour leur collaboration et leur
encouragement durant l’élaboration de ce travail.
III
Résumé
Ce travail de thèse contribue à la détection des microcalcifications par l’analyse et la classification des différents tissus constituant l’image mammographique. La nouveauté par rapport aux travaux antérieurs réside dans l’application des algorithmes d’analyse sur des images codées plutôt que sur les images initiales. L’approche développée consiste, d’abord, à localiser le muscle pectoral et l’éliminer de l’image car sa présence provoque un nombre élevé de faux positifs lors de la détection des masses suspectes. Cette étape se résume en deux phases. Une phase d’initialisation qui consiste en une automatisation de la recherche d’un contour initial représentant le muscle pectoral. Une deuxième phase d’évolution du contour initial basée sur des énergies calculées sur le contour et sur les régions. La combinaison des deux phases a donné des résultats très satisfaisants.
Une fois que nous avons éliminé le muscle pectoral de l’image, nous avons localisé les zones suspectes susceptibles de contenir une pathologie. Ces dernières sont caractérisées par une forte densité mammaire. En utilisant un seuillage basé sur les maxima, nous avons pu segmenter ces zones. L’intérêt d’introduire un seuillage réside dans la réduction de la région d’intérêt à moins de 30% de la surface de l’image initiale après élimination du fond, du muscle pectoral et des zones de faible densité. Les zones d’intérêt trouvées avec la méthode des maxima sont d’abord codées avec un codage adaptatif, puis finement analysées pour la recherche de microcalcifications. Ce codage consiste à attribuer à chaque pixel un code et non pas un niveau de gris.
L’approche développée a été testée sur deux types de pathologies : les masses de type circonscrite et les microcalcifications. Le taux de classification de ces pathologies en utilisant les SVM appliqués aux images codées est de 90%, quand on applique le codage adaptatif sur toute la partie de l’image représentant le sein, alors qu’il est de 95.8%, si on analyse seulement les parties de forte densité trouvées par la méthode des maxima.
La méthode développée permet de conserver la structure des images, tout en supprimant la notion de niveau de gris. Les résultats expérimentaux ont montré que le concept de la texture semble beaucoup plus présent dans les images codées par le codage adaptatif que dans les images codées par le codage d’extrema ou le codage simple sur 16 niveaux de gris. De plus, le codage adaptatif permet de réduire la taille des données traitées, ce qui réduit le temps de calcul.
Mots-clefs : Analyse Statistique, Classification, Codage adaptatif,
IV
Abstract
This thesis contributes to the microcalcifications detection by analyzing and classifying different tissues constituting the mammographic image. Compared to previous works, the innovation here is that the processing is performed in the coded images instead of the original ones. The approach consists, first, in locating the pectoral muscle and eliminating it from the image because its presence causes a high number of false positives during the detection of suspicious masses. This step is summarized in two phases. An initialization phase which consists of an automated search for an initial contour representing the pectoral muscle and a second phase of evolution of this contour. This evolution is done using active contours based on energies calculated on the contour and regions. The combination of the two phases gave very satisfactory results.
The second step is to locate suspicious zones that may contain disease. These areas are characterized by high breast density which can be segmented by using a threshold based on the maxima. The advantage of introducing a thresholding is to reduce the region of interest less than 30% of the surface of the initial image after removing the background, the pectoral muscle and low density areas. Once found, the areas of interest are first encoded with an adaptive coding and finely analyzed to search for microcalcifications.
The approach developed was tested on two types of pathologies: circrumscribed masses and microcalcifications. The classification rates of these diseases using the SVM classifier applied to the coded images is 90%, when we applied the adaptive coding on the whole part representing the breast in the image, whereas it is 95.8%, when we apply our approach on the parts of high density found by the maxima method.
The developed method preserves image structure, while eliminating the notion of gray level. The experimental results showed that the texture concept is more present in the images encoded by the adaptive coding that in images encoded by runk coding or simple coding using 16 gray levels. So the adaptive coding makes the detection of microcalcifications more effective. In addition, the adaptive coding reduces the size of data processed, which reduces the computation time.
Keywords: Adaptatif Coding, Classification Mammography, Pectoral muscle, Segmentation, Statistical Analysis, Texture analysis.
V
Table des matières
Introduction
Chapitre I : : Mammographie numérique et diagnostic assisté par ordinateur
1.1- Mammographie et constitution des images mammographiques ... 1
1.1.1- Anatomie du sein ... 1
1.1.2- Le cancer du sein ... 3
1.1.3- Les facteurs de risque du cancer du sein ... 3
1.1.4- Les types de cancer du sein ... 4
1.1.4.1- Les masses ... 4
1.1.4.2- Les microcalcifications ... 5
1.1.5-Mammographie ... 7
1.1.5.1-Formation de l’image mammographique... 7
1.1.5.2- Limitations de la mammographie ... 9
1.2- Mammographie numérique et diagnostic assisté par ordinateur ... 10
1.2.1- Mammographie numérique ... 10
1.2.2- Qualité de l’image mammographique numérique ... 11
1.2.3- Diagnostic Assisté par Ordinateur (DAO) en mammographie numérique ... 12
1.3- Bases de données des mammogrammes numériques ... 13
1.3.1-Mammography Image Analysis Society (MIAS) ... 13
1.3.2- La base de données numérique de dépistage par mammographie (DDSM) . 15 Bibliographie………...17
Chapitre II : Segmentation des images à niveau de gris 2.1-Principe de la segmentation ... 21
2.2- Segmentation basée sur l’approche contour ... 23
2.2.1- Les opérateurs de détection de contours ... 23
2.2.1.1- L’approche gradient ... 23
2.2.1.2- L’approche Laplacien ... 25
2.2.2- Localisation des contours ... 26
2.2.3- Suivi de contours ... 27
2.2.4- Fermetures des contours ... 27
2.3- Méthodes basées sur l’approche région ... 28
VI
2.3.1.1- Segmentation par ligne de partage des eaux ... 29
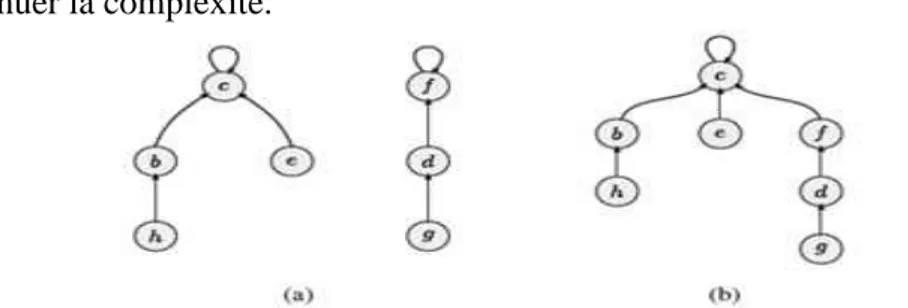
2.3.1.2- Segmentation par transformée en forêt ... 31
2.3.2- Approche fonctionnant par fusion et division de région. ... 32
2.3.2.1-Segmentation par division (Split) ... 33
2.3.2.2-Segmentation par fusion (Merge) ... 33
2.3.2.3-Segmentation par division-fusion (Split and Merge)... 34
2.4- Méthodes basées sur l’approche classification de pixels ... 34
2.4.1- Méthodes monodimensionnelles ou seuillage ... 34
2.4.2- Méthodes de segmentation par regroupement... 36
2.4.3- Méthodes multidimensionnelles ... 36
2.5- Segmentation par les contours actifs ... 37
2.5.1- Modèles déformables ... 37 2.5.2- Contours actifs ... 38 2.5.2-1- Énergie interne ... 39 2.5.2-2- Énergie externe ... 39 2.5.2.3- Énergie de contexte... 40 2.5.3- Différences finies ... 40
2.5.4- Méthodes d’optimisation de la fonctionnelle d’énergie ... 41
2.5.4.1- Optimisation par approche variationnelle ... 41
2.5.4.2- Optimisation par la programmation dynamique ... 43
2.5.5- Contours actifs basés contours ... 44
2.5.6 Contours actifs basés région ... 45
2.5.6.1- Principe des contours actifs basés région ... 47
2.5.6.2- Dérivation des termes basés contour et basés régions ... 48
2.5.7- Implémentation ... 53
2.5.7.1- Approche implicite : Les ensembles de niveaux ... 54
2.5.7.2- Approche explicite : Les modèles paramétriques ... 55
2.6- Segmentation en utilisant l’approche coopérative ... 56
Bibliographie……….……...58
Chapitre III: Segmentation et analyse des images texturées 3.1- Notion de textures ... 65
3.2- Extraction d’attributs texturaux dans les images à niveau de gris ... 68
3.2.1-Analyse des textures par les modèles structurelles ... 68
3.2.1.1- Spectre de texture ... 69
3.2.1.2- Polygones de Voronoï ... 70
3.2.2- Analyse des textures par les méthodes fréquentielles ... 71
3.2.2.1- Transformée de Fourier ... 71
3.2.2.2- Filtre de Gabor ... 72
VII
3.2.3- Les méthodes d’analyse de textures basées sur un modèle ... 74
3.2.3.1- Les fractales ... 74
3.2.3.2- les champs de markov ... 75
3.2.4- Analyse des textures par les méthodes statistiques ... 77
3.2.4.1- Statistiques du premier ordre ... 77
3.2.4.2- Caractéristiques d’auto-corrélation ... 77
3.2.4.3 - Les matrices de longueurs de plages ... 79
3.2.4.4- Les Matrices de Cooccurrence... 79
3.2.4.5- Les matrices des différences de niveaux de gris ... 79
3.3-Critères de choix d'une méthode d’analyse de texture et d’attributs texturaux ... 80
Bibliographie………...……...83
Chapitre IV : Analyse des images par codage de textures 4.1- Extrema de gris... 88
4.1.1-Les extrema globaux ... 89
4.1.2- Les extrema locaux ... 89
4.1.3- Les extrema d’ordre ... 89
4.2- Technique de codage par extrema de gris ... 90
4.2.1- Codage d’extrémalité local ... 90
4.2.2- Codage d’extrémalité régionale ... 92
4.2.3- Codage d’extrémalité local amélioré ... 93
4.3- Codage Directionnel Local ... 94
4.4- Approche proposée pour le codage de textures des images mammographiques .... 97
4.4.1- principe de la Méthode proposée ... 97
4.4.2- Résultats ... 99
Bibliographie………..103
Chapitre V- Segmentation des mammogrammes et localisation des zones d’intérêt 5.1- Détection du contour extérieur du sein ... 106
5.1.1- Méthodes basées sur l’analyse de l’histogramme ... 107
5.1.2- Méthodes basées sur le gradient ... 108
5.1.3- Méthodes basées sur une modélisation polynomiale ... 108
5.1.4- Méthodes basées sur les contours actifs ... 109
5.1.5- Méthodes basées sur la classification ... 109
5.1.6- Approche adoptée sur la base de la méthode d’Otsu ... 109
5.2-Segmentation du muscle pectoral ... 111
5.2.1- Approche proposée pour la segmentation du muscle pectoral ... 112
5.2.1.1- Phase d’initialisation ... 112
5.2.1.2- Phase d’évolution du contour ... 119
VIII
5.3- Segmentation des zones d’intérêt ... 125
5.3.1-Densité mammaire ... 125
5.3.1.1-Classification des mammogrammes par leur densité mammaire .... 126
5.3.1.2- Mesure automatique de la densité du sein ... 127
5.3.2- Approche proposée pour la localisation des zones d’intérêt ... 128
Bibliographie……….………...…….….131
Chapitre VI : Détection des microcalcifications par l’analyse des textures appliquée à des images codées 6.1- Revue de la bibliographie sur la détection des microcalcifications ... 138
6.2- Détection des microcalcifications par analyse de textures des images codées ... 139
6.2.1- Choix de la taille de la fenêtre d’analyse ... 139
6.2.2- Paramètres de caractérisation de textures ... 143
6.2.2.1- Attributs radiaux ... 143
6.2.2.2- Attributs de la matrice de cooccurrence ... 144
6.2.2.3- Attributs de la matrice de longueur des plages ... 148
6.3- Application à la détection des microcalcifications : résultats et discussions ... 150
Bibliographie……….…....155
Conclusion générale……….…..159
Liste des contributions………..………..…...162 Annexe I
IX
Liste des figures
Figure 1.1: Schéma anatomique du sein ... 2
Figure 1.2: Les types de masses ... 5
Figure 1.3: Les différents types de bords de masses ... 5
Figure 1.4: Exemple de calcifications bénignes ... 6
Figure 1.5: Exemple de calcifications malignes ... 7
Figure 1.6: Méthode utilisée pour la prise d’un mammogramme ... 8
Figure 1.7: Incidence CC et l’incidence MLO pour l’acquisition d’un mammogramme ... 9
Figure 2.1: Segmentation par approche contour et par approche région ... 22
Figure 2.2: Principe de la segmentation par approche région, contour ou classification .... 22
Figure 2.3: Le gradient entre 2 régions d’une image ... 24
Figure 2.4: Dérivée partielle selon x, ( ( , ) ) et y, ( ( , ) ) ... 24
Figure 2.5: les opérateurs les plus populaires utilisant le gradient ... 25
Figure 2.6: Les 3 masques de dérivation de Sobel ... 25
Figure 2.7: Masque d’approximation du laplacien ... 26
Figure 2.8: Segmentation par le principe de la croissance de régions ... 29
Figure 2.9: Segmentation par la méthode de ligne de partage des eaux ... 30
Figure 2.10: Exemple de segmentation par ligne de partage des eaux ... 30
Figure 2.11: Exemple de sur-segmentation lors d’un traitement... 31
Figure 2.12: Une forêt d’ensemble disjoints. ... 32
Figure 2.13: Subdivision d’une image jusqu’à la convergence ... 33
Figure 2.14: Binarisation d’un mammogramme avec la méthode d’OTSU ... 36
Figure 2.15: Principe de fonctionnement des contours actifs : évolution ... 38
Figure 2.16: Construction d’une B-spline cubique ... 56
X
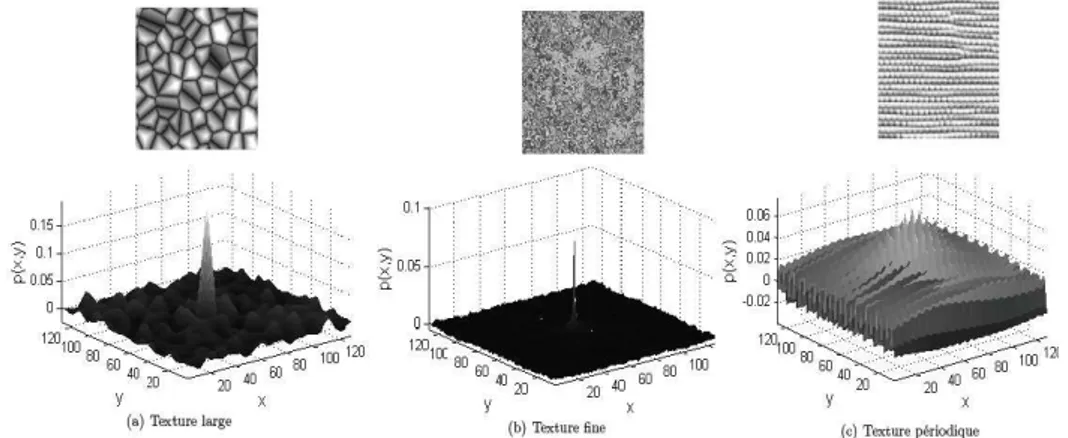
Figure 3.2: Différents types de textures... 66
Figure 3.3: Exemple de textures aléatoires ... 67
Figure 3.4: Exemple de textures structurelles ... 67
Figure 3.5: Exemple de textures directionnelles ... 68
Figure 3.6: Construction des unités de textures en croix et en diagonale ... 70
Figure 3.7: Décomposition en ondelettes d’une image 2D ... 74
Figure 3.8: Représentation d’un système de voisinage d’ordre 2... 75
Figure 3.9: Ensemble de cliques pour un système de voisinage d’ordre 2(8-connexe) ... 76
Figure 3.10: Exemple de fonctions d’auto-corrélation ... 78
Figure 4.1: Principe de codage d’une texture à niveaux de gris ... 88
Figure 4.2: Extrema de gris ... 89
Figure 4.3: Codage d’extréma ... 90
Figure 4.4: Principe du codage d’un pixel x en fonction de ses voisins ... 91
Figure 4.5: Exemple du codage de niveau de gris d’un pixel... 91
Figure 4.6: Exemples de plateaux d’extrema régionaux ... 92
Figure 4.7: Définition du voisinage d’un plateau ... 92
Figure 4.8: Unité de texture ... 94
Figure 4.9: Sous-voisinages CTU (a) et DTU (b) d'un voisinage de 3x3 pixels ... 95
Figure 4.10 : Détermination du CDL d’un voisinage de 3x3 pixels ... 96
Figure 4.11: Méthode proposée: codage adaptatif des NG d’un mammogramme ... 97
Figure 4.12: Histogramme initial ... 98
Figure 4.13: Réduction du nombre de niveaux de gris d’une fenêtre de taille 5x5 pixels . 98 Figure 4.14: Codage des pixels après réduction des niveaux de gris ... 99
Figure 4.15: Illustration des résultats du codage adaptatif ... 99
Figure 4.16: Résultats du codage d’un mammogramme par le codage d’extrémalité local amélioré et le codage simple sur 16 niveaux de gris ... 100
Figure 4.17: Mammogrammes codés par trois méthodes de codage ... ..101
Figure 5.1: Etapes adoptées pour la détection des microcalcifications…………..………106
Figure 5.2: L’histogramme d’un mammogramme……….108
XI
Figure 5.4: Initialisation manuelle utilisée pour les contours actifs ... …113
Figure 5.5: Etapes d’estimation du contour du muscle pectoral par une ligne droit……. 114
Figure 5.6: Représentation d’un mammogramme: Notation utilisée……….115
Figure 5.7: Histogramme de la région d’intérêt R1……….………...116
Figure 5.8: Algorithme de calcul du seuil t ... 117
Figure 5.9: Résultats du seuillage de la région d’intérêt R1 par seuil t ... 117
Figure 5.10: Elimination des points concaves ... 118
Figure 5.11: Estimation de la ligne AB représentant le muscle pectoral ... 119
Figure 5.12: Technique de lissage du contour ... 120
Figure 5.13: Zone d’influence construite à partir de la normale d ... 122
Figure 5.14: Zone de déplacement autorisé pour un point ... 123
Figure 5.15: Estimation du contour du muscle pectoral par une ligne droite…...……….123
Figure 5.16: Résultats de la segmentation du muscle pectoral ... 123
Figure 5.17: Segmentation du muscle pectoral par la méthode de proposée ... 124
Figure5.18: Représentation d’une image à niveau de gris par la méthode de Maxima ... 129
Figure 5.19: Segmentation des mammogrammes par la méthode des maxima………….130
Figure 6.1: Méthode proposée pour la localisation des microcalcifications ... 137
Figure 6.2 : Méthode adoptée pour la détection des microcalcifications ... 139
Figure 6.3: Intérêt de la régionalité sur l’information ... 140
Figure 6.4: Influence de la résolution sur l’information obtenue d’une texture ... 141
Figure 6.5: Distribution radiale Rad réalisée à l’aide d’une fenêtre carrée de taille R. .... 144
Figure 6.6: Distribution radiale directionnelle Radd ... 144
Figure 6.7: Construction de la matrice de cooccurrence ... 145
Figure 6.8: Notation utilisée pour le vecteur de déplacement ... 147
Figure 6.9: Construction de la matrice de longueur des plages ... 148
XII
Liste des tableaux
Tableau 1.1: Nombre de mammogrammes dans la base de données MIAS………... Tableau 1.2: Nombre de mammogrammes contenant des masses dans la base MIAS……… Tableau 3.1: Tableau des caractéristiques calculées sur les polygones de Voronoï ………... Tableau 5.1: Segmentation pour une combinaison d’énergies donnée……….……….. Tableau 5.2: Pourcentages des bonnes segmentations trouvées par plusieurs méthodes…… Tableau 5.3: Travaux sur la détection des masses………….……….. Tableau 5.4: Résultats de la pré-segmentation mammogrammes par les maxima……….… Tableau 6.1: Le nombre maximal de nombre de niveau de gris dans une fenêtre d’analyse.. Tableau 6.2: Combinaison de paramètres pour le calcul de la matrice de cooccurrence…… Tableau 6.3: Combinaisons de paramètres qui ont donné un taux de classifications > à 60% Tableau 6.4: Classification par SVM des mammogrammes codés contenant des masses Circ… Tableau 6.5: Classification par SVM des mammogrammes contenant des masses Circ ….... Tableau 6.6: Classification par SVM des mammogrammes codés contenant des
microcalcifications………. 14 14 71 124 125 128 129 142 148 151 151 152 153
INTRODUCTION
XIII
Introduction
Le cancer du sein est le cancer le plus fréquent dans le monde ; il constitue la première cause de décès chez les femmes. L'Agence Internationale de l'Organisation Mondiale de la Santé pour la recherche sur le cancer a déclaré que chaque année, plus de 150.000 femmes meurent du cancer du sein et un million de nouveaux cas sont détectés à l’échelle mondiale. En France, en 2005, son incidence est de 101.5 pour 100.000 personnes. Au Maroc, il constitue un véritable problème de santé publique. Selon les statistiques officielles de l’Institut National de l’Oncologie Sidi Mohammed Ben Abdellah, 16% des femmes ont développé un cancer du sein. Actuellement, on compte entre 13.000 et 15.000 nouveaux cas chaque année.
Les facteurs tels que le vieillissement de la population, les nouveaux modes de vie, l’obésité due à l’alimentation riche en graisse, la consommation régulière d’alcool (plus courante chez les femmes depuis quelques décennies) ainsi que le traitement hormonal substitutif, contribuent à l’augmentation de l’incidence de ce cancer. Ce dernier est un ensemble de cellules malignes, qui se multiplient sans contrôle jusqu’à créer une tumeur, s’attaquent aux tissus sains avoisinants. Il peut exister sous forme de masses ou de dépôts de sel de calcium appelées micro ou macro-calcifications utilisés comme des indices pertinents pour les radiologues pendant la phase d’analyse des mammogrammes afin de classifier ces derniers en normaux ou pathologiques.
Comme avec toute forme de cancer, le dépistage et le diagnostic précoce du cancer du sein est l'un des facteurs les plus importants contribuant à la guérison de la maladie. En effet, la mammographie est l’outil le plus utilisé pour une détection précoce de la maladie, car elle permet de produire des images de haute résolution du sein.
Actuellement, la mammographie numérique vient de compléter les performances de la mammographie traditionnelle. Elle a permis d’ouvrir la voie au traitement des images digitales avec une meilleure résolution. Son avantage par rapport à la mammographie traditionnelle réside dans le temps requis pour obtenir l’image mammographique qui s’affiche en moins de 10 secondes sur un moniteur de 1280x1024 de haute luminosité. En plus, le format numérique offre d’une part, la possibilité d’envoyer l’image numérique via les réseaux
INTRODUCTION
XIV
informatiques pour un diagnostic à distance ou une lecture par d’autres spécialistes. D’autre part, l’image numérique peut être traitée par des algorithmes d’analyse en vue de rehausser sa qualité facilitant ainsi son interprétation. Les systèmes existants de diagnostic des mammogrammes assisté par ordinateur permettent une deuxième lecture très utile, surtout lors des campagnes de dépistage systématique où on peut avoir jusqu’à 100 cas par heure. Ces systèmes permettent une amélioration des performances du diagnostic de l’ordre de 15% en faisant un criblage ou « second read ».
Malgré les évolutions des nouvelles technologies pour améliorer la qualité des images mammographiques numériques, l’interprétation et l’analyse de ces images restent une tâche difficile même pour un radiologue. Ceci est dû à la grande variabilité dans la forme des masses mammaires malignes et bénignes, et au fait que les pathologies sont souvent cachées dans les tissus mammaires. Depuis quelques années, de nombreuses équipes de recherche tentent de développer un système d’analyse et d’interprétation automatique des images mammographiques numériques. Ces travaux de recherche s’orientent, en fonction de la problématique à traiter, en deux grands axes: (1) la détection automatique qui vise à identifier les anomalies et à classifier les régions d’un mammogramme en régions d’intérêts (suspectes) et (2) le diagnostic assisté par ordinateur qui vise à caractériser et à classifier l’anomalie détectée en bénigne ou maligne. Ce travail de thèse s’inscrit dans le premier volet d’analyse des mammogrammes.
Notre objectif principal est la détection des microcalcifications par l’analyse et la classification des différents tissus constituant l’image mammographique. La nouveauté par rapport aux travaux ultérieurs réside dans l’application des algorithmes d’analyse sur des images codées plutôt que sur les images initiales. En se basant sur une technique de codage des informations texturelles contenues dans les tissus d’un mammogramme, exprimées en niveaux de gris, il s’agit de trouver un codage qui permet d’obtenir des images codées plus riches en information que les images d’origine et ce dans le but de rendre la détection des microcalcifications plus efficace.
Pour atteindre cet objectif, notre approche consiste à
• Segmenter l’image initiale pour (1) localiser le contour extérieur du sein afin d’éliminer le fond de l’image mammographique ; (2) localiser le muscle pectoral et l’éliminer de l’image afin de pouvoir limiter le taux de détection des faux positifs;
INTRODUCTION
XV
• Segmenter pour délimiter les zones de forte densité exprimées en niveaux de gris qui constituent les zones d’intérêts ;
• Coder les zones d’intérêts pour exprimer chaque niveau de gris par un code permettant de mieux exploiter l’information texturelle de l’image initiale et offrant ainsi une analyse plus fine ;
• Analyser les textures des zones d’intérêts pour classifier et caractériser les microcalcifications.
Ce mémoire de thèse décrit ces différentes étapes et illustre les résultats obtenus sur la base d’analyse des mammogrammes provenant de la base de données MIAS1 contenant 322 mammogrammes de 207 sujets normaux et 115 cas pathologiques (6 types de pathologies bien établies). Ce mémoire est structuré en six chapitres.
Nous commençons par une présentation générale des caractéristiques du cancer du sein sur une image mammographique ainsi que le progrès introduit par la mammographie numérique par rapport à la mammographie traditionnelle. Le deuxième chapitre résume les différentes méthodes proposées dans la littérature pour l’analyse et la segmentation des images à niveaux de gris. Une analyse comparative de ces méthodes nous a orienté vers le choix des méthodes de segmentation adéquates pour notre application à savoir les contours actifs basés région et la méthode de segmentation basée sur les maxima de niveaux de gris.
Le troisième chapitre est consacré à la présentation des méthodes d’analyse de textures. Nous justifions le choix des méthodes statistiques retenues et leur adaptation pour les appliquer sur les images mammographiques.
Nous abordons au quatrième chapitre la méthode proposée incluant les techniques développées pour le codage et la classification des mammogrammes. Nous présentons d’abord les résultats du codage obtenus que nous comparons à ceux obtenus par les techniques de codage classique (codage d’extrémalité local (rank coding), codage simple sur 16 niveaux de gris).
Le cinquième chapitre décrit en détails les méthodes développées pour la segmentation des régions d’intérêt sur un mammogramme (profil extérieur du sein, le contour du muscle pectoral et les zones de forte densité) et présente les résultats trouvés.
1
INTRODUCTION
XVI
Dans le dernier chapitre, nous présentons les techniques d’extraction des attributs de texture pour alimenter le classifieur retenu basé sur les SVM et nous illustrons les résultats obtenus sur deux types de pathologies, les microcalcifications et les masses circoncrites
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
1
==========================================================
Chapitre I : Mammographie numérique et diagnostic
assisté par ordinateur
1.1- Mammographie et constitution des images mammographiques
1.1.1- Anatomie du sein
Le mot sein vient du latin sinus [I.1] qui veut dire courbure, sinuosité ou pli qui désigne notamment un pli de la toge recouvrant la poitrine. On désignait le sein par « mamma » et petit sein par mamilla, alors que mammicula désignait petite mamelle. D’ailleurs c’est de là d'où vient le mot « mammifère » dont la caractéristique première est d'être dotée de mamelles ou de seins pour l'être humain.
Le sein est un organe visible et palpable, innervé et richement vascularisé dont la fonction première est la production de lait maternel [I.2]. Situés à la face antérieure du thorax, les seins présentent une base mammaire s’étendant de la deuxième côte jusqu’à la sixième et du bord latéral du sternum jusqu’à la ligne axillaire antérieure. En arrière, le sein repose non pas sur une surface plane mais sur la cage thoracique qui est nettement convexe. La face profonde de la glande repose sur le muscle grand pectoral.
Sur le plan superficiel, le sein est recouvert de peau s’étendant sans limite nette jusqu’à la région mamelonaire. En avant et latéralement, le tissu glandulaire est étroitement uni au derme par des ligaments (ligaments de Cooper) qui permettent de suspendre la glande au
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
2
plan cutané et constituent son principal moyen de fixité. La plaque aréolomamelonnaire située au sommet du cône mammaire constitue également la clé de voûte en termes de stabilité et de fixation cutanée. Le mamelon est implanté sensiblement au centre de l’aréole et présente à son extrémité les orifices de 15 à 20 canaux galactophores terminaux (conduits lactifères), distinctement séparés les uns des autres. L’aréole est pourvue de fibres musculaires lisses qui contrôlent la fonction excrétrice du sein au moment de la lactation [I.3].
Sur le plan interne, le volume mammaire n’est pas constitué uniquement de tissu glandulaire (canalaire et lobulaire) mais aussi de tissu adipeux et conjonctif. La proportion entre ces trois éléments varie considérablement d’une femme à l’autre mais aussi chez une même femme en fonction de son âge, de son statut hormonal et de ses variations pondérales. Ceci explique les grandes variations de densité et de consistance de la glande mammaire.
Le sein comporte cependant des macrostructures qui peuvent être identifiées avec une technique mammographique adéquate. Certaines d’entre elles ne deviennent cependant visibles que lorsqu’elles augmentent de taille ou s’il y a une modification de leur absorption par les rayons X (contenu graisseux ou calcifications). La glande mammaire est composée de 15 à 10 lobes drainés par des canaux mammaires qui vont jusqu’au mamelon [I.2]. Chaque lobe est composé de la convergence de canaux qui proviennent des unités ductolobulaires terminales qui sont entourées d’un tissu conjonctif peu dense qui constitue les lobes [I.4]. Ces unités ductolobulaires terminales ne sont pas normalement visibles, mais peuvent apparaître lorsque leur taille augmente ou si elles contiennent des calcifications. La proportion de tissus “canalaires” et lobulaires est très variable.
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
3 1.1.2- Le cancer du sein
Le mot cancer du sein est un terme générique pour désigner la gamme entière des maladies malignes du sein. Les cellules malignes se multiplient sans contrôle jusqu'à créer une tumeur qui s'attaque aux tissus sains avoisinants. Cette tumeur peut propager des cellules cancéreuses dans tout l'organisme : on dit alors qu'elle devient métastatique [I.5]. Dans le monde entier le cancer du sein est le cancer le plus fréquent mais aussi la première cause de décès par cancer chez la femme dans le monde [I.6] [I.7]. En 2005, en France, son incidence est de 101,5 pour 100.000 personnes, correspondant à 49.8 nouveaux cas, soit 37 % des cancers chez la femme et 11.201 décès soit un taux de mortalité de 17,7 pour 100.000 personnes [I.2]. De 1980 à 2005, l’incidence du cancer du sein a augmenté de 74%, soit une hausse annuelle constante de 2,4%, alors que depuis 1998, le taux de mortalité diminue de 1,3% par an. Le vieillissement de la population, les nouveaux modes de vie (obésité et alcool plus courants chez la femme depuis quelques décennies), ainsi que la mise en place du dépistage du cancer du sein contribuent à l’augmentation de cette incidence, alors que ce même dépistage, combiné à l’amélioration des stratégies thérapeutiques permettent la diminution de la mortalité.
Au Maroc, le cancer du sein est en augmentation continue ; il constitue un véritable problème de santé publique et considéré comme le cancer le plus fréquent chez les femmes (36,1% pour le cancer du sein) [I.8]. Selon les estimations du Centre International de Recherche sur le Cancer, l’incidence actuelle se situerait entre 35 000 et 50 000 nouveaux cas par an [I.9] (absence de chiffres exacts). Ajoutant à ce problème, le retard dans le diagnostic qui cause un nombre important de décès. Pour cela plusieurs mesures ont été prises par l’état pour la détection précoce de cette maladie. Elles comprennent trois activités :
• Le dépistage des cancers du sein au niveau des Etablissements de Soins de Santé de
Base (ESSB);
• Le diagnostic précoce des cancers du sein au niveau des Centres de Référence de Santé Reproductive (CR SR);
• La prise en charge thérapeutique du cancer du sein au niveau des Centres
d’Oncologie.
1.1.3- Les facteurs de risque du cancer du sein
Les facteurs de risque du cancer du sein sont nombreux et très variés [I.10][I.11]. Ils sont classés en fonction de leur importance, on trouve : les risques principaux, les risques importants et les risques d’importance mineure ou dont l’importance reste à déterminer.
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
4
Parmi les risques principaux du cancer du sein, on trouve le genre puisque le cancer du sein concerne 99 % des femmes contre 1 % des hommes [I.12][I.13]. Le facteur âge vient ensuite et représente un facteur principal pour tout type de cancer [I.14][I.15]. Le cancer du sein affecte très rarement les femmes de moins de 30 ans, mais plus une femme avance en âge, plus le risque de développer un cancer du sein augmente [I.10][I.11]. En France, presque 10 % des femmes développent un cancer du sein : moins de 10 % surviennent avant 40 ans, 25 % avant 50 ans et près de la moitié avant 65 ans. L’hérédité joue aussi un rôle principal : 5 à 10 % des cancers du sein sont dus à une prédisposition génétique [I.16][I.17].
Pour les risques importants, on peut citer les maladies histologiques du sein ainsi que les antécédents de cancer, quels qu’ils soient, peuvent augmenter le risque de cancer du sein [I.11][I.18]. L’exposition du tissu mammaire aux radiations ionisantes avant l’âge de 40 ans est susceptible de provoquer un cancer du sein dans les années ultérieures [I.11].
L’origine géographique influence aussi le risque de cancer du sein. Ce risque augmente de plus de 4 fois si la patiente est née en Amérique du Nord ou en Europe du Nord comparé à une femme née en Asie ou en Afrique [I.11].
Beaucoup d’autres facteurs de risques liés au mode de vie tels que la consommation régulière d’alcool [I.19][I.20], le tabagisme [I.21][I.22], l’obésité [I.32][I.24], une alimentation riche en graisse [I.25][I.26] ou encore la puberté précoce [I.27], la ménopause tardive, les traitements hormonaux substitutifs de la ménopause [I.28], la contraception orale [I.29] et bien d’autres peuvent présenter des risques modérés du cancer du sein.
1.1.4- Les types de cancer du sein
1.1.4.1- Les masses
Ce sont des lésions retrouvées en trois dimensions. Etant plus denses que le tissu mammaire adjacent, elles apparaissent blanches sur les mammogrammes. La taille ne prédit pas le caractère malin, sauf si les clichés successifs montrent une augmentation régulière de la taille. On distingue traditionnellement cinq formes différentes de masses: ronde, ovale, lobulaire, irrégulière ou une distorsion architecturale. Cette dernière forme inclut des rayons convergeant vers un point avec une rétraction focale. La figure1.2 présente un ensemble de lésions.
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
5
Masse ronde Masse ovale Masse lobulaire Masse irrégulière Distorsion architecturale
Figure 1.2: Les types de masses
Les bords de la masse sont très importants à étudier lors de l'analyse sémiologique qui nécessite parfois l'utilisation de la loupe. On décrit 5 catégories de bords de type: circonscrits, effacés, micro-lobulés, mal définis et avec des spicules (voir figure1.3). Les bords effacés correspondent à une superposition de tissus adjacents. Les bords mal définis ou les spicules correspondent à une invasion dans le tissu sain.
Bords circonscrits Bords effacés Bords micro-lobulés
Bords
mal définis Bords spiculés
Figure 1.3 : Les différents types de bords de masses 1.1.4.2- Les microcalcifications
Les calcifications sont des indicateurs importants dans l’interprétation des mammogrammes. En général, ce sont des dépôts de sels de calcium ; elles apparaissent sous forme de points blancs et brillants sur les mammogrammes [I.5]. Elles peuvent être produites à partir de la sécrétion de cellules ou à partir des débris cellulaires nécrotiques. Elles peuvent être intramammaires, dans et autour des conduits, dans les lobules, en
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
6
structures vasculaires, en tissu conjonctif ou graisse interlobulaire comme elles peuvent être trouvées dans la peau.
En fonction de leur taille, on peut classer les calcifications en micro ou macro- calcifications. Ces dernières sont souvent bénignes (figure1.4) alors que les microcalcifications constituent un indicateur de malignité (figure1.5). Le diagnostic dépend de leur position dans le sein, de leur arrangement géométrique (linéaire, en forme d'agrégats, etc.) et du nombre de microcalcifications dans un amas, et aussi de la comparaison avec une mammographie antérieure. Il se base sur les analyses suivantes :
- Analyse de forme [I.5]: les calcifications de forme régulière, rondes ou ovales sont
des tumeurs bénignes alors que les calcifications irrégulières de formes variées sont souvent associées avec une pathologie maligne.
- Analyse de taille : Les calcifications de moins de 0.5 mm sont souvent associées à
des cancers, celles de plus de 2 mm sont des lésions bénignes.
- Analyse du nombre : les petites calcifications nombreuses sont suspectes ; un
nombre au-dessus de 4 microcalcifications impose une interprétation plus prudente. - Analyse de l’orientation : les amas en forme triangulaire ou losangique orientée
vers le mamelon indique une nature maligne.
- Analyse de la morphologie : cette analyse permet le plus souvent de séparer
microcalcifications bénignes et malignes. Les calcifications arrondies ou ovales, uniformes dans leur taille et leur forme, sont probablement bénignes. A l'inverse, celles qui sont irrégulières dans leur taille, ressemblant par leur hétérogénéité à des 'débris de verre', sont probablement malignes.
a) Punctuate Calcifications b) Rod-Shaped Calcifications c) Vascular Calcifications
d) Round Calcifications e) Coarse or Popcorn-like Calcifications f) Spherical or Lucent-Centered Calcifications g) Rim or Egg-shell Calcifications h) Milk of Calcium Calcifications
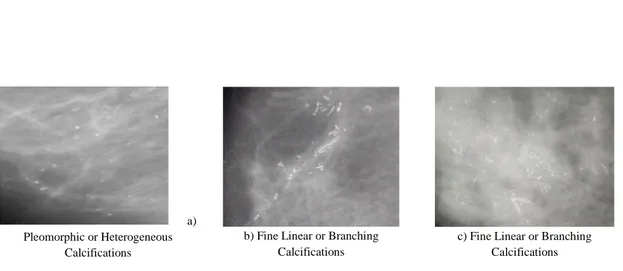
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR 7 a) Pleomorphic or Heterogeneous Calcifications b) Fine Linear or Branching
Calcifications
c) Fine Linear or Branching
Calcifications
Figure 1.5 : Exemple de calcifications malignes
1.1.5-Mammographie
En 1966, le professeur Jean-Marie Gros à Strasbourg- France, avec l'aide des ingénieurs de la Compagnie Générale de Radiologie de la section de cristallographie, a mis au point le premier système d'imagerie RX du sein comme outil d’examen radiologique du sein. L’objectif de cet examen, appelé mammographie, est la détection des pathologies du sein grâce à un appareil dédié appelé le mammographe. Cet appareillage utilise les rayons X pour produire des images de haute résolution du sein. Les différences d'absorption des rayons X par le tissu mammaire permettent de former une image qui révèle l'architecture du sein. L'utilité de cet examen se trouve surtout dans la détection de la désorganisation de l'architecture du sein qui peut révéler la présence d'un cancer. Malgré l’évolution des technologies, la mammographie reste l'outil principal de détection des pathologies du sein pour plusieurs raisons [I.5]:
- le coût moyen d'un examen mammographique est faible comparé à d'autres
techniques d'imagerie. De plus l'appareillage est mobile et peu encombrant;
- l'examen n'est pas traumatisant.
- la résolution spatiale d'une radiographie est de l'ordre de quelques dizaines de microns, ce qui permet de visualiser les microcalcifications, contrairement aux autres techniques d'imagerie.
1.1.5.1-Formation de l’image mammographique
Le sein a une structure tridimensionnelle ; l’image mammographique est le résultat de la superposition des différents éléments anatomiques [I.30] qui ont des coefficients d'atténuation aux rayons X presque identiques. Les densités des structures mammographiques sont basses et il y a un recouvrement entre les densités d’éléments normaux et des tissus pathologiques. La structure fibreuse du sein est plus clairement
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
8
identifiable quand la quantité de tissu graisseux est plus abondante. Dans le cas contraire, l’examen mammographique devient plus difficile puisque on sera amené à distinguer des densités tissulaires proches ; ce qui correspond à des effets de sommation d’éléments fibreux normaux d’une distorsion architecturale ou d’une stroma-réaction d’origine tumorale. Le sein comporte cependant des macrostructures qui peuvent être identifiées avec une technique mammographique adéquate. Certaines d’entre elles ne deviennent cependant visibles que lorsqu’elles augmentent de taille ou s’il y a une modification de leur absorption par les rayons X.
La réalisation d'une mammographie passe par plusieurs étapes [I.31]. D’abord les rayons X sont générés par un tube RX. Ce faisceau est filtré puis collimaté pour éviter les fuites de radiations hors de la zone de l'examen. Il traverse ensuite le sein sous compression, pour atteindre le récepteur d’image placé immédiatement sous le sein. Une grille anti-diffusante est le plus souvent interposée entre le sein et le récepteur pour atténuer les rayons X diffusés par le sein qui peuvent causer une diminution de la lisibilité de l'image en introduisant un flou indésirable. Deux vues par sein sont nécessaires et en général suffisantes pour couvrir l'ensemble des tissus dans et autour du sein : une vue de face, appelée incidence cranio-caudale (CC) et une vue en oblique appelée incidence médio-latérale oblique (MLO). La figure 1.8 présente ces deux prises de vue.
Figure 1.6 : Méthode utilisée pour la prise d’un mammogramme
Le mammographe possède un dispositif de compression du sein. Cette compression participe tout autant au processus permettant d'obtenir des images de haute résolution tout en diminuant les doses de rayonnements utilisées.
L’agrandissement géométrique permet d’augmenter le contraste de détail, ce qui permettra une meilleure visualisation des détails fins de l’architecture ainsi que des microcalcifications. Ce contraste augmente quand on utilise un kilovoltage bas et lorsque l’on utilise une grille, mais le temps d’exposition est également augmenté ce qui expose à un risque de flou cinétique. De plus la dose d’irradiation à la glande augmente [I.32]. Le récepteur d’image a pour rôle de traduire la modulation de l’intensité du faisceau qui
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
9
résulte de l’absorption des rayons X dans le sein. En principe, les différentes densités doivent être présentées dans la partie linéaire de la courbe sensitométrique des films. Pour lire les films, on les met sur un négatoscope. Selon la puissance et l’éclairement de celui-ci, la perception que le lecteur aura de la densité optique des films sera très variable.
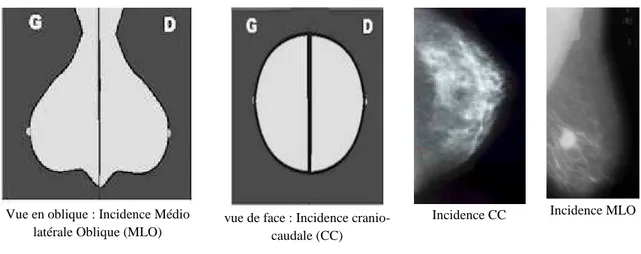
Vue en oblique : Incidence Médio latérale Oblique (MLO)
vue de face : Incidence cranio-caudale (CC)
Incidence CC Incidence MLO
Figure 1.7 : Incidence cranio-caudale et l’incidence Médio latérale oblique pour l’acquisition d’un mammogramme
1.1.5.2- Limitations de la mammographie
Bien que la mammographie reste l’outil le plus performant pour la détection des lésions du sein, elle n'est pas toujours facile de déceler la présence d'une tumeur. Chez les femmes jeunes, le parenchyme mammaire peut être dense et masquer la présence des lésions, pour cela l'examen sénologique est complété par une échographie des seins. L'échographie est beaucoup plus performante que la mammographie dans la détection des lésions lorsque le parenchyme mammaire est abondant. En plus la mammographie ne permet pas de dire si une lésion est liquidienne (kyste), ou solide. Cette distinction ne peut se faire qu'à l'échographie, raison pour laquelle une mammographie peut être suivie d'une échographie.
Par conséquent, la mammographie n'est pas le reflet d'une visualisation directe des pathologies du sein. L'interprétation du radiologue ne correspond qu'à une hypothèse radiologique et doit être corroborée avec l'examen microscopique de la lésion mammaire.
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
10
1.2- Mammographie numérique et diagnostic assisté par ordinateur
1.2.1- Mammographie numérique
La première solution utilisée pour avoir un équivalent numérique d'un film radiographique est effectuée par une caméra CCD (Charge Coupled Device) ou un microdensitomètre (scanner) [I.33]. Dans le premier cas, le signal vidéo acquis par la caméra est numérisé. Dans le deuxième cas, un faisceau laser de haute densité mesure la densité optique de chaque point radiographique [I.34]. Cette nouvelle technologie ouvre la voie aux traitements d'image numérique avec une meilleure résolution en contraste à dose équivalente.
En 1999, Medical Sytems (GE), introduit le premier appareil de mammographie numérique [I.31], celui-ci remplaçant le traditionnel film RX par une image produite à l'aide d'un large capteur numérique.
Le plus grand avantage de la mammographie numérique par rapport à la mammographie traditionnelle et le temps requis pour l’obtention de l’image mammographique. Ceci évitera le temps mis pour développer le film, de s’assurer si l'exposition du cliché est correcte ou si le sein est parfaitement positionné. En effet, les images numériques sont affichées en moins de 10 secondes avec une résolution de 2000x2500 pixels, spécialement choisis pour l’imagerie médicale, sur un moniteur 1280x1024 de haute luminosité [I.31].
La mammographie numérique rend l’image numérique transportable ; les clichés de l'examen d’une patiente peuvent être envoyés, via réseau pour un diagnostic à distance par d’autres spécialistes. En plus, elle offre également la possibilité d’organiser une chaîne complète de gestion de l'information des données médicales, données démographiques du patient, informations de gestion automatique des procédures et facturation. Quant à l'archivage des images, les grands locaux réservés à l’archivage des films dans les sous-sols des hôpitaux sont remplacés par des systèmes de stockage d’images numériques (disques durs).
L'autre grande nouveauté par rapport au film est la possibilité d’accéder aux données brutes affichées sur l’image numérique. Pour un film, Une fois révélée chimiquement, il sera impossible de modifier les contrastes locaux autour d'une zone d'intérêt par exemple. Il est possible de numériser le film, mais l'information resterait limitée à la dynamique de la courbe de son contraste. En numérique, on peut accéder directement à l'image brute, s'assurer de son exposition correcte par calcul dans des zones d'intérêts, et bénéficier pleinement de la grande dynamique des composantes d’acquisition.
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
11
Lors des campagnes de dépistage systématique, un médecin peut revoir jusqu'à 100 cas par heure, ce qui entraine fatigue, manque de concentration pouvant induire des erreurs d’interprétation. Alors que, avec l’image numérique et les outils de traitements d'image classiques à base de processeurs temps réel, l'interprétation de l'image devient plus facile. Néanmoins, l’introduction d’autres traitements appliqués à l’image numérique peuvent rehausser davantage les densités et les contours près de la bordure du sein et améliorer ainsi la détection des tumeurs souvent difficilement décelables.
Il y a lieu de signaler que les avantages de la mammographie numérique reste limités par d’autres facteurs. L’un des facteurs est lié aux pratiques habituelles des médecins, le besoin de formation aux nouvelles technologies de diagnostic assisté par ordinateur ; ce qui peut engendrer une résistance compréhensible de la part de certains radiologues. Les contraintes économiques (coût de l’appareil, coût de l’examen) constituent un autre facteur limitant l’utilisation de la mammographie numérique.
1.2.2- Qualité de l’image mammographique numérique
Pour avoir une image mammographique numérique, on utilise des filtres qui mesurent la densité optique des petites fenêtres des régions de l’image. La taille de la fenêtre détermine la résolution spatiale de l’image numérisée. La résolution est typiquement exprimée en unités de microns par pixel indiquant la taille de la région carrée de l’image que chaque pixel représente. La valeur exacte de pixel dépend du rang de la densité optique et du nombre de bits employés pour stocker le niveau de gris de chaque pixel. Le taux de détection des anomalies sur un mammogramme dépend fortement de la qualité de l’image qui est basée sur trois paramètres physiques [I.35]:
- la résolution : la capacité à discerner de fins détails
- le contraste : la capacité à discerner de faibles différences d'absorption de rayons X
par les tissus,
- le bruit qui est la fluctuation intrinsèque des niveaux de l'image noyant les faibles
détails peu contrastés. Cette fluctuation provient de la nature des rayons X, de la chaîne de formation de l'image, du bruit électronique du capteur ou grain du film, du rayonnement diffusé, etc.
Ces trois paramètres dépendent des différentes étapes de la formation de l’image à savoir : (1) l’exposition aux rayons X et la détection de ceux-ci, (2) le traitement de l’information acquise et la visualisation de celle-ci et (3) l’interprétation de l’information en vue de poser un diagnostic.
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
12
Le radiologue est confronté quotidiennement à l’évaluation de la qualité de l’image des différents clichés de patients qui lui sont présentés. Cette évaluation clinique est indispensable, cependant elle ne permet pas une appréciation complète de la qualité d’un système d’imagerie due essentiellement à l’appréciation du même observateur qui risque de changer au cours du temps et de la variabilité de l’appréciation d’un observateur à l’autre. Ce qui rend cette évaluation subjective, d’où la nécessité d’une méthode d’analyse objective de la qualité de l’image.
Une méthode d’évaluation objective de la qualité d’image s’appuie sur la mesure de paramètres physiques pertinents. On compte parmi ceux-ci l’efficacité quantique de détection, le rapport signal sur bruit ou encore le bruit quantique équivalent. Notons que ces paramètres quantifient la qualité intrinsèque du système d’imagerie, toutefois, il y a d’autres types de paramètres qui tiennent compte des étapes de la visualisation et de l’interprétation de l’information présente sur l’image. A titre indicatif, l’indice de qualité d’image correspond à la taille de la plus petite microcalcification détectable [I.36][I.37].
1.2.3- Diagnostic Assisté par Ordinateur (DAO) en mammographie numérique
Des études ont montré qu'une seconde lecture des mammogrammes assistée par ordinateur améliore la sensibilité de plus de 15% [I.38][I.39]. Elle constitue une approche standardisée [I.40][I.41] d’interprétation basée sur le criblage appelé en anglais ‘second reader’.
Depuis quelques années, de nombreuses équipes de recherche tentent de développer des systèmes d’analyse et d’interprétation automatique de mammogrammes. Ces techniques se regroupent en deux processus [I.42]: (1) la détection assistée par ordinateur et (2) le diagnostic assisté par ordinateur. La détection est la capacité d'identifier des anomalies potentielles en classifiant les régions d'un mammogramme en régions positives et d’autres négatives. Le diagnostic est la capacité de caractériser et de classifier une anomalie détectée en bénigne ou maligne.
Le principe de fonctionnement des systèmes existants est basé sur l’utilisation d’un logiciel de traitement d'image numérique ; ces images peuvent être des films radiographiques de la mammographie conventionnelle après numérisation, soit provenant d’un système d’acquisition des mammogrammes numériques. Les algorithmes utilisés sont basés sur une succession de techniques mathématiques qui commencent toujours par une phase de prétraitement [I.5] dont l’objectif est
- la détection de la peau, du muscle pectoral et les zones glandulaires et graisseuses ;
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
13
- la classification des éléments détectés, utilisant une méthode d’aide à la décision qui permet de marquer une indication sur une image imprimée ou sur un écran. Des systèmes de détection assistée par ordinateur CAD sont déjà commercialisés et leurs performances sont largement publiées dans la presse scientifique internationale. Parmi ces systèmes on trouve [I.43]:
- Image Checker M1000, de la société R2 technology développé à l'Université
de Chicago [I.44].
- Second Look, de la société CADX Medical Systems
- Mammex TR, de la société Scanis
- GP-CALMA (Grid Platform for Computer Assited Library for Mammography)
[I.45], développé principalement en Italie et dont l'originalité repose sur la conception d'une large base de données d'images (plus de 5000 correspondant à 1650 patientes)
1.3- Bases de données des mammogrammes numériques
Pour évaluer les performances d’une nouvelle approche d’analyse ou pour comparer de nouvelles méthodes, il est recommandé de les valider sur des bases de données de tests standards. En effet les chercheurs ont besoin de comparer leurs résultats sur les mêmes images. Malheureusement la plupart des bases de données d’images médicales réelles ne sont pas toujours accessibles au public. Actuellement les bases de mammogrammes numériques les plus utilisées par les chercheurs sont MIAS et DDSM.
1.3.1-Mammography Image Analysis Society (MIAS)
La base de données MIAS [I.46] est le fruit de travail d’une organisation de groupes de recherche britanniques qui s'intéressent à la mammographie. Les images mammographiques sont obtenues après numérisation de films X-ray soigneusement sélectionnés à partir du programme national de dépistage fait à l’échelle du Royaume-Uni. La numérisation est faite avec un scanner Joyce-Lobel microdensitomètre qui est un dispositif linéaire dans la gamme de densité optique est de 0 à 3,2 et qui a une résolution de 50x50 micromètre. Chaque pixel est codé sur 8 bits. Toutes les images sont découpées de telle sorte qu’elles sont toutes de taille 1024x1024. Tous les noms des mammogrammes ont la forme suivante : mdbXXXBS, où :
- XXX : représentent le nombre del'image, allant de 001 à 322 ;
- B estle côtédu sein, il prend la valeur «L» pour le sein gauche ou «R» pour le sein droit (Left or Right);
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
14
- S est la taille de l'image qui peut être «s» pour la petite image (1600x4320 pixels), «m» pour des images de taille moyenne (2048x4320 pixels), «l» pour les grandes images (2600x4320 pixels) et «x» pour les très grandes images (4000x5200pixels).
Chaque image est stockée au format brut: chaque numéro stocké dans le fichier correspond à la valeur du niveau de gris (de 0 à 255) du pixel correspondant dans l'image.
La base de données contient deux prises de vue du sein gauche et droit de 161 patients ; elle est constituée de 322 images classées en trois types :
• Type normal : il y a 208 cas;
• Type bénin : il y a 63 cas ;
• Type malin : il y a 51 cas
Pour chaque image, les radiologues ont décrit le type de la pathologie, sa localisation en donnant les coordonnées du centre de la pathologie, le diamètre d’une surface entourant la pathologie, sa taille, l'échelle, et d'autres informations utiles. Les tableaux 1.1 et 1.2 présentent les types de mammogrammes présents dans cette base de données. Sur ce tableau on peut trouver le nombre de mammogrammes contenants des calcifications, des masses, d'autres types d'anomalies, ainsi que le nombre de mammogrammes normaux, tous répartis selon le type du tissu mammaire (gras, glandulaire, ou dense).
Pathologies Gras Glandulaire Dense Total
Calcification 6 9 10 25
Masses 17 15 10 42
Autres 17 15 16 48
Normal 66 65 76 207
Total 106 104 112 322
Tableau 1.1: Nombre de mammogrammes dans la base de données MIAS
Masses Gras Glandulaire Dense Total
Circrumscribed 12 8 3 23
Spiculated 5 7 7 19
Total 17 15 10 42
Tableau 1.2: Nombre de mammogrammes contenant des masses dans la base de données MIAS
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
15
Un fichier joint à la base de données décrit en détails les images. Il est organisé en sept colonnes de la manière suivante :
1ère colonne : le numéro de référence de l’image dans la base de données MIAS
2ème colonne: caractérise le type des tissus du sein. Il y a trois types :
• F : Graisseux (Fatty)
• G : Glandules Graisseux (Fatty-glandular)
• D :Dense (Dense-glandular)
3ème colonne: Type de pathologie
• CALC : Calcification (Calcification)
• CIRC : Well-defined/circumscribed masses
• SPIC :Spiculated masses
• MISC :Other, ill-defined masses
• ARCH :Architectural distortion
• ASYM :Asymmetry
• NORM :Normal
4ème colonne: Sévérité de pathologie
• B Benin
• M Malin
5ème et 6ème colonne: les coordonnées (x,y) du centre de la pathologie
7ème colonne: Rayon approximatif (en Pixel) d'un cercle enfermant l'anomalie.
1.3.2- La base de données numérique de dépistage par mammographie (DDSM)
La base de données numérique de dépistage par mammographie (DDSM: Digital Database for Screening Mammography) [I.47] est une autre ressource de mammogrammes numériques mise à la disposition de la communauté de chercheurs en analyse des images mammographiques développée par Marathon de l’université de la Floride du Sud. Cette base contient 2620 dossiers de patientes classées en trois groupes : normaux, bénins et malins. Chaque cas contient quatre images, deux prises de vue pour chaque sein, une vue en MLO et une autre CC. En plus la base fournit un fichier contenant des informations sur les images comme le scanner, la résolution spatiale et des informations sur la patiente comme l’âge au moment de l'étude, la densité du sein, etc. Pour les images qui contiennent une ou plusieurs anomalies, une marque a été introduite par un radiologue expérimenté localisant les régions contenant les pathologies.
CHAPITRE I : MAMMOGRAPHIE NUMERIQUE ET DIAGNOSTIC ASSISTE PAR ORDINATEUR
16
Conclusion
Nous avons présenté dans ce chapitre l’anatomie du sein, comme une première étape aidant à une bonne compréhension de l’image mammographique. Nous avons ensuite passé à la présentation des pathologies qui peuvent atteindre les tissus du sein en donnant quelques caractéristiques comme la forme, la taille, la densité, les bords, etc. Pour visualiser une image Rayon X du sein, la mammographie reste l’outil le plus efficace et le plus utilisé par les radiologues. Nous avons ainsi présenté ses avantages et ses limitations en termes d’interprétation. Nous avons ensuite présenté la mammographie numérique et ses avantages par rapport à la mammographie conventionnelle et discuté les approches d’analyse utilisés par les systèmes de diagnostic assisté par ordinateur existants. Nous avons également décrit deux bases de données d’images mammographiques (MIAS et DDMS) utilisées comme bases de référence par les chercheurs. Nous avons choisi de travailler avec la base MIAS pour la simplicité d’exploitation par rapport à la base DDMS. Le chapitre suivant sera consacré à la présentation des différents travaux de recherche trouvés dans la littérature pour la segmentation et classification des images à niveau de gris