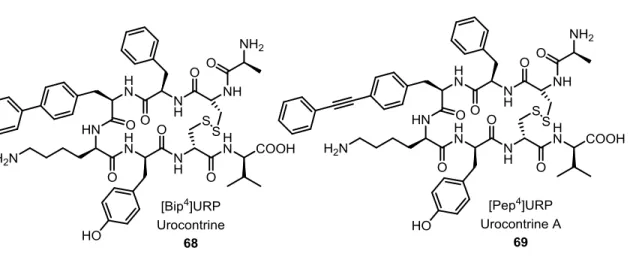
Synthèse en phase solide de pyrrolo[3,2-e][1,4]diazépin-2-ones modulateurs du système urotensinergétique
Texte intégral
Figure
Documents relatifs
Cette réaction a l’avantage d’insérer l’éthylène sur la 5-iodoisatine 193, avec un excellent rendement en présence d’une faible quantité de catalyseur (Schéma 72).
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des
Ainsi même si les valeurs d’enthalpies d’activation calculées sont plus faibles que celles obtenues pour la réaction entre le N-méthylimidazole et l’oxyde de
184 Les amines sont des nucléophiles qui ne peuvent pas être utilisés dans les mêmes conditions opératoires pour cette réaction et aucune réactivité n’a été observée
Une autre méthode classique de substitution d’un groupe hydroxyle activé in situ est la réaction de Mitsunobu (Schéma 2), consistant en l’utilisation conjuguée
Pour préparer nos réactifs en série azotée, nous avons travaillé avec la p-phénylènediamine et les phénylisocyanates selon les conditions réactionnelles décrites par Garofalo
En effet, nous avons découvert que les pyridylsilanes non fonctionnels sont inertes vis-à-vis des ions fluorures quelles que soient les conditions réactionnelles utilisées alors
Ces catalyseurs ont été utilisés pour accélérer deux réactions essentielles dans les procédés de synthèse totale développés dans cette thèse, à savoir la ligation SEA ainsi
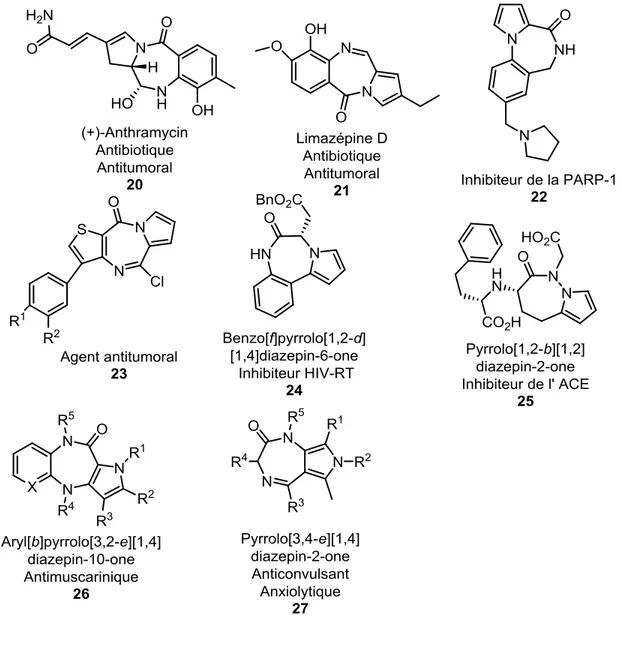
![Figure 1.6: Quelques exemples de pyrrolo[3,2-e][1,4]diazépin-2-ones obtenus par la réaction de Pictet-Spengler](https://thumb-eu.123doks.com/thumbv2/123doknet/12462229.337131/37.918.138.782.192.833/figure-exemples-pyrrolo-diazépin-obtenus-réaction-pictet-spengler.webp)