ASSEMBLAGE DES COMMUNAUTÉS D’HERBACÉES : UNE APPROCHE FONCTIONNELLE
par
Jessy LORANGER
thèse en cotutelle présentée
au Département de biologie en vue
de l’obtention du grade de docteur ès sciences (Ph.D.) FACULTÉ DES SCIENCES,UNIVERSITÉ DE SHERBROOKE
à l’École Doctorale SIBAGHE en vue de l’obtention du grade de docteur
UNIVERSITÉ DE MONTPELLIER
ii
Le 13 janvier 2016
le jury a accepté la thèse de Monsieur Jessy Loranger dans sa version finale.
Membres du jury
Éric Garnier Codirecteur de recherche
Centre d’Écologie Fonctionnelle et Évolutive (France)
Bill Shipley Codirecteur de recherche
Département de biologie, Université de Sherbrooke (Québec)
Richard Michalet
Évaluateur externe – Rapporteur
Institut National de la Recherche Agronomique, Université Bordeaux 1 (France)
Vincent Maire
Évaluateur externe – Rapporteur
Département des sciences de l’environnement, UQTR (Québec)
Mark Vellend
Évaluateur interne – Président-rapporteur
Département de biologie, Université de Sherbrooke (Québec)
Sabrina Gaba Évaluatrice externe Centre INRA de Dijon (France)
iii
Délivré par l’UNIVERSITÉ DE MONTPELLIER
Préparée au sein de l’école doctorale SIBAGHE
Et de l’unité de recherche UMR 5175 – CEFE
Spécialité : Écologie
Présentée par Jessy LORANGER
Soutenue le 10.12.2015 devant le jury composé de
M. Richard MICHALET, Professeur, Université Bordeaux 1 Rapporteur
M. Vincent MAIRE, Professeur, UQTR Rapporteur
M. Mark VELLEND, Professeur, Université de Sherbrooke Examinateur Mme Sabrina GABA, Chargée de recherche, CNRS - INRA Examinatrice M. Éric GARNIER, Directeur de recherche, CNRS - CEFE Directeur M. Bill SHIPLEY, Professeur, Université de Sherbrooke Directeur
L’ASSEMBLAGE DES COMMUNAUTÉS
D’HERBACÉES: UNE APPROCHE
iv
« Il semble que les modernes aient pris arbitrairement, dans le domaine de la connaissance scientifique, un certain nombre de portions qu’ils se sont acharnés à étudier à l’exclusion de tout le reste, et en faisant comme si ce reste était inexistant ; et, aux sciences particulières qu’ils ont ainsi cultivées, il est tout naturel, et non point étonnant ni admirable, qu’ils aient donné un développement beaucoup plus grand que n’avaient pu le faire des hommes qui n’y attachaient point la même importance […] et qui s’occupaient en tout cas de bien d’autres choses qui leur semblaient plus sérieuses. » « […] les apôtres de la tolérance sont très souvent, en fait, les plus intolérants des hommes. Il s’est produit, en effet, cette chose qui est d’une ironie singulière : ceux qui ont voulu renverser tous les dogmes ont créé à leur usage […] une caricature de dogme, qu’ils sont parvenus à imposer à la généralité du monde occidental ; ainsi se sont établies, sous prétexte d’« affranchissement de la pensée », les croyances les plus chimériques qu’on ait jamais vues en aucun temps […]. » « L’histoire vraie peut être dangereuse pour certains intérêts politiques ; et on est en droit de se demander si ce n’est pas pour cette raison que certaines méthodes […] sont imposées officiellement à l’exclusion de toutes les autres : consciemment ou non, on écarte a priori tout ce qui permettrait de voir clair en bien des choses, et c’est ainsi que se forme l’« opinion publique ». » « Sans doute, le pouvoir des mots s’est déjà exercé plus ou moins en d’autres temps que le nôtre ; mais ce dont on n’a pas d’exemple, c’est cette gigantesque hallucination collective par laquelle toute une partie de l’humanité en est arrivée à prendre les plus vaines chimères pour d’incontestables réalités […] » « […] celui dont l’intelligence est bornée à l’activité rationnelle trouve celle-ci admirable et sublime ; pour être pleinement à l’aise dans une sphère fermée, quelle qu’elle soit, il ne faut pas concevoir qu’il puisse y avoir quelque chose au-delà. »
René Guénon
v SOMMAIRE
Deux facteurs principaux, une fois combinés, permettent de comprendre l’assemblage des communautés, soient i) l’environnement (abiotique et biotique), qui agit comme un filtre sélectionnant les espèces les mieux adaptées aux conditions données, et ii) les traits fonctionnels, sur lesquels s’effectue ce filtrage environnemental puisqu’ils représentent les adaptations des espèces aux conditions données. Il est donc essentiel d’établir des relations fiables entre les conditions environnementales et la structure fonctionnelle des communautés afin de pouvoir identifier et comprendre les mécanismes régissant l’assemblage des communautés. Cependant, plusieurs facteurs tels que les interactions entre variables environnementales à différentes échelles spatiales (par exemple le climat et la fertilité des sols) peuvent complexifier la situation et c’est pourquoi, malgré une quantité grandissante d’études sur le sujet, les processus d’assemblage des communautés restent difficiles à définir et à généraliser. Cette thèse vise donc à i) mieux définir et quantifier les relations trait-environnement des systèmes d’herbacées au travers de différentes échelles spatiales et ii) déterminer l’influence de ces relations sur l’assemblage des communautés et le fonctionnement des écosystèmes. Pour réaliser ces objectifs, j’ai travaillé avec les données de programmes ayant collecté des données taxonomiques et fonctionnelles sur les communautés d’herbacées à travers la France (DivHerbe et DivGrass) et, à moindre mesure, l’Europe (VISTA). Ces bases de données couvrent donc de larges gradients climatiques régionaux ainsi que des gradients environnementaux plus locaux relatifs à la qualité des sols et aux perturbations.
J’ai d’abord testé l’importance de considérer à la fois des variables environnementales locales et régionales ainsi que leurs interactions pour déterminer la structure fonctionnelle
vi
et taxonomique des communautés. J’ai ensuite étudié comment l’importance relative des processus menant soit à la convergence ou à la divergence fonctionnelle peut changer le long d’une succession, puis comment ces deux types de processus influencent notre capacité à prédire l’assemblage des communautés à partir des traits fonctionnels. Finalement, j’ai présenté comment les résultats au niveau des communautés peuvent être utiles pour étudier le niveau des écosystèmes. Les résultats de cette thèse démontrent que les variables climatiques régionales interagissent fortement avec les variables environnementales locales pour influencer les processus locaux déterminant l’assemblage des communautés. Évaluer le contexte régional semble donc nécessaire afin d’éviter des interprétations erronées des patrons d’assemblage observés. Travaillant avec ces deux niveaux de variation environnementale, une dissociation important entre la variation taxonomique et fonctionnelle des communautés a été mise à jour, reflétant l’importance de considérer plusieurs facettes de biodiversité pour comprendre la dynamique des communautés. Les résultats ont aussi démontré que les processus d’assemblage menant à la convergence et à la divergence ont un impact très différent et prédictible sur les relations liant les traits et les abondances des espèces, c’est-à-dire notre capacité à prédire l’assemblage des communautés à partir des traits. Finalement, toutes ces notions, relatives aux relations trait-environnement et à l’assemblage des communautés basé sur les traits, ont été utilisées dans un contexte de biogéographie fonctionnelle. Il a été démontré qu’il était possible de construire des cartes de valeurs de traits fonctionnels dans les prairies permanentes à l’échelle de la France, à partir de variables environnementales. Certaines propriétés écosystémiques ont ensuite pu être prédites à partir de ces cartes. Ces travaux ont donc permis d’illustrer les défis à surmonter pour utiliser nos connaissances de l’écologie fonctionnelle en vue d’une conservation et d’une exploitation viables de nos écosystèmes.
Mots-clés : traits fonctionnels; gradients environnementaux; structure des communautés; écologie prédictive; fonctionnement des écosystèmes; modélisation; biogéographie fonctionnelle
vii
A FUNCTIONAL APPROACH TO HERBACEOUS COMMUNITY ASSEMBLY ABSTRACT
There are two main factors which, combined together, allow understanding community assembly : i) the environment (both abiotic and biotic), which acts as a filter selecting species according to how well-adapted they are to given conditions, and ii) functional traits, on which this environmental filtering occurs since they represent species adaptations to particular conditions. It is thus essential to establish reliable relationships between environmental conditions and the functional structure of communities in order to identify and understand the mechanisms driving community assembly. However, several factors such as cross-scale interactions between environmental variables (e.g. between climate and soil fertility) complicate the situation. This is why, despite a growing body of studies on the subject, processes of community assembly are still poorly understood and are difficult to generalize. The purpose of this thesis is to i) better define and quantify the trait-environment relationships in herbaceous systems across different spatial scales and ii) determine the influence of those relationships on community assembly and on ecosystem functioning. To realize these objectives, I worked with data from programs which assembled taxonomic and functional data on herbaceous communities across France (DivHerbe and DivGrass) and, to a lesser extent, Europe (VISTA). These databases thus cover large regional climatic gradients, as well as more local environmental gradients related to soil quality and disturbances.
I first tested the importance of simultaneously considering local and regional environmental variables as well as their interactions to determine the taxonomic and functional structure of
viii
communities. Then, I studied how the relative importance of processes leading to either functional convergence or divergence can change along a successional gradient, and how these two types of processes influence our ability to predict community assembly from functional traits. Finally, I presented how the results at the community-level can be used to study the ecosystem-level. The results of this thesis demonstrate that regional climatic variables strongly interact with local environmental variables in driving the local processes responsible for community assembly. Assessing the regional context is thus necessary in order to avoid erroneous interpretations of observed assembly patterns. Working with those two levels of environmental variation, important discrepancies were found between taxonomic and functional variations across communities, reflecting the importance of considering several aspects of biodiversity in order to understand community dynamics. The results also demonstrated that the assembly processes leading to functional convergence and divergence have a very different and predictable impact on the relationships between traits and species relative abundances, i.e. on our ability to predict community assembly from traits. Finally, these notions related to trait-environment relationships and to trait-based community assembly were used in a functional biogeography framework: It was possible to build maps of functional traits values in permanent grasslands across France using environmental variables. These maps then allowed predicting particular ecosystem properties. Thus, this work allowed illustrating some challenges that we are facing in using our knowledge in functional ecology to build sustainable conservation and exploitation plans for our ecosystems.
Key-words: functional traits; environmental gradients; community structure; predictive ecology; ecosystem functioning; modelling; functional biogeography
ix
REMERCIEMENTS
Je tiens à remercier tout d’abord mes deux codirecteurs, Éric Garnier et Bill Shipley, pour la confiance sans faille qu’ils m’ont donnée tout au long de la thèse et pour leur flexibilité exceptionnelle qui m’a permis de faire coïncider ma vie professionnelle et personnelle. Au-delà de leurs contributions scientifiques – qui, il va sans dire, étaient très différentes, mais tout aussi indispensables l’une que l’autre – ils m’ont tous deux montré une vision du travail en recherche qui m’a inspiré et donné l’envie de finir cette thèse. Je tiens aussi à remercier Cyrille Violle pour ces idées toujours excellentes qui arrivaient au bon moment, pour son soutien moral plus d’une fois mis à l’épreuve et aussi, un peu, pour m’avoir aidé à bien comprendre l’importance du végétarisme. Franchement, sans lui la qualité de cette thèse et de mon expérience aurait été bien amoindrie.
Un grand merci à toute l’équipe d’ECOPAR pour l’accueil chaleureux auquel j’ai eu droit. Malgré mes courtes visites et mes absences nombreuses, j’ai toujours eu l’impression d’y être plus que bienvenu, de faire partie de la « famille » ECOPAR. Merci à Ben Borgy, sans qui je serais vraisemblablement toujours en train de travailler sur mes scripts R. Merci à François Munoz pour ses contributions à mes travaux, pour le brin d’humour qu’il ne manquait jamais d’apporter et aussi pour m’avoir toujours retrouvé lorsqu’il me perdait au gré de ses explications. Je remercie également tous les contributeurs – trop nombreux pour être nommé un à un – des programmes DivHerbe, VISTA et DivGrass. Leur contribution généreuse, en données et en idées, aura rendu cette thèse possible. Merci au CRSNG, au FQRNT, au GDRI et à Bill pour avoir financé cette thèse.
Je tiens à remercier ma famille proche – aussi très nombreux – pour leur soutien moral et pour m’avoir fourni ce qu’il me faut, en défi comme en aide, afin de construire la vie dont j’ai envie. Un merci tout particulier à Pauline, Roman et Xavier qui, de par nos longues (et trop peu nombreuses) conversations sur la vie, m’ont aidé à réaliser que les seules choses qui valent vraiment la peine qu’on s’y attarde étaient l’amour et le bonheur. Merci à Paméla pour les sorties ornithos et pour s’être pris les « coups » de la cotutelle avant moi et m’y avoir préparé. Zuletzt möchte ich mich bei meiner wunderbaren Frau bedanken, für die Schönheit und die Glückseligkeit die sie in jeden Aspekt unserem Leben mitbringt. Sie war meine stärkste Unterstützung während der Doktorarbeit und hat mir immer geholfen, der beste Mann zu werden, der ich sein kann. Ich könnte mir niemanden vorstellen, mit wem ich mehr Lust hätte, mein ganzes Leben aufzubauen und zu genießen, und ich habe keinen Zweifel daran, dass wir zusammen die wundervollsten und fabelhaftesten Erfahrungen erleben werden.
x
TABLE DES MATIÈRES
SOMMAIRE………... v
ABSTRACT……….………... vii
REMERCIEMENTS………. ix
TABLE DES MATIÈRES……….... x
LISTE DES ABRÉVIATIONS ET ACRONYMES………... xix
LISTE DES TABLEAUX………. xxiii
LISTE DES FIGURES………....…………....……….... xxvii
CHAPITRE I – INTRODUCTION GÉNÉRALE……….. 1
1.1 – Histoire et développement de l’écologie des communautés……….... 1
1.2 – De l’identité taxonomique à l’identité fonctionnelle……… 7
1.3 – Importance des gradients environnementaux et leurs relations avec la structure des communautés………... 11
1.3.1 – Gradients environnementaux et propriétés taxonomiques des communautés……….. 11
1.3.2 – Les réponses des traits à l’environnement………... 12
1.3.3 – Les effets des traits sur l’environnement……….. 18
1.4 – L’assemblage des communautés……… 19
1.4.1 – Réconcilier les théories d’assemblage neutre et déterministe…. 19 1.4.2 – Assemblage des communautés et l’importance du pool régional 23 1.4.3 – Filtres environnementaux et convergence fonctionnelle……….. 26
1.4.4 – Limite à la similarité et divergence fonctionnelle……… 29
1.4.5 – Convergence et divergence fonctionnelle: effets simultanés…... 31
xi
1.5 – Modélisation de l’assemblage des communautés: Distribution et
abondance des espèces………... 34
1.6 – Écosystèmes et biogéographie fonctionnelle……….... 37
1.7 – Projet de thèse………. 39
1.7.1 – Problématiques générales……… 39
1.7.2 – Objectifs généraux……… 41
1.7.3 – Bases de données utilisées: un aperçu………. 43
CHAPITRE II – OCCUPANCY AND OVERLAP IN TRAIT SPACE ALONG A SUCCESSIONAL GRADIENT IN MEDITERRANEAN OLD-FIELDS……..………. 49
2.1 – Présentation de l’article et contribution des auteurs………... 49
2.2 – Abstract………... 50
2.3 – Introduction………. 52
2.4 – Methods………... 56
2.4.1 – Study site……….. 56
2.4.2 – Sampling and functional traits………. 56
2.4.3 – Hypervolume calculations and null model………... 58
2.4.4 – Functional space variation along a successional gradient…….. 60
2.5 – Results………... 62
2.5.1 – Step 1: Displacement of functional space hypervolume (H1)….. 62
2.5.2 – Step 2: Size of the functional space (H2)………... 65
2.5.3 – Step 3: Overlap of the functional space (H3)………... 67
2.6 – Discussion……….... 70
2.6.1 – Displacement of the functional space………... 71
2.6.2 – Size of the functional space……….. 71
2.6.3 – Overlap of functional space between successional stages……... 76
2.7 – Conclusion………... 77
xii
2.9 – Literature cited………... 78
CHAPITRE III – RECASTING THE DYNAMIC EQUILIBRIUM MODEL THROUGH A FUNCTIONAL LENS: THE INTERPLAY OF TRAIT-BASED COMMUNITY ASSEMBLY AND CLIMATE……….. 84
3.1 – Présentation de l’article et contribution des auteurs………... 84
3.2 – Summary………... 85
3.3 – Introduction………. 87
3.4 – Material and Methods……… 92
3.4.1 – Study sites and experimental design………. 92
3.4.2 – Environmental data……….. 92
3.4.3 – Vegetation plots and functional traits: sampling strategies……. 94
3.4.4 – Data analysis……… 95
3.5 – Results……….. 99
3.5.1 – Species richness variation along regional and local environmental gradients……… 99
3.5.2 – Occupied functional space and species packing variation along regional and local environmental gradients……….. 100
3.5.3 – Relating species richness to occupied functional space and species packing……….. 103
3.6 – Discussion……… 103
3.6.1 – Species richness: A revisited dynamic equilibrium hypothesis… 104 3.6.2 – Occupied functional space variation along regional and local environmental gradients……… 106
3.6.3 – Species packing variation along environmental gradients…….. 107
3.6.4 – Relating species richness to occupied functional space and species packing……….. 108 3.7 – Acknowledgements………. 110
xiii
3.9 – References……… 110
3.10 – Supporting information………... 116
CHAPITRE IV – TRAIT-ABUNDANCE RELATIONSHIPS: A THEORETICAL EXPLORATION………... 117
4.1 – Présentation de l’article et contribution des auteurs……….. 117
4.2 – Abstract………... 118
4.3 – Introduction………. 119
4.4 – Methods………... 124
4.4.1 – Simulated communities………. 124
4.4.2 – Trait distribution under different assembly conditions………… 126
4.4.3 – Community Assembly by Trait Selection (CATS)………. 127
4.5 – Results……….. 129
4.5.1 – Moments of local trait distribution across processes…………... 129
4.5.2 – Regional species pool and dispersal limitation……… 129
4.5.3 – Filtering processes and moments of the trait distribution……... 131
4.6 – Discussion……….... 132
4.6.1 – Regional species pool and dispersal limitation……… 133
4.6.2 – Filtering processes and moments of the trait distribution……... 134
4.6.3 – Implications for the real world………. 136
4.7 – Acknowledgements………. 138
4.8 – Literature cited………... 139
4.9 – Supplemental material………... 143
CHAPITRE V – SENSITIVITY OF COMMUNITY-LEVEL TRAIT-ENVIRONMENT RELATIONSHIPS TO DATA REPRESENTATIVENESS: A TEST FOR FUNCTIONAL BIOGEOGRAPHY……….. 144
5.1 – Présentation de l’article et contribution des auteurs………... 144
xiv
5.3 – Introduction………. 147
5.4 – Materials and Methods………... 150
5.4.1 – Vegetation data……… 150
5.4.2 – Trait data……….. 151
5.4.3 – Climate data………. 152
5.4.4 – Sensitivity of species’ mean trait estimates to the number of individual values per species (NIV)………... 152
5.4.5 – Sensitivity of Community Weighted Means (CWM) to measurement intensity in trait databases (NIV) and data coverage (PCover)………. 153
5.4.6 – Sensitivity of the climate-CWMSLA relationship to measurement intensity in trait databases (NIV) and data coverage (PCover)………. 154
5.5 – Results……….. 154
5.5.1 – Sensitivity of species’ mean trait estimates to the number of individual values per species (NIV)………... 154
5.5.2 – Sensitivity of Community-Weighted Means (CWM) to measurement intensity in trait databases (NIV) and data coverage (PCover)………. 157
5.5.3 – Sensitivity of climate-CWMSLA relationships to measurement intensity in trait databases (NIV) and data coverage (PCover) 160 5.6 – Discussion……….... 161
5.6.1 – Sensitivity of trait means at species level………. 162
5.6.2 – Sensitivity of Community-Weighted Means to measurement intensity (NIV) and trait coverage (PCover)……….. 163
5.6.3 – Sensitivity of CWM-climate relationships to measurement intensity (NIV) and trait coverage (PCover)……….. 166
xv
5.8 – References……… 168
5.9 – Titles of annexes……….. 172
5.10 – Biosketch……… 173
CHAPITRE VI – VEGETATION ECOLOGY MEETS ECOSYSTEM SCIENCE: PERMANENT GRASSLANDS AS A FUNCTIONAL BIOGEOGRAPHY CASE STUDY 174 6.1 – Présentation de l’article et contribution des auteurs………... 174
6.2 – Abstract………... 175
6.3 – Introduction………. 176
6.4 – Permanent grasslands as a case study……….. 179
6.5 – Vegetation and plant trait databases in the era of ‘big data’: an ecoinformatics challenge……… 181
6.6 – A call for a better characterization of environmental gradients…… 186
6.7 – Scaling up from organismal traits to forage digestibility……… 188
6.8 – Conclusions and future directions………. 192
6.9 – Acknowledgements………. 196
6.10 – References……….. 196
CHAPITRE VII – DISCUSSION GÉNÉRALE ET CONCLUSION………….. 204
7.1 – Résultats généraux, signification et interrelations………... 204
7.2 – Variabilité intraspécifique des traits fonctionnels………... 209
7.3 – Estimer la niche écologique des espèces……… 214
7.4 – Conclusion………... 217
ANNEXE A – Towards a better understanding of multi-scale trait-environment relationships………... 219
A.1 – Présentation de l’article et contribution des auteurs……….. 219
A.2 – Introduction……… 221
A.3 – Methods………... 226
xvi
A.3.2 – Environmental data……….. 229
A.3.3 – Botanical relevés and functional traits……… 231
A.3.4 – Data analysis………... 232
A.4 – Results………. 238
A.4.1 – Selection of environmental variables………... 238
A.4.2 – Predicting functional variables………... 243
A.4.3 – Final models: a trait by trait presentation………... 244
A.5 – Discussion………... 250
A.5.1 – On the interpretation of the results...……….... 250
A.5.2 – Regional climatic controls…….……… 252
A.6 – Literature cited………... 253
Annex AA – Detailed methods of measurement for community-level environmental variables……… 261
AA.1 – Environmental variables for the estimation of plot level variables………. 261
AA.2 – Drought duration and intensity……… 262
AA.3 – Nutrient limitation indices……… 263
AA.4 – Disturbance indices……….. 265
Annex AB – Regression summary of the final models………. 268
ANNEXE B – List of species selected in this study (Chapter II) with their successional and functional details………. 281
ANNEXE C – Supporting results for the overlap analyses (Chapter II)………. 284
ANNEXE D – Mean functional trait variation during succession (Chapter II): non-weighted and abundance-weighted……… 287
ANNEXE E – Detailed methods of measurement and calculation for the growing season length, the nutrient index and the disturbance intensity (Chapter III)………. 292
xvii
E.2 – Nutrient limitation indices……….. 293
E.3 – Disturbance intensity……….. 295
ANNEXE F – Illustration of the range and distribution of values for the local
environmental variables (Chapter III)……….. 297 ANNEXE G – Partitioning of functional variation between site-, species-, and
individual-level (Chapter III)………. 300 ANNEXE H – Supplementary taxonomic and functional details on the sites
(Chapter III)………. 302
ANNEXE I – Disturbance frequency in the system (Chapter III): Variation and relative impacts on species richness, volume of occupied functional
space and species packing………... 304 ANNEXE J – Variation in the proportion of perennials and perennial grasses
along local and regional environmental gradients (Chapter III)………… 311 ANNEXE K – Summary of regression coefficients for significant patterns in
the mixed effect models (Chapter III)……….... 315 ANNEXE L – Three types of habitat filtering: An analogy with biological
evolution……… 316
ANNEXE M – Detection of the functional signatures of different assembly
processes (Chapter IV)……… 319
ANNEXE N – Details on the methods of Community Assembly by Trait
Selection (CATS)……….. 321
N.1 – CATS: The basics……… 321
N.2 – Including higher moments of the trait distribution as constraints in
CATS……… 324
ANNEXE O – Main fit results (Chapter IV) for neutral assembly, stabilizing and disruptive filtering processes, with a result summary for all
xviii
ANNEXE P – Fit results (Chapter IV) considering a uniform prior
(maximally uninformative) in CATS………. 333
P.1 – Results and Discussion……… 333
ANNEXE Q – Fit results (Chapter IV) under a directional filtering where the
optimal trait value is within the range of available values………... 338 ANNEXE R – Sources and number of vegetation plots in the DivGrass
database (Chapter V)……….. 340
ANNEXE S – Methodology (Chapter V) used in the estimation of the impact of the number of individual values (NIV) on the mean trait values of
species in TRY……….. 342
ANNEXE T – Methodology (Chapter V) used for the estimation of the impact of the number of individual trait values per species in TRY (NIV) and the coverage proportion for which mean trait value of species were available in TRY (PCover) on the estimation of Community Weighted
Mean (CWM)………... 344
ANNEXE U – Thresholds of minimum number of trait values (NIV) required per species to estimate species’ mean trait values with an error inferior
to 20%, 10% and 5% (Chapter V)………. 346 ANNEXE V – Impact of the number of individual values (NIV) on the
probability to discriminate pairs of species based on their mean trait
values (Chapter V)………... 350
ANNEXE W – Sources for vegetation relevés and traits used in DivGrass
(Chapter VI)………. 352
xix
LISTE DES ABRÉVIATIONS ET ACRONYMES
Abréviation/ Acronyme
Définition Page*
DAE Distribution d’abondance des espèces……….. p.4 CWM Community-weighted mean……….. p.21
CATS Community assembly by trait selection………. p.35
LAU Col du Lautaret……….. p.45 MER Métrola/Castro Verde……… p.45 SUT South Uist……….. p.45 MAG Les Magnils………... p.45 SLP Saint-Laurent de la Prée……… p.45
ERC Ercé……….... p.45
MAR Marcenat……….... p.45
THE Theix……….. p.45
FAG La Fage……….. p.45
xx
TDV Tour du Valat……… p.45 SAI Les Saisies………. p.45 BAT/BER Båttjønndale/Berghøgda……….... p.45 MNP Müritz National Park………. p.45 OHR Ohrazeni……….... p.45 BAL South-east Baltic Sea………. p.45
LAG Lagadas……….. p.45
KDE Karei Deshe………... p.45 L-H-S Leaf-Height-Seed……….…….. p.53
SLA Specific leaf area………..………. p.55
LDMC Leaf dry matter content………. p.58
SES Standardized effect size………. p.59
DEH Dynamic equilibrium hyptohesis………... p.84
IDH Intermediate disturbance hypothesis………. p.87
GSL Growing season lenght……….. p.92
occFSstand Standardized estimate of occupied functional space…. p.96
SESPack Standard effect size of packing……….. p.97
xxi
CWS Community-weighted skewness………. p.126
CWK Community-weighted kurtosis………... p.126
NIV Number of individual trait values per species………... p.146
PCover Cover proportion of species with available trait
values………. p.147
SM Seed Mass……….. p.150
LNC Leaf nitrogen content per dry mass………... p.150
GDD Growing degree days……… p.150
FPG French permanent grassland……… p.150
MTV Mean trait values for a species………. p.153
LA Leaf area………... p.184
LPC Leaf phosphorus content per dry mass……….. p.184
PET Potential evapotranspiration………. p.187
AWC Soil available water capacity……… p.187
AW Soil available water content……….. p.187
GSLtw Growing season length……….. p.187
LSM Land surface model………... p.194
xxii
HM Hierarchical model………... p.224
TEMP Mean temperature during the growing season………... p.229
RAIN Accumulated rainfall during the growing season…….. p.229
NNI Nitrogen nutrient index………. p.229
PNI Phosphorus nutrient index... p.229 MCMC Markov Chain Monte Carlo……….. p.235
DIC Deviance information criterion………. p.236
LCC Leaf carbon concentration……… p.247
RepPH Reproductive plant height………. p.247
OF_day Onset of flowering in Julian day………... p.248
OF_DD Onset of flowering in degree-day……….. p.248
FC Field capacity……… p.262
NI Nutrient index……… p.294
CWMLD Community-weighted mean of life duration………….. p.311
CWMPG Proportion of perennial grasses in the community…... p.311
SAD Species abundance distribution………... p.336
xxiii
LISTE DES TABLEAUX
Tableaux tirés du Chapitre II
Tableau 2.1 Definition of abbreviations and units of the nine functional traits………... p.57 Tableau 2.2 Results from the centroid distance analyses for each pair of
successional stages (columns) and each 3-trait hypervolume considered in this study (rows)………. p.64 Tableau 2.3 Mean difference in overlap (in %) and p-values as determined
by a null model analysis using F-values to compare the overlap between pairs of stages………. p.69 Tableau tiré du Chapitre III
Tableau 3.1 Main descriptors and environmental characteristics of the eight study sites……….. p.93 Tableau tiré du Chapitre IV
Tableau 4.1 Hypotheses regarding the effect of different community assembly processes on local trait distribution and
xxiv Tableaux tirés de l’Annexe A
Tableau A1 Geographical and topo-climatic characteristics of the 18 sites
under study..…..……… p.227 Tableau A2 List of environmental variables included in the analyses,
measured at the regional and local spatial scales…………... p.230 Tableau A3 Definition of abbreviations and units of the twelve functional
variables……….... p.232 Tableau A4 Summary of the final models for the twelve traits studied.…….. p.240 Tableaux tirés des Annexes du Chapitre II (Annexes B-D)
Tableau B1 List of species occurring in at least one of the twelve abandoned vineyards of this study with their values of the following
functional traits………. p.281 Tableau C1 Overlap score for each pair of successional stages (columns)
and each 3-trait hypervolumes considered in this study
(rows)……… p.284
Tableaux tirés des Annexes du Chapitre III (Annexes E-K)
Tableau G1 Percentage of the variation in functional trait values explained
by different nested factors: Site/Species/Individuals……… p.300 Tableau G2 Percentage of the variation in functional trait values explained
by different nested factors: Species/Individuals………... p.300 Tableau H1 Supplementary taxonomic and functional details on the sites... p.302
xxv
Tableau K1 Summary of the regression coefficients of significant patterns of species richness (SR), standardized values of the volume of occupied functional space (occFSstand) and standard effect size
of species packing (SESPack) in the communities along a
nutrient index (NI), disturbance intensity (DI), and growing
season length (GSL) gradients……….. p.315 Tableau tiré des Annexes du Chapitre IV (Annexes L-Q)
Tableau O1 Summary of the results for all assembly processes using a
regional prior and observed trait values……… p.332 Tableaux tirés des Annexes du Chapitre V (Annexes R-V)
Tableau R1 Sources and number of vegetation plots in the DivGrass
database………. p.340 Tableau U1 Thresholds of minimum number of trait values (NIV) required
per species to estimate species’ mean trait values with an error
inferior to 20%, 10% and 5%, for specific leaf area (SLA)... p.346 Tableau U2 Thresholds of minimum number of trait values (NIV) required
per species to estimate species’ mean trait values with an error inferior to 20%, 10% and 5%, for mass-based leaf nitrogen
content (LNC)………... p.347 Tableau U3 Thresholds of minimum number of trait values (NIV) required
per species to estimate species’ mean trait values with an error
xxvi
Tableau U4 Thresholds of minimum number of trait values (NIV) required per species to estimate species’ mean trait values with an error
inferior to 20%, 10% and 5%, for plant height………. p.349 Tableau tiré de l’Annexe du Chapitre VI (Annexe W)
Tableau W1 Sources and number of vegetation relevés in the DivGrass
database………... p.352 Tableau W2 Databases and sources for the traits used in DivGrass…………. p.353
xxvii
LISTE DES FIGURES
Figures tirées de l’Introduction générale (Chapitre I)
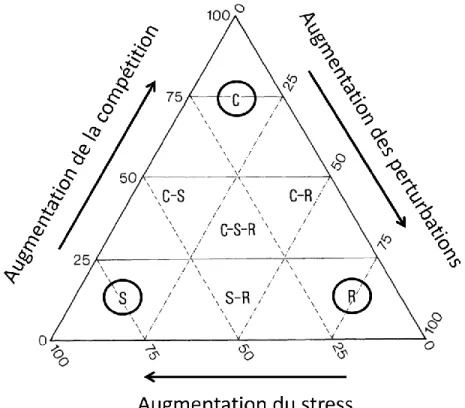
Figure 1.1 Distribution d’abondance des espèces (DAE)……….... p.5 Figure 1.2 Schéma triangulaire des stratégies fonctionnelles C-S-R de
Grime……….. p.13
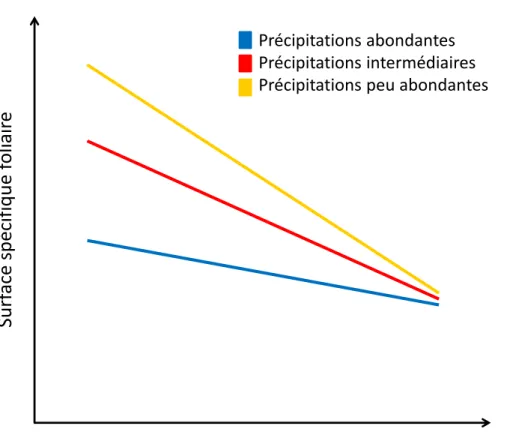
Figure 1.3 Schématisation de l’effet sur la surface spécifique foliaire de différentes variables environnementales agissant à différents niveaux spatiaux et de leurs interactions……… p.17 Figure 1.4 Différents modèles généraux de la modification de la structure
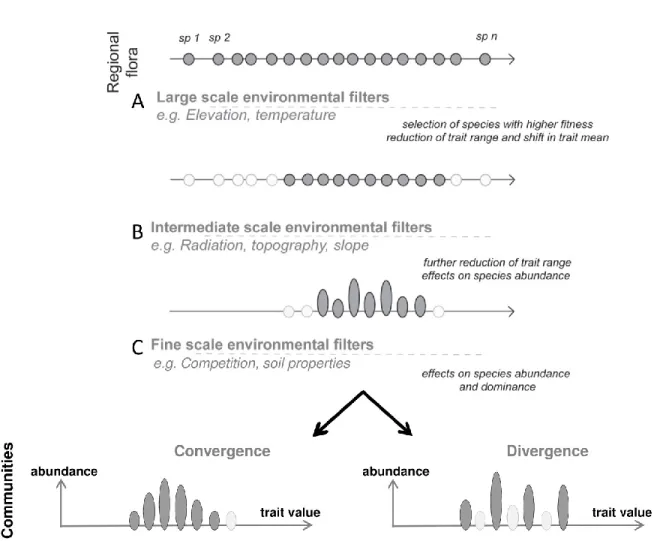
fonctionnelle subie par des communautés distribuée le long de gradients environnementaux……….. p.22 Figure 1.5 Schéma hiérarchique des différents types de filtres
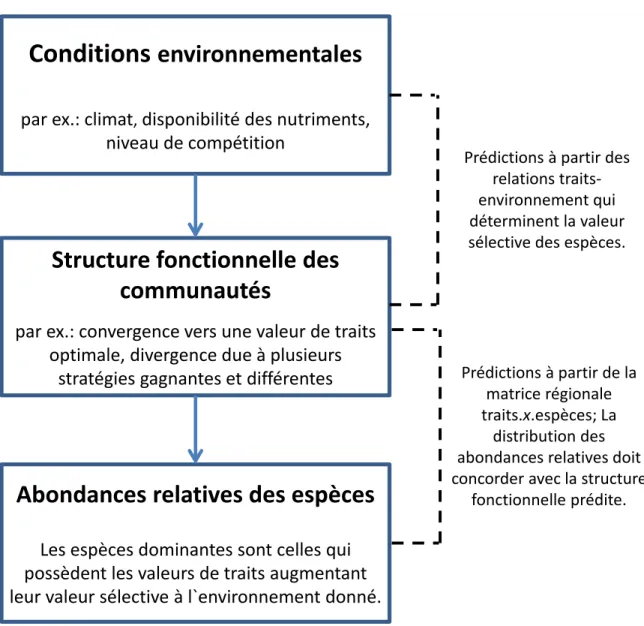
environnementaux pouvant affecter l’assemblage de communautés locales……….. p.25 Figure 1.6 Schéma simplifié de la théorie (non-statistique) sur laquelle
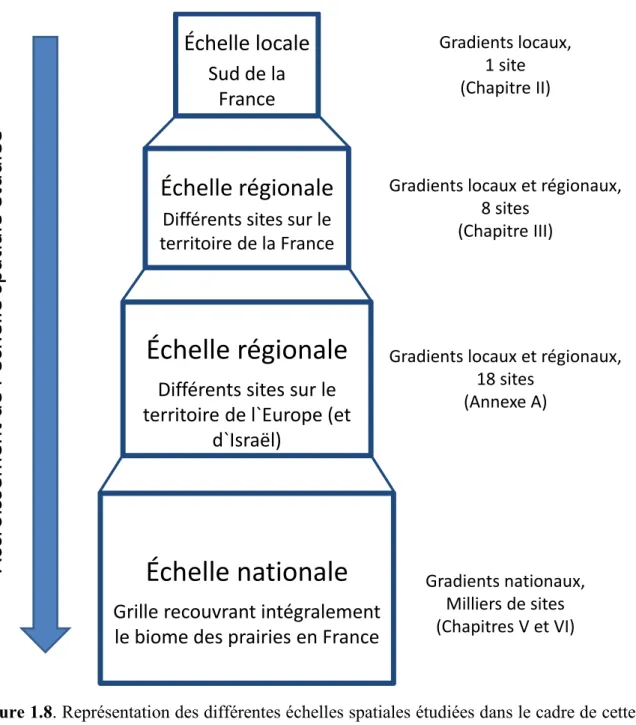
les modèles de prédictions de l’assemblage des communautés tels que CATS se basent.……… p.36 Figure 1.7 Les trois facettes de la biogéographie fonctionnelle………….. p.38 Figure 1.8 Représentation des différentes échelles spatiales étudiées dans
xxviii
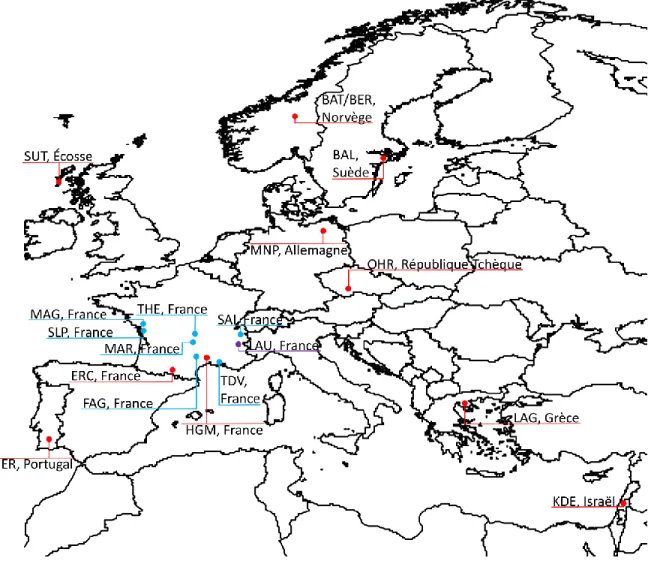
Figure 1.9 Emplacement géographique des sites d’étude des programmes VISTA (rouge) et DivHerbe (bleu) utilisés dans cette thèse….. p.45 Figure 1.10 Distribution spatiale des prairies françaises selon les 51 486
relevés botaniques de l’initiative DivGrass……… p.47 Figures tirées du Chapitre II
Figure 2.1 Pairwise plots representing the displacement across successional stages and along trait axes of the three dimension-specific hypervolumes……….. p.63 Figure 2.2 Variation in standardized effect size (SES) of the
hypervolume of grassland communities along a successional gradient………... p.66 Figure 2.3 Variation during succession (x-axis of each panel) of the
standardized effect size (SES) values of hypervolumes calculated from the 27 L-H-S combinations (y-axis of each panel)……….. p.68 Figures tirées du Chapitre III
Figure 3.1 Hypothetical illustration of how species richness, volume of available niche space, and species packing in a local community are expected to vary along local gradients of nutrient availability (a) and disturbance intensity (b)……….... p.90
xxix
Figure 3.2 Predicted species richness (SR) from a significant linear mixed model (see main text for details) as a function of a nutrient index (NI; a, b, c) and disturbance intensity (DI; d, e,
f)………...….. p.100 Figure 3.3 Predicted standardized occupied functional space (occFSstand)
from a significant linear mixed model (see main text for details) as a function of a nutrient index (NI; a, b, c) and
disturbance intensity (DI; d, e, f)………...…………. p.101 Figure 3.4 Predicted SES of species packing (SESPack) from significant
linear mixed models (see main text for details) along a
disturbance intensity gradient....………. p.102 Figures tirées du Chapitre IV
Figure 4.1 Conceptual framework of community assembly processes…... p.122 Figure 4.2 Fit of the trait-abundance relationship in local communities
assembled through directional filtering, plotted against an
immigration gradient……….. p.130 Figures tirées du Chapitre V
Figure 5.1 Species-level and community-level trait measurements: comparisons between on-site trait values and trait values
extracted from the TRY database………... p.155 Figure 5.2 Impact of the number of individual values (NIV) on the
estimates of species’ mean trait values using the TRY
xxx
Figure 5.3 Impact of the number of individual trait values per species (NIV) in TRY and of the community-level cover proportion (PCover) of species for which trait values were available in
TRY on the estimation of Community Weighted Means
(CWM)………... p.158
Figure 5.4 Effect of dataset selection criteria (i.e. minimum NIV and PCover required) on the dataset size and gradient
representativeness………... p.159 Figure 5.5 Impact of the dataset selection criteria on the Growing Degree
Day (GDD) gradient coverage and on the relationship
between CWMSLA and GDD at the climate grid-cell level…… p.160
Figure 5.6 NIV – PCover tradeoff across the whole dataset………... p.165
Figures tirées du Chapitre VI
Figure 6.1 (A) Spatial distribution of French permanent grasslands (FPGs) and (B) location of the 51,486 vegetation relevés
collated in the DIVGRASS database………. p.180 Figure 6.2 Distribution of functional groups in the DIVGRASS
vegetation relevés………... p.183 Figure 6.3 Trait availability in the plant traits module of the DIVGRASS
ecoinformatics platform………. p.185 Figure 6.4 A comparison between on-site leaf dry matter content
(LDMC, mg.g-1) and LDMC values extracted from the TRY
xxxi
Figure 6.5 Community Weighted Mean of Leaf Dry Matter Content (CWM LDMC) as a function of Growing Season Length estimated through temperature and water limitations (GSLtw,
days)………... p.191 Figure 6.6 Mapping of Leaf Dry Matter Content (CWM LDMC) of
permanent grasslands across France, potential evapotranspiration during the growing season and predicted
forage digestibility……….. p.192 Figures tirées de la Discussion générale et conclusion (Chapitre VII)
Figure 7.1 Schéma conceptuel illustrant comment des compromis fonctionnels se produisant le long de gradients d’utilisation des terres ou de succession secondaire peuvent se traduire en compromis entre certaines propriétés et services
écosystémiques………... p.208 Figure 7.2 Théorie de l’assemblage d’une communauté locale à partir
d’un pool régional, sans considération de la variabilité
intraspécifique……… p.211 Figure 7.3 Théorie révisée de l’assemblage d’une communauté locale à
partir d’un pool régional, avec considération de la variabilité
intraspécifique……… p.213 Figures tirées de l’Annexe A
xxxii
Figure A2 Mean effect of the local variables (βij) on the CWM of the
traits in the final models………. p.239 Figure A3 Comparison of the variance of the parameters (αij and βij) of
the final models……….. p.245 Figure AB1 Regression summary of the final models, in twelve parts…….. p.268-280 Figures tirées des Annexes du Chapitre II (Annexes B-D)
Figure C1 Bar plots of overlap scores for all 30 hypervolumes calculated between early and middle succession (upper panel), early and late succession (middle panel) and middle and late succession
(lower panel)……….. p.286 Figure D1 Functional trait variation during succession for the nine traits
considered in this study……….. p.288 Figure D2 Pairwise plots representing the displacement across
successional stages and along trait axes of the three dimension-specific hypervolumes weighted with species
relative abundances……… p.290 Figures tirées des Annexes du Chapitre III (Annexes E-K)
Figure F1 Illustration of the range and distribution of values for the local
environmental variables………. p.298 Figure I1 Boxplot of the frequency of disturbances measured at the plot
xxxiii
Figure I2 Predicted species richness (SR) from a significant linear mixed model (see main manuscript for the construction of the models) along a nutrient index (NI; a, b, c) and disturbance
frequency (DF; d, e, f) gradients……… p.306 Figure I3 Predicted standardized values of occupied volume of
functional space (occFSstand) from a significant linear mixed
model (see main manuscript for the construction of the models) along nutrient index (NI; a, b, c) and disturbance
frequency (DF; d, e, f) gradients……… p.307 Figure I4 Predicted SES of species packing (SESPack) from a significant
linear mixed model (see main manuscript for the construction
of the models) along a disturbance frequency gradient……….. p.308 Figure J1 Predicted proportion of perennials in the communities
(expressed as a CWMLD) from a significant linear mixed
model (see main text for details) along nutrient index (NI; A, B, C) and disturbance intensity (DI; D, E, F) gradients for
different growing season lengths (GSL)………... p.312 Figure J2 Predicted proportion of perennial grasses in the communities
(expressed as a CWMPG) from a significant linear mixed
model (see main text for details) along nutrient index (NI; A, B, C) and disturbance intensity (DI; D, E, F) gradients for
different growing season lengths (GSL)……… p.313 Figures tirées des Annexes du Chapitre IV (Annexes L-Q)
xxxiv
distribution according to different types of habitat filtering….. p.317 Figure M1 Mean values for the four first moments of the trait distribution
in local communities shaped through various assembly
processes………. p.320 Figure O1 Fit of the trait-abundance relationship in local communities
assembled through purely neutral assembly, plotted against an
immigration gradient……….. p.329 Figure O2 Fit of the trait-abundance relationship in local communities
assembled through stabilizing filtering, plotted against an
immigration gradient……….. p.330 Figure O3 Fit of the trait-abundance relationship in local communities
assembled through disruptive filtering, plotted against an
immigration gradient……….. p.331 Figure P1 Fit of the trait-abundance relationship in local communities,
plotted against an immigration gradient. These communities
were shaped by neutral assembly…………..………….……… p.334 Figure P2 Fit of the trait-abundance relationship in local communities,
plotted against an immigration gradient. These communities
were shaped by directional filtering………... p.335 Figure P3 Fit of the trait-abundance relationship in local communities,
plotted against an immigration gradient. These communities
xxxv
Figure P4 Fit of the trait-abundance relationship in local communities, plotted against an immigration gradient. These communities
were shaped by disruptive filtering……… p.337 Figure Q1 Fit of the trait-abundance relationship in local communities,
plotted against an immigration gradient. These communities were shaped by directional filtering where the optimal trait
value was within the available range (uniform prior)………… p.338 Figure Q2 Fit of the trait-abundance relationship in local communities,
plotted against an immigration gradient. These communities were shaped by directional filtering where the optimal trait
value was within the available range (regional prior)………… p.339 Figures tirées des Annexes du Chapitre V (Annexes R-V)
Figure S1 Methodology used in the estimation of the impact of the number of individual values (NIV) on the mean trait values of
species in TRY………... p.343 Figure T1 Methodology used for the estimation of the impact of the
number of individual trait values per species in TRY (NIV) and the coverage proportion for which mean trait value of species were available in TRY (PCover) on the estimation of
Community Weighted Mean (CWM)……… p.345 Figure V1 Impact of the number of individual values (NIV) on the
probability to discriminate pairs of species based on their
CHAPITRE I –
INTRODUCTION GÉNÉRALE
1.1 – Histoire et développement de l’écologie des communautés
La nature a toujours exercé une attraction particulière sur les humains. Très tôt déjà, le besoin d’identifier, de caractériser et d’inventorier les différentes espèces qui nous entourent a été ressenti; Historia animalium (Aristotélēs, 384-322 av. J.C.) et Historia
Plantarum (Théophrastos, 372-287 av. J.C.) sont les premières œuvres connues sur le sujet.
Aujourd’hui, le besoin de simplement caractériser notre entourage biotique a fait place au besoin de comprendre les processus et les facteurs causant les patrons observés en nature et de prédire les changements futurs de ces patrons. Ce savoir est d’une importance de plus en plus grande dans nos sociétés contemporaines puisqu’il nous est essentiel afin de protéger et d’exploiter de façon adéquate et efficace nos ressources naturelles. Le domaine de l’écologie des communautés se consacre à la recherche de réponses à ces questions. Il n’existe encore aucune définition fixe et universelle pour le concept de communauté, mais une définition générale peut être formulée comme suit: Une communauté est un assemblage d’espèces partageant le même espace en même temps et interagissant ensemble (Begon et
al., 2006). Par contre, toute définition de temps et d’espace est arbitraire et
contexte-dépendante, ce qui fait que le terme « communauté » peut prendre plusieurs sens différents dans l’écologie des communautés contemporaine (Mittelbach, 2012).
Pour passer des travaux de Théophrastos au niveau de connaissance actuel dans le domaine de l’écologie des communautés, il a fallu plus de deux millénaires durant lesquels la discipline ne s’est développée que lentement. C’est au courant du XIXe siècle que la
perception de la distribution des espèces a pris un tournant décisif dans le monde scientifique. Le grand explorateur et scientifique Alexander von Humboldt fut un des précurseurs de ce changement. Célèbre pour son exploration de l’Amérique latine et son approche holistique de l’univers, du monde et de la nature, il publia de nombreux ouvrages tout au long de la première moitié du XIXe siècle, notamment un essai sur la distribution géographique des plantes et les différents types de communauté qui en résultent (von Humboldt et Bonpland, 1805). De telles observations sur les différents patrons de diversité, de distribution et d’abondance des espèces le long de gradients environnementaux ont mené les naturalistes Charles R. Darwin et Alfred R. Wallace à développer la célèbre théorie de la sélection naturelle des espèces (Darwin et Wallace, 1858). Ceci constitua la pierre angulaire sur laquelle s’appuient encore aujourd’hui les disciplines de l’écologie des populations et des communautés. C’est durant cette même époque que le terme même d’écologie (ou plutôt « Oecologie ») fut officiellement introduit par Ernst Haeckel qui reconnut déjà l’intérêt de cette nouvelle discipline dont l’objectif est de comprendre les relations entre les organismes vivants et leur environnement (Haeckel, 1866).
À l’aide d’expériences semi-contrôlées, les écologues ont en même temps commencé à comprendre de façon plus précise et plus complète les patrons de distribution des espèces en relation avec différentes conditions environnementales. Un exemple est « The Park
Grass Experiment ui a été lancée en 1856 à Rothamsted, Angleterre, et qui dure encore
aujourd’hui, ce qui en fait la plus longue expérience du monde en écologie (Silvertown et
al., 2006). Le but premier de cette expérience était à caractère agronomique, voulant
déterminer l’effet de la fertilisation artificielle sur différentes espèces herbacées prairiales (Lawes et Gilbert, 1859). Alors que les traitements ont continué à être appliqués et que les changements des communautés des différentes parcelles étaient documentés à chaque année, ce projet s’est révélé être une source d’information aussi profonde que variée pour le domaine de l’écologie des communautés et ce, pendant plus d’un siècle (les contributions scientifiques du Park Grass Experiment sont résumées dans Silvertown et al., 2006).
Cependant, au début de l’écologie des communautés, une expérience à grande échelle comme le Park Grass Experiment était l’exception plutôt que la règle et ce sont surtout des études fondées sur l’observation qui dominaient. Celles-ci ont éventuellement menées au développement de théories toujours de plus en plus complètes et générales sur les associations entre l’environnement et la présence des espèces. De bons exemples sont les travaux d’Andreas F. W. Schimper (Schimper, 1898), qui démontrent des liens entre les divers besoins physiologiques des plantes et leur distribution géographique, et ceux d’Eugenius Warming (Warming et Vahl, 1909), qui présentent les grands biomes de la planète et décrivent comment, à travers ces biomes, différentes espèces de plantes se sont adaptées de façon similaire à des conditions défavorables similaires comme par exemple la sécheresse. Par la suite, Frederic E. Clements a développé ses travaux sur la succession des communautés végétales vers un climax particulier et fixe selon des conditions environnementales spécifiques (Clements, 1916; Weaver et Clements, 1938). Dans ces travaux, la communauté est considérée comme un organisme complexe en développement vers un état fixe et constitue donc l’unité d’observation. Cette vision «fixe» des communautés a cependant été critiquée par plusieurs écologues, notamment Henry A. Gleason et William S. Cooper, qui démontrent une réticence à conceptualiser de manière stricte le développement des communautés comme le fait Clements. Ils développent tous deux une vision individualiste des communautés qui se rapproche plus de la vision contemporaine, où chaque espèce est sujette à ses propres contraintes de colonisation et de distribution et où un grand nombre de facteurs sont susceptibles d’influencer la succession, qui elle-même n’est pas un processus fixe (Cooper, 1926; Gleason, 1926, 1927). Arthur G. Tansley (1935) critique avec ferveur à la fois la sémantique utilisée par Clements et par Cooper. Alors que ces derniers se concentrent sur la sphère biotique, Tansley propose pour la première fois le concept d’écosystème en soulignant l’importance en écologie de considérer à la fois les facteurs biotiques, les facteurs abiotiques et leurs échanges pour comprendre les patrons observés. Josias Braun-Blanquet a quant à lui apporté une précieuse contribution à notre façon d’analyser les communautés végétales et de quantifier et classifier leur structure (Braun-Blanquet et al., 1932).
Ces premières descriptions des relations entre la structure des communautés – c’est-à-dire les espèces qu’on y retrouve et leurs abondances – et les variables environnementales ainsi que la théorie de la sélection naturelle ont donc permis de commencer à comprendre les patrons observés et à identifier les processus qui en sont responsables. L’étape suivante a été l’élaboration de techniques et de modèles plus spécifiques, permettant de lier quantitativement l’environnement des espèces et leur distribution. Par exemple, la description mathématique du concept de sélection par l’environnement biotique, c’est-à-dire les interactions entre différentes espèces (Lotka, 1925; Volterra, 1931), a donné naissance aux équations bien connues de Lotka-Volterra permettant de prédire l’effet des interactions inter-espèces sur le taux de croissance d’une population particulière. Un autre exemple sont les travaux de Whittaker (1956), découlant des idées de Gleason et Tansley et portant sur la visualisation graphique et la comparaison de la structure d’une communauté d’arbres le long de différents gradients environnementaux.
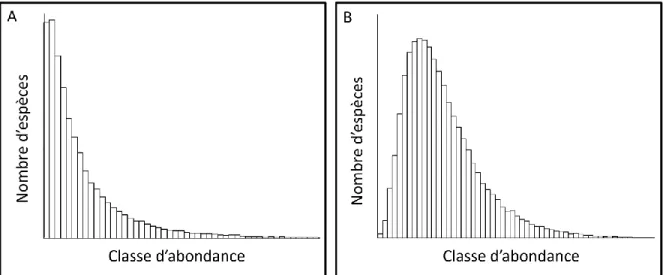
En parallèle avec ces nouveaux développements, la modélisation statistique de la distribution d’abondance des espèces (DAE) a vu le jour (Fisher et al., 1943), une discipline ayant un grand potentiel pour nous permettre de mieux comprendre les mécanismes structurant les communautés (McGill et al., 2007). Dans une communauté, on trouve toujours un grand nombre d’espèces rares et peu d’espèces communes et ceci constitue une des rares lois universelles en écologie (McGill et al., 2007). C’est donc dans les années 1940 – à l’exception de Motomura (1932), disponible uniquement en japonais à l’époque – que les écologues ont commencé à observer que la DAE pouvait être approximée avec succès à partir d’une fonction mathématique. En représentant dans un histogramme le nombre d’espèces dans chaque classe d’abondance (nombre d’individus par espèces) d’une communauté, Sir Ronald Fisher et ses collègues ont donc observé que les DAE suivaient une distribution logarithmique (Fig. 1.1A), où les classes d’abondance les plus faibles ont toujours le plus grand nombre d’espèces (Fisher et al., 1943). Cependant, Frank W. Preston postula qu’à mesure que l’effort d’échantillonnage augmente, c’est-à-dire que la chance d’échantillonner les espèces les plus rares augmente, la DAE suivra plutôt
une distribution log-normale (Fig. 1.1B; Preston, 1948). Ces premiers modèles de DAE se sont au début développés sans considération des mécanismes responsables de la forme des
Figure 1.1. Distribution d’abondance des espèces (DAE). A- DAE suivant une distribution logarithmique selon Fisher. B- DAE suivant une distribution log-normale selon Preston.
distributions observées, le but étant seulement de les caractériser mathématiquement (Hubbell, 2001). Très vite par contre, un autre type de modèle de DAE s’est développé, intégrant les notions d’immigration, de naissance et de mortalité (Hubbell, 2001; Kendall, 1948). Aujourd’hui, les DAE sont toujours très explorées et quatre types de modèles de DAE, en plus des modèles purement statistiques, ont été développés pour tenter de comprendre les mécanismes qui en sont responsables: processus de spéciation, dynamiques des populations, partitionnement des niches et distribution spatiale (voir McGill et al., 2007 pour les détails et des exemples de ces différents types de modèles). Un problème potentiel des modèles de DAE est le fait que plusieurs d’entre eux ne font que prédire la forme creuse typique de la DAE, ce qui les rend infalsifiables (McGill et al., 2007). Selon McGill et al., la théorie neutre (Hubbell, 2001) résout en partie ce problème en travaillant d’abord avec une série de suppositions desquelles on peut dériver non seulement une DAE, mais aussi plusieurs autres patrons écologiques. Cette théorie sera discutée de façon plus
détaillée plus loin, mais disons simplement ici que sa supposition de base la plus frappante est la complète équivalence entre les différentes espèces d’une communauté, c’est-à-dire qu’il n’y a pas de partitionnement de niche ni d’occupation optimale d’une niche puisque chaque espèce est écologiquement équivalente. Au final, peu importe le type de modèle utilisé pour modéliser les DAE, l’intégration de gradients environnementaux dans les analyses, que ce soient des gradients spatiaux ou temporels, est une perspective prometteuse et essentielle pour l’avancement du domaine d’étude des DAE (McGill et al., 2007).
Effectivement, l’environnement est depuis toujours reconnu comme un facteur important à considérer en écologie. Le concept de niche écologique est d’ailleurs entièrement basé sur les relations entre les organismes et leur environnement, quoiqu’il puisse être vu sous deux angles différents. D’un côté la niche d’un organisme peut être définie comme son rôle écologique, c’est-à-dire la façon dont il modifie son environnement et la disponibilité des ressources dans son habitat (Elton, 1937). De l’autre côté, la niche d’un organisme est plutôt définie comme ses besoins écologiques pour survivre (Grinnell, 1917). Sauf avis contraire, dans cette thèse je travaillerai avec la deuxième définition et ici une différence doit être faite entre la niche fondamentale, considérant seulement l’environnement abiotique, et la niche réalisée, considérant en plus les interactions interspécifiques comme la compétition (Hutchinson, 1957). Dans le concept de partitionnement des niches écologiques, on suppose donc que différentes espèces auront des exigences différentes quant aux ressources nécessaires à leur survie et des mécanismes différents pour acquérir ces ressources, leur permettant de coexister. Ce concept, initialement abordé par Darwin et Wallace (1858), représente une des perspectives principales pour non seulement expliquer les distributions d’abondance des espèces observées (MacArthur, 1957), mais aussi certains autres patrons écologiques. Un exemple est la relation entre productivité primaire nette et richesse spécifique. Effectivement, l’hypothèse est qu’à long terme, les différences de niche entre espèces permettraient une utilisation plus complète et efficace des ressources limitantes (comme l’azote du sol), ce qui en retour affecterait à la hausse la productivité
d’un site (Fargione et al., 2007; Loreau et Hector, 2001; Marquard et al., 2009). Il faut cependant noter que cette hypothèse n’est pas la seule tentant d’expliquer la relation productivité-diversité. L’alternative principale est l’effet d’échantillonnage, stipulant qu’avec l’augmentation de la diversité, la chance d’avoir des espèces très productives dominant la communauté augmente aussi, ce qui expliquerait pourquoi la productivité et la diversité sont positivement corrélées (Aarssen, 1997; Huston, 1997; Loreau et Hector, 2001).
L’étude de l’écologie des communautés a donc évolué vers des concepts de plus en plus complexes et/ou complets pour tenter d’expliquer et prédire, étant donné des conditions environnementales particulières, la structure d’une communauté locale. Cependant, avant d’aller beaucoup plus loin dans la modélisation de l’écologie des communautés, deux points importants méritent d’être présentés ici et décrits plus en détails: le passage de l’identité taxonomique à l’identité fonctionnelle et, découlant de ce passage, l’importance de travailler dans un contexte de gradients environnementaux. De plus, bien que plusieurs des exemples cités ci-dessus et ci-dessous puissent s’appliquer aussi bien aux communautés animales qu’aux communautés végétales, dans le cadre de cette thèse, je me concentrerai principalement sur la littérature portant sur les plantes.
1.2 – De l’identité taxonomique à l’identité fonctionnelle
Un trait fonctionnel est défini comme étant:
« […] any morphological, physiological or phenological feature measurable
at the individual level, from the cell to the whole-organism level, without reference to the environment or any other level of organization. » (Violle et al., 2007).
Un trait devrait aussi refléter une adaptation aux conditions environnementales, c’est-à-dire sa valeur sélective (Violle et al., 2007). Cette relation entre trait et adaptation permet donc en principe d’identifier la niche écologique d’un individu, c’est-à-dire les conditions environnementales requises à sa survie et à son succès reproducteur (Hutchinson, 1957), à partir de la valeur de ses traits fonctionnels (Tilman, 2004; Violle et Jiang, 2009). Il est cependant important de noter que ces relations sont plus souvent inférées que démontrées dans la littérature, ce qui est un problème réel en écologie fonctionnelle (Shipley et al., 2015) qui sera discuté plus loin. Néanmoins, le rôle inhérent de ces attributs pour la détermination du succès relatif des différentes espèces dans différentes conditions environnementales était déjà supposé au début de l’écologie elle-même (Darwin et Wallace, 1858; Haeckel, 1866; Raunkiӕr, 1934; Schimper, 1898; Warming et Vahl, 1909). De plus, l’importance que prendrait le passage de l’identité taxonomique vers l’identité fonctionnelle dans les analyses était déjà préssenti il y a plus de 100 ans:
« Just as species are the units in systematic botany, so are growth-forms the
units in oecological botany. […] It cannot be sufficiently insisted that the greatest advance, not only in biology in its wider sense, but also in oecological phytogeography, will be the oecological interpretation of the various growth-forms: from this ultimate goal we are yet far distant. »
(Warming et Vahl, 1909, chapitre 2, page 5).
Comme préssenti cependant, cette vision était effectivement bien avant son temps, ne faisant l’objet que d’une simple note de bas de page 20 ans plus tard:
« It has often occurred to the writer that much of the structural variation in
… [a community] … would disappear if those taxonomic units which have the same vegetational form and behavior could be considered as a single ecological unit. » (Gleason, 1926).
Il a donc fallu des décennies avant que cette idée du passage de l’identité taxonomique à l’identité fonctionnelle ne prenne vraiment racine dans la vision et la méthodologie des écologues. De fait, traditionnellement les espèces (ou populations) ont été les unités d’observation utilisées en écologie des communautés. Non seulement cette façon de faire réduit le potentiel d’extrapolation des résultats entre régions avec peu ou pas d’espèces communes, mais elle devient aussi très vite difficilement applicable lorsque le nombre