Université de Montréal
Le Délai entre le traumatisme médullaire et la chirurgie a-t-il un
impact sur la survenue de complications durant la phase aigüe
d’hospitalisation?
par
Étienne Bourassa-Moreau
Département de chirurgie Faculté de Médecine
Mémoire présenté à la Faculté des études supérieures en vue de l’obtention du grade de
Maître ès sciences (M.Sc.) en Sciences biomédicales option Mobilité et Posture
Avril, 2014
i
Résumé
Le délai optimal entre une lésion médullaire traumatique (LMT) et la chirurgie demeure indéterminé. Cependant, la relation entre la prévention de complications et le délai chirurgical n’a jamais été spécifiquement étudiée.
L’objectif principal de ce travail était de détecter si les taux de complications chez des LMT étaient associés avec le délai chirurgical. L’objectif secondaire était d’identifier si le délai chirurgical est un prédicteur indépendant de la survenue de complications.
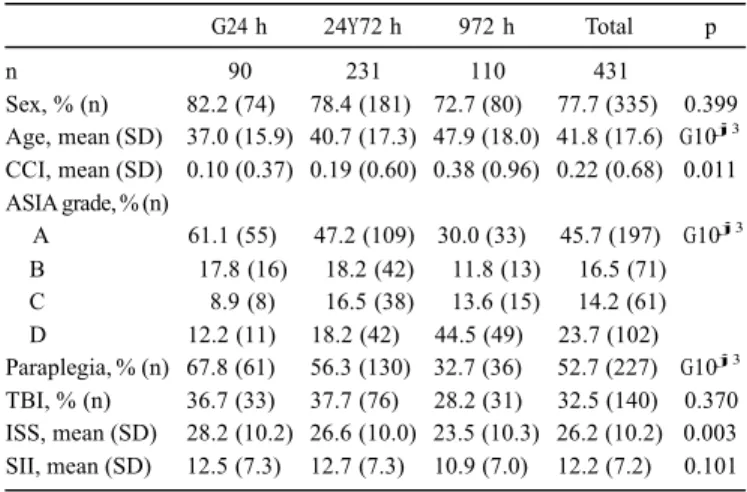
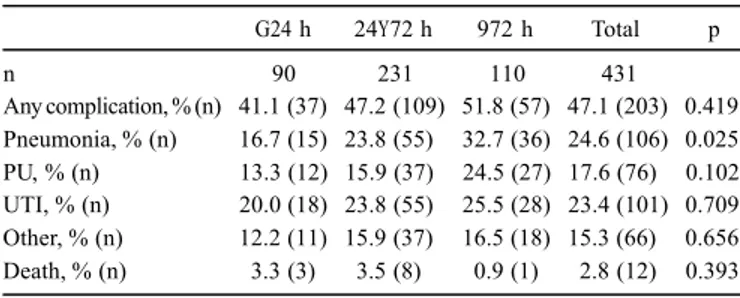
Un premier article présente l’analyse d’une cohorte rétrospective de 431 LMTs. Une chirurgie réalisée dans un délai inférieur à 24h (ou inférieur à 72h si un délai de 24h ne peut être respecté) prédisait une diminution du taux de l’ensemble des complications, du taux de pneumonies et du taux de plaies de pression. Les autres facteurs prédictifs de complications identifiés étaient : l’âge, la sévérité de l’atteinte neurologique de la lésion selon l’échelle ASIA, un traumatisme cervical plutôt que thoracique, la présence de comorbidités, la sévérité du traumatisme selon l’échelle ISS et la complexité de la chirurgie.
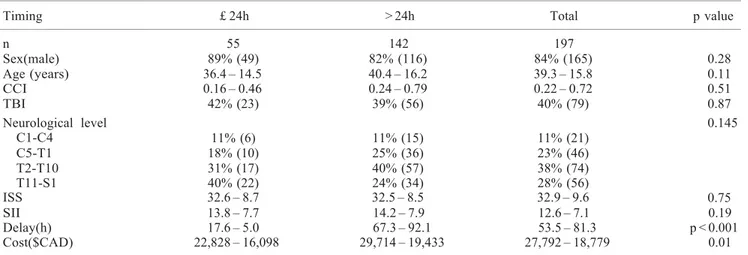
Les connaissances actuelles suggèrent qu’une opération chirurgicale rapide n’a que peu d’effet sur la récupération neurologique chez les LMTs complètes (interruption complète des fonctions sensorimotrices). Pour cette raison, notre second article analyse l’impact du délai chirurgical sur la survenue des complications à partir d’une sous-population de 197 LMTs complètes de notre cohorte. Un délai chirurgical supérieur à 24h prédisait une augmentation des complications, notamment les pneumonies et les infections urinaires.
Bien que des études prospectives randomisées sont nécessaires pour confirmer nos conclusions, nos études supportent un délai chirurgical rapide afin de diminuer le taux de complications non neurologiques chez les LMTs.
Mots-clés : Lésion Médullaire, Traumatisme, Délai chirurgical, Complications, Pneumonies,
iii
Abstract
Optimal timing of surgery after traumatic spinal cord injury (SCI) is one of the most controversial subjects in spine surgery. However, the relationship between prevention of peri-operative complications and timing of surgical decompression was never specifically studied.
The primary goal of our study was to evaluate if the peri-operative complication rate was associated with surgical timing. The secondary goal of our study was to identify if surgical timing is an independent predictor of complications.
A first publication presents the analysis of a retrospective cohort of 431 cases of traumatic SCI. A reduction in the global rate of complications as well as the incidence of pneumonia and pressure ulcer were predicted by surgery performed earlier than 24 hours (or earlier than 72 hours if the surgery could not be performed within 24 hours following the SCI). Other predictors where statistically related to the occurrence of complications: increasing age, severity of neurological injury, a cervical rather than a thoracic lesion, medical comorbidities, the severity of trauma, and the complexity of surgery.
Previous studies suggest that early surgery is of little benefit for neurological recovery in complete traumatic SCI (with complete interruption of sensorimotor function). Therefore our second publication analyzed the impact of early surgical intervention in the sub-population of 197 complete SCI. Surgical timing later than 24 h was a predictor of complications, specifically pneumonia and UTI.
Although a randomized controlled trial is needed to confirm our findings, our studies support that early surgical timing after traumatic SCI (typically within 24 hours) could decrease the rate of non neurological complications.
Keywords : Spinal Cord Injury, Trauma, Surgical Timing, Complications, Pneumonia,
v
Table des matières
RÉSUMÉ ... I ABSTRACT ... III LISTE DES FIGURES ... VIII REMERCIEMENTS ... X
INTRODUCTION ... 1
1. CONSIDÉRATIONS HISTORIQUES ... 2
2. ANATOMIE, PHYSIOLOGIE ET CORRÉLATION CLINIQUE ... 4
2.1 L’ANATOMIE DE LA COLONNE VERTÉBRALE ... 4
2.2 PHYSIOLOGIE DE LA COLONNE VERTÉBRALE ... 7
2.2.1 Support postural ... 7
2.2.2 Mobilité vertébrale ... 7
2.2.3 Protection neurologique ... 8
2.3 ANATOMIE ET PHYSIOLOGIE DE LA MOELLE ÉPINIÈRE ... 9
2.3.1 Segments médullaires ... 9
2.3.3 Fonctions médullaires autonomes et réflexes médullaires ... 15
3. MÉCANISMES PATHOLOGIQUES CELLULAIRES ET MOLÉCULAIRES DE LA LÉSION MÉDULLAIRE ... 17
4. ÉPIDÉMIOLOGIE ET IMPACT SOCIOÉCONOMIQUE ... 19
4.1 INCIDENCE ET PRÉVALENCE ... 19
4.2 ÉTIOLOGIE DE LA LMT ... 20
4.3 NIVEAU DE LA LÉSION ... 21
4.4 SÉVÉRITÉ DE LA LÉSION ... 22
4.5 LÉSIONS ASSOCIÉES ... 22
4.6 SURVIE DURANT LA PHASE AIGUË ... 23
4.7 ESPÉRANCE DE VIE ... 23
4.9 PARTICIPATION PROFESSIONNELLE ... 24
5. IMPLICATIONS CLINIQUES SUIVANT LA LÉSION MÉDULLAIRE ... 25
5.1 RÉCUPÉRATION NEUROLOGIQUE ... 25
5.1.2 Évolution neurologique naturelle ... 26
5.2 COMPLICATIONS INTRA-‐HOSPITALIÈRES ... 28
5.2.1 Complications fréquentes ... 29
5.2.2 Facteurs prédicteurs des complications intra hospitalières ... 35
5.2.3 Délai chirurgical et complications : mécanisme physiologiques ... 37
6. LA PRISE EN CHARGE DU BLESSÉ MÉDULLAIRE ... 38
6.1 PRISE EN CHARGE EN PÉRIODE AIGÜE ... 38
6.2 PRISE EN CHARGE CHIRURGICALE ... 39
6.3 CENTRES SPÉCIALISÉS DANS LA PRISE EN CHARGE DES LÉSIONS MÉDULLAIRES ... 40
7. L’IMPACT DU DÉLAI CHIRURGICAL ... 40
7.1 DÉLAI CHIRURGICAL ET RÉCUPÉRATION NEUROLOGIQUE ... 41
7.2 DÉLAI CHIRURGICAL ET COMPLICATIONS EN PHASE AIGÜE ... 44
7.2.1 Délai chirurgical et complications : études cliniques ... 44
8. RÉSUMÉ DE LA PROBLÉMATIQUE DE RECHERCHE ... 47
8.1 HYPOTHÈSES DE RECHERCHE ... 49
8.2 OBJECTIFS DE RECHERCHE ... 49
9. MATÉRIEL ET MÉTHODE ... 51
9.1 CRITÈRES D’INCLUSION ET D’EXCLUSION ... 51
9.2 VARIABLE INDÉPENDANTE ... 51
9.3 VARIABLE DÉPENDANTE ... 52
9.4 COVARIABLES ... 52
9.5 ANALYSES STATISTIQUES ... 53
10. PRÉSENTATION DES ARTICLES ... 53
10.1 ARTICLE 1 ... 53
10.2 ARTICLE 2 ... 55
10.3 CONTRIBUTIONS DES AUTEURS AUX ARTICLES ... 56
vii
11.2 ANALYSE DES COMPLICATIONS ... 61
11.2.1 Résultats de nos études ... 61
11.2.2 Détection des complications ... 62
11.2.3 Facteurs de risques des complications ... 64
11.2.4 Corticostéroïdes à haute dose et complications ... 65
11.2.5 Mécanismes de diminution des complications ... 66
11.3 EXCLUSION DES LMTS CENTROMÉDULLAIRES ... 67
11.4 PERSPECTIVES D’AVENIR ... 68
12. CONCLUSION ... 70
BIBLIOGRAPHIE ... 72 LISTE D’ABRÉVIATIONS ... I ANNEXES ... II ANNEXE 1 : AMERICAN SPINAL INJURY ASSOCIATION CLASSIFICATION OF SPINAL CORD INJURY ... II ANNEXE 2. ARTICLE 1: COMPLICATIONS IN ACUTE PHASE HOSPITALIZATION OF TRAUMATIC ... IV SPINAL CORD INJURY: DOES SURGICAL TIMING MATTER? ... IV ANNEXE 3. ARTICLE 2 NON-‐NEUROLOGICAL OUTCOMES AFTER COMPLETE TRAUMATIC SPINAL CORD INJURY: THE IMPACT OF SURGICAL TIMING ... XI
Liste des figures
Figure 1 - La Colone Vertébrale ... 5
Figure 2 - La Vertèbre et le Segment Intervertébral ... 6
Figure 3 - La Moelle Épinière ... 10
Figure 4 - Racines Nerveuses et Moelle Épinière ... 12
Figure 5 - Coupe de la Moelle Épinière ... 13
ix
Ce mémoire est dédicacé à mes parents, Pauline et Thierry qui m’ont transmis leur curiosité, et leur passion pour la connaissance.
Remerciements
Je tiens à remercier Cynthia Thompson, Valérie Desrosiers, Jean Paquet et tous les employés du centre de recherche de l’Hôpital du Sacré-Cœur de Montréal pour leur aide et leur patience.
Je remercie la fondation de recherche en orthopédie à Montréal (FRÉOM) et
l’organisme MENTOR (le programme de recherche en musculosquelettique des IRSC) pour leur support financier.
Je remercie Debbie Feldman et Dany Gagnon de l’IRGLM pour leur soutien et pour avoir partagé leur vision de la recherche.
Je remercie mon Co-directeur Stefan Parent pour le partage généreux de ses connaissances et de son expérience.
Je remercie mes parents Pauline et Thierry, ainsi que mes frères Félix, Julien, Benoît et Antoine pour leurs encouragements et leur support moral inconditionnel.
Je remercie ma conjointe Liliane pour ses judicieux conseils et pour m’avoir soutenu dans toutes les étapes de ce projet.
Je tiens finalement à remercier mon directeur de maitrise, Jean-Marc Mac-Thiong pour son dynamisme inépuisable et pour l’encouragement au dépassement continuel de soi.
Introduction
La lésion médullaire traumatique (LMT) est dévastatrice, tant au plan physiologique, que fonctionnel et social. La compression de la moelle épinière interrompt la perception sensorielle et le contrôle moteur distaleguement à la lésion. Une perte de fonction des sphincters, de la marche, de la préhension et des muscles respiratoires peut survenir immédiatement suite au trauma. Après une période de quelques mois durant laquelle la récupération neurologique est possible, l’incapacité résiduelle perdurera pour le restant de la vie de l’individu. Elle s’accompagne d’un risque élevé de complications urinaires, cutanés et respiratoires qui entrainent une diminution de la qualité de vie et de l’espérance de vie. Sans contredit, la LMT bouleverse la participation sociale des victimes avec des conséquences familiales, psychologique et financières majeures.
Malgré de nombreuses avancées médicales, beaucoup de chemin reste à faire pour améliorer la survie et la qualité de vie des victimes. La période post-traumatique immédiate semble cruciale pour le devenir à long terme. Une stabilisation médicale et une intervention chirurgicale rapide avec une prise en charge ciblée sur les risques de complications pourraient améliorer le devenir des traumatisés médullaires.
Cet ouvrage étudiera l’association entre le délai chirurgical (temps écoulé entre un traumatisme médullaire et la chirurgie) et le taux de complications. Plus spécifiquement, il présentera l’étude d’une cohorte de patients LMTs pris en charge à l’hôpital du Sacré-Cœur de Montréal. Deux articles concernant cette cohorte ont été publiés dans des revues révisées par des pairs. Ces articles sont présentés dans ce mémoire.
1. Considérations historiques
Le décryptage d’un papyrus datant de 3000 à 2500 avant Jésus-Christ par Edwin Smith relate la première mention connue de la LMT et de son traitement médical.1 La LMT y est décrite comme une affection qu’il vaut mieux ne pas traiter étant donné son sombre pronostic. Ce dogme de fatalité prédominera dans la culture médicale jusque dans les années 1940. Effectivement, l’histoire naturelle de la LMT comporte le risque de décès rapide par insuffisance respiratoire, une récupération neurologique imprévisible et une fin de vie précoce quasi inévitable en raison d’infections urinaires ou respiratoires.
Dans la Grèce antique, Hippocrate décrit une technique de réduction fermée et fut le premier à traiter des complications secondaires, notamment des plaies de pression. Au 2ème siècle, Galéen est le premier à reconnaitre des patrons spécifiques de paralysie selon le niveau de transsection médullaire.2
Au 7ème siècle après JC, le chirurgien byzantin Paul d’Égine décrit la première chirurgie de décompression et de laminectomie pour la LMT. L’importance du délai d’intervention est soulevée pour la première fois par le médecin italien Roland de Parma en 1210. 3
Au début du 19ème siècle, une nouvelle controverse apparaît dans la communauté médicale. Les mérites de la décompression de la moelle épinière et de la laminectomie sont débattus par les chirurgiens britanniques Sir Astley Cooper et Charles Bell. Le développement de l’anesthésie, de l’asepsie, des transfusions sanguines et de l’imagerie médicale au courant du 19ème siècle rend la chirurgie spinale de plus en plus acceptable pour les LMTs.
3
Avec la première guerre mondiale, le développement d’unités de traitement spécialisées en LMT est instauré afin de répondre provisoirement à l’explosion du nombre de victimes. En 1916, George Riddoch, de la Grande-Bretagne, constate un taux de survie en phase aiguë qui passe de 10 % à 90% après l’instauration d’une unité de réadaptation de LMTs.
Les premières unités de traitement permanentes sont instaurées par Donald Munro en 1936 à Boston aux États-Unis et par Sir Ludwig Guttman au Royaume-Uni en 1944. Avant la deuxième guerre mondiale, l’espérance de vie des victimes de LMT est de quelques semaines alors qu’après la deuxième guerre, elle se trouve augmentée de 10 ans avec l’amélioration de la prévention des complications urinaires, respiratoires et cutanées. L’espérance de vie et la qualité de vie continueront de s’améliorer tout au long du 20ème siècle. Au cours des années 1980, les progrès de l’instrumentation chirurgicale avec Cotrel et Dubousset rendent plus acceptable la chirurgie de décompression extensive. L’instabilité de la biomécanique vertébrale suite à une décompression chirurgicale peut maintenant être compensée par une instrumentation rigide qui stabilise des segments de la colonne. Malgré une effervescence autour des thérapies neuroprotectrices et de multiples larges études cliniques sur le sujet, aucune thérapie n’a démontré son efficacité à améliorer de façon significative le pronostique neurologique chez les humains jusqu’à ce jour. 3, 4
L’histoire a donné tort au fatalisme longuement véhiculé au sujet des LMTs. Cette perspective historique met en valeur la pertinence de la recherche d’interventions novatrices visant à améliorer le pronostic et la qualité de vie des personnes souffrant de LMTs. Notre projet de recherche s’inscrit dans la quête visant à déjouer l’histoire naturelle catastrophique de la LMT.
2. Anatomie, physiologie et corrélation clinique
La compréhension de l’anatomie et de la physiologie de la colonne vertébrale nous permet de comprendre l’impact de la lésion médullaire. Ce paragraphe résume les connaissances fondamentales pour comprendre les phénomènes discutés dans le cadre de ce mémoire.
2.1 L’Anatomie de la colonne vertébrale
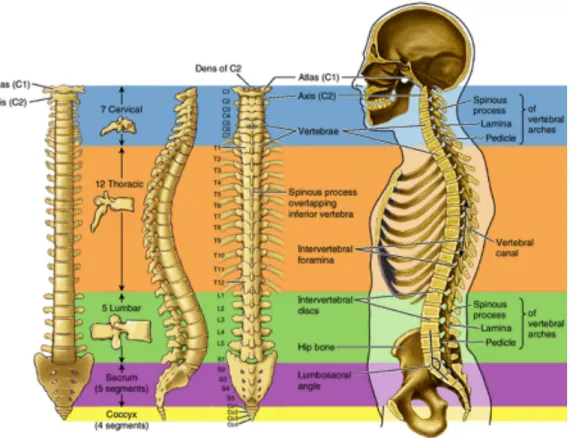
La colonne vertébrale est une structure segmentée constituée d’une série de vertèbres osseuses reliées par des structures ligamentaires et disques intervertébraux. On compte généralement 29 vertèbres : 7 vertèbres cervicales, 12 thoraciques, 5 lombaires et 5 sacrées fusionnées.
5
Figure 1 Représentation schématique de la colone vertébrale dans son ensemble avec 7 vertèbres cervicales, 12 thoracique, 5 lombaires, 5 sacrées et 4 coccygienne. Tiré de Clinically Oriented Anatomy, 5th, p479 5
Bien que chaque vertèbre possède des caractéristiques distinctes, elle présente un patron d’organisation général issu du développement embryologique. La portion antérieure de la vertèbre est appelée corps vertébral. Le corps vertébral est cylindrique et composé majoritairement d’os spongieux. Les corps vertébraux s’empilent successivement, séparés par des structures fibro-cartilagineuses appelées disques intervertébraux et connectées par les ligaments longitudinaux antérieurs et postérieurs.
Les éléments postérieurs de la vertèbre constituent une structure complexe composée majoritairement d’os cortical avec de multiples proéminences appelées apophyses. Les éléments postérieurs des vertèbres successives sont interconnectés à l’aide d’articulations
zygapophysaires, de capsules articulaires et de multiples ligaments reliant les apophyses osseuses.5
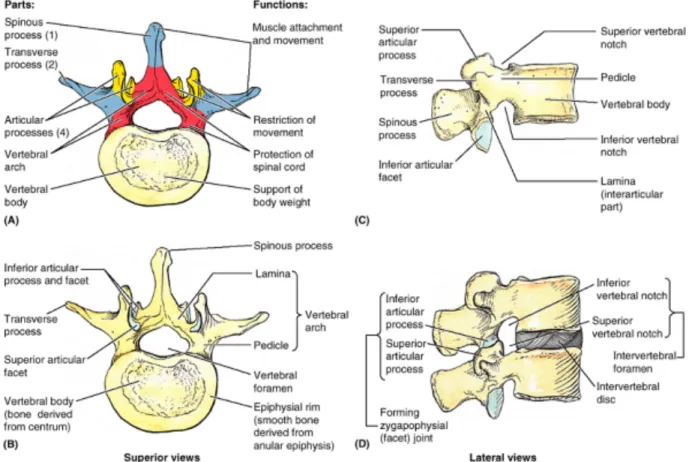
Figure 2 Représentation shématique des éléments osseux d’une vertèbre lombaire.Tiré de Clinically Oriented Anatomy,5th,p480 5
Les pédicules vertébraux sont des structures osseuses cylindriques reliant le corps vertébral aux éléments postérieurs. Corrélation clinique : les pédicules peuvent servir de points d’insertion pour du matériel orthopédique au niveau des vertèbres thoraciques et lombaires.
Les lames vertébrales constituent le recouvrement postérieur osseux de la moelle épinière et des méninges. Corrélation clinique : l’exérèse chirurgicale de la lame vertébrale
7
(laminectomie) est une procédure permettant de décomprimer la moelle épinière par une approche postérieure.
2.2 Physiologie de la colonne vertébrale
La colonne vertébrale a 3 rôles principaux : le support postural, la mobilité et la protection neurologique.
2.2.1 Support postural
Le support postural qui implique le support du poids des vertèbres supérieures et de la tête est principalement assuré par les corps vertébraux et les disques intervertébraux. Notons que les éléments postérieurs participent aussi au partage des forces compressives sur la colonne mais d’une façon moins importante. Normalement, les vertèbres s’alignent de façon rectiligne dans le plan coronal et adoptent des courbures harmonieuses dans le plan sagittal. Ceci permet le maintien d’un équilibre postural avec une dépense énergétique minimale. Corrélation clinique : un traumatisme vertébral peut perturber cet équilibre architectural et entrainer des déformations vertébrales aux conséquences fonctionnelles catastrophiques.
2.2.2 Mobilité vertébrale
La deuxième fonction fondamentale de la colonne vertébrale est la mobilité. Les muscles para-spinaux s’insèrent sur les éléments postérieurs des vertèbres. Leur contraction spécifique entrainera un mouvement de flexion, extension, flexion latérale et rotation. Les ligaments et disques intervertébraux s’étirent et génèrent une force tensile et une élasticité
permettant un degré de mouvement physiologique entre les vertèbres. De plus, les articulations zygapophysaires sont recouvertes de cartilage hyalin permettant un mouvement de glissement. Le degré de mouvement entre chaque vertèbre contribue partiellement à une mobilité vertébrale globale permettant une fonction normale.
Corrélation clinique : Une lésion médullaire entraine une perte de contrôle des muscles stabilisateurs du rachis sous le niveau lésionnel. Cette atteinte musculaire peut se manifester en spasticité, raideur, faiblesse ou atonie musculaire et affecte la fonction du patient.
La fusion vertébrale chirurgicale entraine la formation d’un pont osseux entre plusieurs vertèbres qui sacrifie la mobilité d’un ou plusieurs segments vertébraux. Le mouvement compensatoire des segments adjacents permet au patient de maintenir une mobilité fonctionnelle adéquate. Un traumatisme qui déstabilise suffisamment un segment vertébral pour causer une lésion médullaire nécessite une fusion chirurgicale qui permettra la mobilisation du patient sans aggraver la compression médullaire.
2.2.3 Protection neurologique
Le troisième rôle de la colonne vertébrale est de protéger la moelle épinière et ses racines nerveuses. La moelle épinière est située dans une cavité cylindrique osseuse appelée le canal spinal. Le corps vertébral, les pédicules et les lames vertébrales forment une arche osseuse continue autour de chaque segment de moelle épinière. La superposition de ces arches osseuses constitue le canal spinal. Latéralement au canal spinal, les foramen intervertébraux se succèdent et constituent le point de sortie des racines nerveuses à chaque niveau.
Corrélation clinique : la conséquence la plus tragique du traumatisme vertébral est la perte de protection neurologique et la lésion associée de la moelle épinière due à un rétrécissement
9
ou une déformation du canal spinal. La compression de la moelle peut survenir par une amplitude de mouvement extra physiologique ou par la migration d’un fragment osseux, ligamentaire ou discal dans le canal spinal. Un trauma pénétrant par balle ou par objet tranchant peut aussi entrainer une lacération du contenu neurologique rachidien. Un traumatisme neurologique iatrogénique est une complication hautement redoutée par les chirurgiens spinaux. Le mécanisme de trauma peut être une compression/lacération malencontreuse, le mal-positionnement d’implants, la formation d’un hématome post-opératoire ou l’étirement excessif du tissu neurologique lors de la correction d’une déformation posturale. Mentionnons que des lésions d’étiologie infectieuse, néoplasique ou inflammatoire peuvent aussi compromettre la protection du contenu neurologique rachidien.
2.3 Anatomie et physiologie de la moelle épinière
Nous avons décrit la structure ostéo-ligamentaire de la colonne vertébrale. Nous décrirons maintenant l’anatomie et la physiologie de la structure qu’elle protège : la moelle épinière.
2.3.1 Segments médullaires
La moelle épinière est divisée anatomiquement en 8 segment cervicaux (dénotés C1 à C8), 12 thoraciques (T1 à T12), 5 lombaires (L1 à L5) et 5 sacrés (S1 à S5). Elle s’étend habituellement du foramen magnum jusqu’à la première ou deuxième vertèbre lombaire, où elle se termine en cone medullaire.
Figure 3 Illsustration du tissus neurologique protégé contenue dans le rachis soit : la moelle épinière, le cone médullaire, la queue de cheval et les racines.Tiré de Clinically Oriented Anatomy,5th edition, p5225
11
Caudalement à la deuxième vertèbre lombaire, le canal spinal contient seulement les racines nerveuses des niveaux vertébraux inférieurs qui forment ce que nous appelons communément la queue de cheval en raison de leur apparence filamenteuse.
La moelle épinière est divisée en segments responsables d’un territoire musculaire et sensitif prédictible. Par exemple, le muscle respiratoire du diaphragme est innervé par les niveaux cervicaux C3, C4 et C5, les membres supérieurs sont majoritairement innervés par les racines C5 à T1, les muscles abdominaux sont innervés par les niveaux T7 à T11, les membres inférieurs sont innervés par les niveaux lombaires L2 à S2 et les sphincters urinaires et anaux sont innervés par les racines sacrées S3 à S5.
Corrélation Clinique : l’échelle de l’American Spinal Cord Injury Association (ASIA : voir Annexe 1) est largement acceptée par les cliniciens et scientifiques pour décrire la sévérité et le niveau de la lésion médullaire. La sévérité de la lésion se décline en 5 grades ASIA : A,B,C,D et E. Le grade ASIA A représente une lésion complète sensorimotrice alors que le grade ASIA E représente une fonction sensorimotrice normale. L’échelle ASIA sert aussi de référence pour les muscles et territoires sensitifs clés des segments médullaires permettant de déterminer le niveau d’atteinte médullaire.6, 7
Pour chacun des segments, des racines ventrales (motrices) et dorsales (sensitives) sortent de la moelle vis-à-vis les cornes antérieures et postérieures de la substance grise médullaire (Figure 4). Les racines nerveuses font partie du système nerveux périphérique et non du système nerveux central comme la moelle épinière et le cerveau.
Figure 4 Les racines nerveuses et un segment de la moelle épinière. Tiré de Fundamental anatomy, 1rst edition p2028
2.3.2 Voies sensitives et motrices
La moelle épinière assure la connexion neurologique motrice, sensorielle et autonome entre l’ensemble du corps et le cerveau. Les multiples voies motrices et sensitives représentent un regroupement de fibres nerveuses ayant un parcours et une fonction similaire. Une coupe transverse de la moelle démontre l’organisation des voies sensitivomotrices décrite ici-bas et permet de mieux comprendre la présentation clinique des lésions médullaires.
13
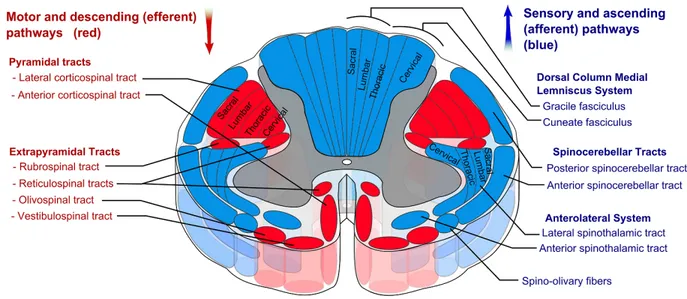
Figure 5 Coupe transverse dépitant les voies afférentes et afférente de la moelle épinière cervicale. Tiré de http://en.wikipedia.org/wiki/Spinal_tracts#Structure9
Les voies cortico-spinale, antérolatérale, ainsi que celle des cordons postérieurs méritent une attention particulière.
La voie cortico-spinale est composée de motoneurones supérieurs dont le corps neuronal origine du cortex moteur. Les motoneurones projettent leur axone à travers la substance blanche de la moelle épinière. La décussation axonale s’effectue au niveau des pyramides du bulbe rachidien. Le motoneurone supérieur fera synapse avec le motoneurone inférieur au niveau de la corne antérieure de la matière grise. Le motoneurone inférieur projettera son axone dans la racine nerveuse qui constituera le nerf périphérique pour permettre le contrôle musculaire.
Il existe deux voies sensitives médullaires majeures : la voie antérolatérale spino-thalamique et la voie des cordons postérieurs. Ces deux voies reçoivent les influx sensitifs du
système nerveux périphérique et les acheminent vers le thalamus. Elles se différencient par leur fonction et leur trajet dans la moelle épinière.
Les neurones de la voie antérolatérale spino-thalamique sont responsables de la transmission de la nociception et de la thermoception. La décussation de leurs fibres se fait au niveau du segment médullaire à travers la commissure grise puis les fibres suivent un trajet ascendant via la voie antérolatérale jusqu’au thalamus.
La voie des cordons postérieurs transmet les influx proprioceptifs et les influx du toucher léger. Ces fibres voyagent au niveau des colonnes dorsales et elles font synapse au niveau du tronc cérébral avant de décusser et emprunter le faisceau du lemniscus médian jusqu’au thalamus.
Corrélation Clinique : une lésion postérieure de la moelle épinière altère la proprioception et le toucher fin alors qu’une atteinte antérieure se manifeste par une atteinte motrice thermoceptive et nociceptive plus marquée. Une hémisection de la moelle se manifeste par le syndrome de Brown-Sequard, soit une perte de sensibilité fine, de proprioception et de motricité fine du côté ipsi-latéral à la lésion et une perte de la nociception et de la thermoception controlatérale à la lésion.
Les voies motrices et sensitives de la moelle adoptent une disposition somatotopique prévisible (Figure 5). Les axones situés en périphérie innervent les segments médullaires associés au plancher pelvien et aux membres inférieurs alors que les axones situés plus centralement innervent les segments médullaires associés aux membres supérieurs. Cette disposition explique qu’une lésion centrale de la moelle épinière cervicale se manifeste le plus souvent en déficit des membres supérieurs en épargnant la fonction des membres inférieurs (syndrome centromédullaire).
15
2.3.3 Fonctions médullaires autonomes et réflexes médullaires
Le système nerveux autonome contrôle les mécanismes viscéraux autonomes. Il a un rôle important dans le contrôle des systèmes cardio-vasculaire, respiratoire, digestif, génito-urinaire et cutané. Il est divisé en système sympathique, responsable de la réponse au stress et parasympathique, responsable de la détente et de la digestion. Les fibres nerveuses sympathiques proviennent des niveaux thoraciques alors que les fibres parasympathiques proviennent du tronc cérébral et des niveaux sacrés de la moelle épinière.
Corrélation clinique : La régulation inadéquate de la tension artérielle suivant la lésion médullaire peut contribuer aux épisodes d’hypotension orthostatique (associé aux changements de position). Le terme dysréflexie autonomique décrit la survenue d’élévation brusque et intense (>20%) de la tension artérielle systolique en réponse à un stimulus nociceptif (par exemple une infection urinaire) sous un niveau lésionnel cervical ou thoracique haut. Cette hypertension subite s’accompagne d’hypersudation, de piloérection, de flushing facial, de céphalée, de vison embrouillée et de congestion nasale.
La moelle épinière est un centre de réflexes majeur avec différents niveaux de complexité. L’étirement tendineux rapide entraine une connexion synaptique médullaire directe du neurone propriocepteur sur le motoneurone inférieur innervant le muscle.
Corrélation Clinique : Une lésion médullaire aboli la modulation corticale des réflexes médullaires inférieurs à la lésion. Cela résulte en une hyper-réflexie et une spasticité. Toutefois, ces phénomènes peuvent être absents initialement en raison d’un phénomène appelé choc spinal. Le choc spinal constitue une inhibition généralisée de la moelle épinière caudale à la lésion. Ceci se manifeste par une paralysie flasque et une aréflexie. Le choc spinal survient immédiatement après la lésion et peut durer de quelques heures à quelques jours.
Dans la période immédiate suivant le trauma médullaire, il est parfois impossible de statuer sur l’atteinte médullaire tant que le choc spinal n’est pas résolu. Le réflexe bulbo-caverneux est le plus caudal de la moelle épinière. Il n’a donc aucune chance d’être affecté par une lésion médullaire sauf pendant le délai du choc spinal. Pour cette raison, le réflexe bulbo caverneux est évalué pour déterminer si le choc spinal est résolu.
En résumé, la colonne vertébrale est une structure ostéo-ligamentaire complexe, à la fois solide et flexible, contribuant à la posture et à la protection de la moelle épinière. Une lésion de la moelle épinière se manifeste par une atteinte motrice, sensitive et autonomique dans un territoire spécifique déterminé par le segment de moelle épinière lésé.
3. Mécanismes pathologiques cellulaires et moléculaires de
la lésion médullaire
Une lésion à la moelle épinière implique un bris de la continuité des éléments cellulaires et tissulaires de la moelle épinière. Un traumatisme implique un transfert d’énergie cinétique dans la colonne vertébrale qui surpasse la capacité physiologique de l’os, des ligaments et des disques intervertébraux. La colonne vertébrale devenue instable ne protège plus la moelle épinière.
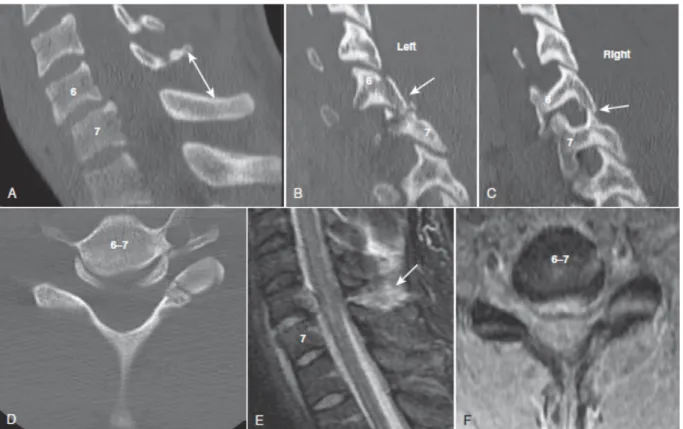
Figure 6. Modalités radiologiques démontrant un trauma médullaire secondaire à une fracture-luxation C6-C7. Les Tiré de The Spine, 6th edition, p135010
Selon l’importance du traumatisme, les tissus ostéoligamentaires peuvent oblitérer partiellement ou complètement le canal médullaire. Ceci entraine une compression, une
contusion ou transsection du tissu médullaire. Ce phénomène est appelé lésion primaire, par opposition à la lésion secondaire. La lésion secondaire est un concept impliquant des évènements délétères survenant à retardement par rapport au traumatisme initial. Les mécanismes identifiés dans la lésion secondaire impliquent des phénomènes vasculaires et la relâche de glutamate, de radicaux libres et de calcium.11, 12 Ces phénomènes ont des répercussions d’ordre moléculaire cellulaire et histologique. Beaucoup d’énergie est déployée dans la recherche scientifique afin de minimiser la lésion secondaire. La cible de plusieurs traitements en investigation est d’intervenir sur les mécanismes de la lésion secondaire.13, 14 Notamment, plusieurs études sur des modèles animaux divers ont démontré qu’un délai de décompression court suivant la contusion médullaire diminuerait la lésion secondaire et améliorerait donc la récupération neurologique.15-25 Ce sont ces études qui sont la principale base scientifique permettant de justifier un délai chirurgical court en clinique.
4. Épidémiologie et impact socioéconomique
Malgré un faible taux d’incidence, la LMT a un profil démographique particulier qui implique des conséquences socioéconomiques majeures. Ce chapitre résumera les connaissances sur les données démographiques, épidémiologiques et socio-économiques les plus récentes. De façon stéréotypée, la LMT survient chez deux populations distinctes : les patients jeunes et les patients âgés. La population plus jeune est majoritairement masculine, victime d’accident de la route ou de sport, chez qui nous retrouvons plus souvent des paraplégies et des lésions complètes. Chez les patients plus âgées, la proportion de femme est plus importante, plus souvent victime de chute qui engendre une tétraplégie incomplète. La réalité est néanmoins beaucoup plus nuancée que ce portrait simplifié.
4.1 Incidence et prévalence
L’incidence mondiale des LMTs varie entre 10 et 60 cas par million d’habitants par année selon la région étudiée.26 Au Canada, l’incidence des LMTs a été estimée par Noonan et al27 en 2010 à 41 cas par million d’habitants. L’incidence des lésions médullaires non
traumatiques serait de 68 par million d’habitants. Pirouzmand a décrit l’incidence de LMTs dans une population de patients traumatisés du centre spécialisé de trauma Sunnybrook en Ontario entre 1986 et 2006.28 Parmi les patients traumatisés, 23,2% avaient un trauma spinal, 5,4% avaient une LMT et 3,0% avaient une lésion complète. Dans l’étude de Lenehan et al, l’incidence de la LMT en Colombie-Britanique a été établie à 37,5 cas par million par année et n’aurait pas varié significativement entre 1995 et 2004.29
La prévalence de lésion médullaire dans la population active est influencée par l’amélioration de la survie des patients avec LMT. Une revue des études publiées entre 1995 et 2005 suggère que la prévalence varie entre 223 et 755 (485) cas par million d’habitants.26 Basé sur l’estimation actuarielle de Noonan et al, 85 556 canadiens vivaient avec les séquelles d’une LMT.27
L’âge moyen des patients au moment de leur trauma varie entre 33 et 50 ans selon les études canadiennes.27-31 C’est chez les patients de 15 à 24 ans que l’incidence de LMTs est la plus importante, suivi des patients de plus de 65 ans. Les données démographiques canadiennes collectées depuis les dernières décennies démontrent un vieillissement de l’âge au moment du traumatisme qui va de pair avec le vieillissement général de la population.28-30 Environ 3 fois plus d’hommes que de femmes subissent une LMT. Cette proportion est encore plus importante chez les jeunes et s’atténue chez les patients plus âgés. Toutefois plusieurs études démontrent que cette proportion est demeurée inchangée au courant des dernières décennies.28, 29, 32
4.2 Étiologie de la LMT
L’étiologie principale de la LMT demeure les accidents de véhicules motorisés (35 à 57%), suivi des chutes (19 à 31%), des sport (10 à 18%), et des actes violents (2 à 18%).28, 29, 32, 33 Les accidents de véhicules motorisés frappent particulièrement la tranche d’âge plus
jeune de 16 à 45 ans, alors que les chutes frappent plus les personnes âgées de plus de 50 ans.28, 31-33 Au courant des dernières décennies plusieurs auteurs ont observé une augmentation des chutes comme étiologie des LMTs, phénomène allant de pair avec le vieillissement de la population.28, 32, 33
21
4.3 Niveau de la lésion
Lorsqu’on parle de localisation de la lésion, il faut distinguer le niveau du traumatisme vertébral du niveau médullaire. Le niveau de la lésion est décrit en spécifiant le dernier niveau normal au niveau neurologique ou en utilisant la dénotation paraplégie ou tétraplégie. Pour cette discussion, nous emploierons le niveau médullaire comme référentiel. Plus une lésion est située à un niveau élevé, plus la perte de fonction sera importante puisque le nombre de muscles atteints sera plus significatif et qu’il y aura plus de risques d’atteinte des membres supérieurs et de la musculature respiratoire.
Le taux de lésions cervicales (par opposition à thoracique et lombaire) varie selon les populations étudiées de 29% à 75% et se situe généralement autour de 50%.28, 29, 31, 33 Dans
une étude sur l’ensemble de la population albertaine, Dryden et al ont établi à 54,1% le taux de tétraplégie par rapport à 45,9% de paraplégie.31 Cette étude souligne que la majorité des LMTs décédées sur les lieux de l’accident ont souffert de lésions cervicales hautes (de C1 à C4). Les victimes plus jeunes souffrent plus souvent de paraplégie alors que chez les plus âgées, nous retrouvons d’avantage de tétraplégie.29, 31 Les actes de violence sont fréquemment la cause de
paraplégie plus que de tétraplégie.31, 32 De plus, les patients souffrant de paraplégie ont plus souvent une atteinte médullaire complète alors que la tétraplégie est plus souvent associée aux lésions incomplètes.
Parmi la population de la Colombie-Britanique étudiée de 1995 à 2004, la distribution du niveau de la lésion se situe à C1-C4 chez 10,4% des patients; à C5-C7 chez 34,7% des patients; au niveau thoracique chez 24,5% des patients; au niveau lombosacrée chez 20,9% des patients et est non spécifié dans 9,5% des cas. 29 Plus les patients sont âgés, plus leur risque de lésion cervicale est élevé. Par exemple, chez les patients de moins de 50 ans, 80%
souffriront de paraplégie (par rapport à 20% de tétraplégie) alors que cette proportion chute à 50% chez les 50 à 74 ans et à 20% chez les plus de 75 ans. Chez les personnes âgées de plus de 75 ans, il semble que la présence de lésion cervicale haute (C1 à C4) soit encore plus importante.29, 33
4.4 Sévérité de la lésion
Il y aurait une grande variation de proportion de lésion complète (ASIA grade A) selon la population étudiée. La plupart des études rapportent un taux de lésion complète de 45 à 50% parmi les LMTs.26, 29, 32 Parmi tous les patients référés au centre tertiaire de Colombie-Britanique, la distribution de la sévérité de la lésion démontrait 45,3% de ASIA A; 9,3% de ASIA B; 13,3% de ASIA C; 24,7% de ASIA D; 5,2% de syndromes de la queue de Cheval et 2,3% d’atteintes neurologiques non spécifiées.
4.5 Lésions associées
Un traumatisme vertébral peut survenir de façon isolée mais survient fréquemment dans le cadre d’un polytraumatisme. On retrouve une association fréquente de TCC avec les traumatismes vertébraux cervicaux et les traumatismes thoraciques sont fréquemment associés aux fractures vertébrales thoraciques.34 Des fractures des os longs et des traumatismes abdominaux accompagnent fréquemment les LMTs.35 L’ISS est un indice de sévérité fréquemment utilisé pour décrire la sévérité des traumatismes. L’ISS est un score basé sur les régions anatomiques principales, soit : la tête et le cou, le visage, les extrémités, le thorax l’abdomen, la ceinture pelvienne et les surfaces externes. À chaque région est attribué un score de 0 à 5 et le score des trois régions les plus sévèrement atteintes est mis au carré et additionné
23
pour un score global de 0 à 75. L’ISS moyen associé aux LMTs dans la littérature varie de 10 à 40 en raison des critères de sélection différents d’une étude à l’autre.36-41
4.6 Survie durant la phase aiguë
Malgré les avancements de la médecine moderne, un risque de décès durant la phase d’hospitalisation aiguë demeure présent. Une étude sur la population de la Caroline du Sud de 1993 à 2003 a trouvé un taux de décès aussi élevé que 13% durant la phase d’hospitalisation aiguë.42 Les facteurs de risque identifiés pour le décès en phase aiguë sont : l’âge de plus de 20 ans, une lésion cervicale haute, la sévérité de l’atteinte neurologique, la présence d’au moins une comorbidité médicale et la présence d’un TCC sévère. 42, 43 Le traitement dans un centre de trauma de niveau 1 a aussi été identifié comme un facteur de risque pour le décès en phase aiguë mais un biais de référence altère cette observation puisque ces patients sont plus souvent polytraumatisés.
4.7 Espérance de vie
Après avoir survécu à la phase aiguë, les patients avec LMT en phase chronique courent un risque de décès secondaire aux complications respiratoires, urinaires et cardiovasculaires.44 Une étude australienne de 1998 comparant l’espérance de vie des LMTs à
celle de la population générale estimait l’espérance de vie des LMTs tétraplégiques complètes à 70% de la moyenne, celle des paraplégiques complètes à 84% et celle des patients avec une motricité fonctionnelle à 90% de la moyenne.45 Un âge avancé et un niveau neurologique plus proximal sont des prédicteurs de décès reconnus dans la population de LMTs chroniques.44
4.8 Impact financier
Le coût social d’une LMT est considérable en raison des frais hospitaliers, des frais de réhabilitation et de la perte de participation sociale et professionnelle. Dryden a estimé le coût des soins de santé suivant une LMT en dollar canadien en se basant sur la population albertaine.46 Selon cette étude, le coût moyen lié aux soins de santé pour une LMT complète
serait de 121 600 $ la première année puis de 5 400 $ pour les années subséquentes. Pour une lésion incomplète le coût serait de 42 100 $ la première année puis de 2 800$ par année subséquente. Selon Winslow et al, la majorité des coûts et la durée de l’hospitalisation aiguë sont engendrées par les complications respiratoires.47 Dans une récente étude menée à l’Hôpital du Sacré-Cœur de Montréal une chirurgie dans un délais de moins de 24 heure était associée à une diminution des coûts d’hospitalisation en phase aiguë.48
4.9 Participation professionnelle
L’objectif final de la réadaptation après la LMT est le retour à la participation à la vie active. Dans la littérature américaine, nous observons que 21% à 67% des patients ne retourneraient pas au travail après une LMT.49
Une méta-analyse d’études entre 1992 et 2005 suggère que, en Amérique du nord, seulement 30% des blessés médullaires retournaient au travail alors que cette proportion atteignait 50% en Europe. Cet écart serait possiblement attribuable aux différentes politiques de réinsertion au travail.50 Les facteurs identifiés favorisant le retour au travail seraient: un plus jeune âge, un degré de scolarisation plus avancé, une bonne santé générale, une lésion moins sévère, des incitatifs financiers et des mesures institutionnalisées de réintégration. La race demeure un
25
sujet de controverse quant à sa valeur comme facteur pronostique de retour au travail. Il est à noter que le délai de retour au travail peut être ralenti par des besoins de réinsertion dans un nouveau milieu, spécialement pour les travailleurs manuels. Une étude récente dénote un délai médian de 539 jours avant le retour aux activités productives et un délai médian de 660 jours avant le retour au travail.51
5. Implications cliniques suivant la lésion médullaire
5.1 Récupération neurologique
Les études sur l’évolution naturelle des LMTs ont démontré qu’une récupération spontanée est possible surtout dans les premiers mois suivant la lésion médullaire. Toutefois, le corps médical demeure confronté à l’absence de modalités prouvées efficaces pour améliorer la récupération neurologique.
Il est capital de distinguer la récupération neurologique de la récupération fonctionnelle.52 La récupération neurologique dépend de la ré-innervation de groupes musculaires et territoires sensitifs. L’échelle de gradation du ASIA permet la gradation de la sévérité de l’atteinte neurologique de A à E (Annexe 1). La gradation ASIA A représente une lésion avec interruption complète des fonctions sensorimotrice sous lésionnelles alors que ASIA E signifie une fonction sensorimotrice normale. Une lésion complète ASIA A est déterminée par l’évaluation sensorielle et motrice du segment médullaire le plus distal, soit la
sensation rectale profonde et la contraction volontaire du sphincter anal. Zariffa et al53 soulignent qu’une faible proportion de patients (3,4%) peut avoir une préservation des fonctions motrices sous lésionnelles correspondant à un niveau fonctionnel (ASIA D) bien qu’ils soient catégorisés ASIA A en raison de l’absence de fonction et de sensation au niveau péri-anal. Il est donc possible d’avoir une fonction motrice et sensorielle aux membres inférieurs malgré une lésion ASIA A affectant majoritairement le sphincter anal. Les scores ASIA sensitifs et moteurs constituent la somme numérique des niveaux complètement ou partiellement préservés. L’échelle de gradation ASIA est largement inspirée de son prédécesseur, l’échelle de Frankel.44 La récupération fonctionnelle représente plutôt la capacité de l’individu à accomplir une tâche de la vie quotidienne. Le Functionnal Independance Measure (FIM) et le Spinal Cord Injury Independence Measure (SCIM) sont des outils mesurant le degré de récupération fonctionnelle.
Toutefois, la récupération neurologique (ie échelle ASIA) demeure l’outil le plus utilisé dans les études sur les LMTs.54-58
5.1.2 Évolution neurologique naturelle
Afin de déterminer l’évolution neurologique naturelle des LMTs, Fawcett et al56 ont réalisé une revue de 7 essais cliniques randomisés avec placébo et ont cumulé les observations sur la récupération neurologique des patients ayant reçu un placébo. Toutes les études suggéraient un taux de conversion considérable du grade ASIA durant la première année suivant le traumatisme. Le taux de conversion semblait grandement influencé par le degré de lésion initiale. Une amélioration d’au moins un grade ASIA, soit 20% de conversion, était notée chez les personnes ASIA A. Toutefois, seulement 10% retrouvent un certain niveau de
27
fonction motrice (ASIA C) dans cette population. Chez les ASIA B, nous retrouvions un taux de conversion de 80%, dont 40% vers un niveau ASIA D.59, 60 Cette étude suggère que le niveau lésionnel affecterait aussi la récupération neurologique puisque les LMTs paraplégiques avaient un potentiel de récupération inférieur au tétraplégique. Cette observation découlerait probablement d’un canal médullaire plus étroit et une vascularisation plus précaire au niveau thoracique par rapport aux niveaux cervicaux et lombaires. Une étude récente suggère que les patients avec lésion ASIA A thoracique haute (entre T2-T5) auraient un taux de conversion inférieur à ceux avec lésion thoracique moyenne (T6-T10) et basse (T10-12).53
La revue de Fawcett et al suggère que 80% de la récupération neurologique survient généralement dans les 3 premiers mois suivant le traumatisme et semble se stabiliser à 12 mois. À noter qu’un faible pourcentage de patients aurait une amélioration neurologique même après 1 an.
Au delà du grade ASIA, le score ASIA sensitif et moteur (sur 100 points) a été utilisé afin d’avoir une idée plus précise du volume lésionnel. Ce score est particulièrement intéressant pour les lésions cervicales. Pour les lésions ASIA A cervicales, plusieurs études montrent une amélioration naturelle de 10 à 14 points plafonnant à un an. Pour les LMTs incomplets, cette amélioration serait entre 30 et 50 points.
Plusieurs études ont examiné les indicateurs de récupération fonctionnelle chez les LMTs. Selon l’étude de Wilson et al, sur une cohorte de 396 patients LMT,61 l’indépendance fonctionnelle à un an post trauma était prédite par : le grade ASIA, un score ASIA>50, l’âge au moment du traumatisme et la présence d’œdème ou d’hémorragie médullaire à l’IRM. Dans leur échantillon, 39,4% des patients atteignaient une indépendance fonctionnelle un an
après le trauma. Van Middendorp et al62 ont présenté un modèle de prédiction simple de marche autonome un an post trauma. Ce modèle est basé sur l’âge (≥65ans ou <65ans) et la fonction sensitive et motrice segmentaire L3 (quadriceps) et S1 (fléchisseurs plantaires) présente initialement suite au trauma. Leur modèle simple a démontré une excellente capacité de discrimination lors de sa validation dans un groupe prospectif indépendant de 99 patients LMT.
Plusieurs interventions visant à favoriser la récupération neurologique ont été étudiées avec des stratégies visant la neuro-protection ou la neuro-régénération. Notamment les stéroïdes à haute dose (Étude NASCIS II et III),54, 55 le GM-1 Ganglioside (Sygen),63 les anticorps anti
Nogo et les antagonistes des récepteurs NMDA. Pour le moment aucune modalité thérapeutique n’est prouvée efficace pour favoriser la récupération neurologique.
5.2 Complications intra-‐hospitalières
Une lésion médullaire augmente fortement le risque de développer des complications non neurologiques de nature pulmonaire, cutanée et génito-urinaire. Ces complications constituent un facteur de risque de mortalité64 et de ré-hospitalisation.65 Historiquement, une lésion médullaire était inévitablement fatale en raison des complications non neurologiques.3
Aujourd’hui, bien que la prévention et la prise en charge contribuent à la meilleure espérance de vie des patients, les complications constituent la principale cause de décès dans cette population.64
29
5.2.1 Complications fréquentes
Les complications de nature pulmonaire, urinaire et cutanée sont les plus fréquentes suivant une LMT traumatique.
5.2.1.1 Complications pulmonaires
Le traumatisme médullaire prédispose aux complications pulmonaires en raison de multiples phénomènes : perte de fonction des muscles respiratoires, mouvement thoracique respiratoire paradoxal, rigidité de la cage thoracique, risque accru d’aspiration, hypersécrétion endo-trachéale, diminution de la fonction de toux, bronchospasme, atélectasie d’immobilisation, surcharge volumique lors de la réanimation initiale et présence d’un traumatisme thoracique associé.
Les complications pulmonaires sont les plus fréquentes avec une incidence variant de 36% à 83% durant la phase aiguë d’hospitalisation.66-68 Elles causeraient 80% des décès chez les blessés médullaires cervicaux lors de l’hospitalisation aiguë. Le coût et la durée de l’hospitalisation sont davantage expliqués par les complications pulmonaires que par le niveau de la lésion neurologique chez les LMTs cervicales.47 Les pneumonies et l’atélectasie sont les complications pulmonaires les plus fréquentes.
La pierre angulaire de la prise en charge pulmonaire des blessés médullaires est une toilette pulmonaire agressive avec lavage broncho alvéolaire au besoin. Des exercices de respiration à pression positive aident à prévenir l’atélectasie et une ventilation percussive intra pulmonaire diminue la rétention de sécrétions. Avec les lésions médullaires cervicales hautes, l’intubation est souvent indiquée dès le premier signe de détresse respiratoire. Pour les patients
ayant besoin d’intubation prolongée, la trachéostomie joue un rôle pour faciliter le sevrage respiratoire.
5.2.1.2 Complications urinaires
La physiopathologie des complications urinaires varie selon le niveau de la lésion médullaire. Une LMT au-dessus de la région sacrée isole les centres mictionnels sacrés des centres responsables de la coordination vésico-urétérale (au niveau pontique et cortical).69 Après une brève période d’aréflexie, l’absence de contrôle supérieur entraine une hyper-réflexie et un dys-synchronisme vésico-urétral. Les pressions de vidange et de remplissage de la vessie sont donc augmentées. À cela s’ajoute un risque plus élevé de reflux vésico-urétéral avec des lésions entre T10 et L2. Avec une lésion sacrée de la moelle épinière ou une lésion de la queue de cheval, la vessie devient complètement paralytique et atone. Toutefois la vessie est peu compliante au remplissage et de hautes pressions sont générées par de petits volumes urinaires. Ces anomalies expliquent l’augmentation drastique du risque d’infection urinaire suivant la lésion médullaire et ce risque sera d’autant plus élevé que la lésion sera sévère. Le facteur de risque d’infection urinaire le plus important est l’usage prolongé d’une sonde urinaire. En comparaison, l’usage de cathétérisation intermittente, d’un condom cathéter ou d’une sonde sus pubienne diminuent le risque de bactériurie chez les LMTs.69
Le foyer de sepsis le plus commun est d’origine pulmonaire lors de la phase aiguë d’hospitalisation et d’origine urinaire durant la phase de réadaptation chronique.70 Les infections urinaires expliquent 45% des sepsis et augmentent significativement le risque de décès chez les blessés médullaires . En moyenne, les patients avec LMT auraient 2,5 épisodes d’infection urinaire par année.71
31
L’infection urinaire est définie comme la présence de Bactériurie > 105 bactérie par ml associée à un épisode de fièvre et une atteinte physique telle la douleur, une augmentation de spasticité ou une sudation profuse.
Pour le traitement de l’infection urinaire chez le patient LMT, il est recommandé de traiter sur courte période de temps avec un antibiotique au spectre étroit et ciblé sur le pathogène. Il est aussi recommandé de changer le cathéter vésical permanent régulièrement ou d’adopter une stratégie de cathétérisme intermittent pour diminuer les volumes intra-vésicaux.
La définition de bactériurie a été établie par consensus à > 102 CFU par ml d’urine via cathéter vésical, > 104 CFU par ml dans un spécimen récolté au méat urinaire ou la présence de bactérie dans un spécimen de ponction sus pubienne.72
L’indication de traiter la bactériurie asymptomatique demeure un sujet de controverse. Malgré un consensus d’expert recommandant de ne pas traiter, plusieurs centres rapportent le traitement systématique de cette condition. Il a été noté que les LMTs avaient en moyenne 18,4 épisodes de bactériurie par année mais que seulement 10% de ces épisodes s’accompagnaient de fièvre.73 Les bactéries les plus souvent incriminées sont E.Coli, Klebsiella et une augmentation de l’incidence de Pseudomonas, Proteus et Serratia a été notée.74
5.2.1.3 Complications cutanées
L’incidence des plaies de pression durant la phase aiguë d’hospitalisation varie d’une étude à l’autre entre 4,6% et 57,1% et dépend beaucoup du niveau de spécialisation de l’unité d’hospitalisation.66, 67, 75-77
Les sites les plus fréquents sont les points de contact du corps avec le lit, soit le sacrum, les talons, l’occiput et les ischions. La pression exercée par le poids du corps s’oppose
à la pression hydrostatique vasculaire au niveau de ces points de contact avec le sol, ce qui diminue localement l’apport sanguin d’oxygène et de nutriment. De nombreux facteurs de risque ont été identifiés afin de prédire la survenue d’une plaie de pression dans la population hospitalière. L’altération de la sensibilité et de la motricité suivant la LMT prédisposent spécialement à la survenue de plaie de pression puisque le patient perd son mécanisme de détection et protection de la peau le plus fondamental. D’autres facteurs de risque dans la population hospitalière sont les comorbidités, l’état nutritionnel et le niveau cognitif des patients.78 La sévérité de la plaie de pression est généralement classifiée selon la profondeur de la plaie par le National Pressure Ulcer Advisory Staging System (NPUASS).
(Stade I : érythème local sans bris cutané, Stade II : perte partielle de l’épaisseur de l’épiderme ou du derme, Stade III : perte totale de l’épaisseur de la peau sans extension dans les fascia profonds, Stade IV : destruction extensive impliquant le muscles, l’os ou le tendon)79 L’étude de Idowu suggère que le manque de ressource et le délai de consultation dans un centre spécialisé augmente drastiquement le risque de plaie de pression.75 La prévention de la progression d’une plaie vers un stade avancé est possible avec des ressources adaptées à la population LMT. Cette prévention pourrait épargner au patient des traitements plus invasifs, une hospitalisation prolongée et un délai d’initiation de la réadaptation. Les stratégies de prévention de plaies sont la gestion des apports nutritionnels, le traitement des comorbidités médicales, l’usage d’une surface thérapeutique77 et la mobilisation fréquente par le personnel hospitalier.80 La majorité des plaies de pression apparaissaient dans les 30 jours suivant la LMT. Durant cette période, le risque accru d’aggravation neurologique, secondaire à l’instabilité de la lésion vertébrale, rend la mobilisation du patient particulièrement difficile. La chirurgie de stabilisation vertébrale a l’avantage de permettre la mobilisation rapide d’une
33
lésion vertébrale instable et donc, possiblement, causer une réduction du risque de plaies de pression.
5.2.1.4 Complications thromboemboliques
La LMT prédispose aux phénomènes thromboemboliques par l’augmentation de la stase veineuse (immobilisme), l’hypercoagulabilité (contexte de trauma) et le dommage endothélial fréquemment associé. Les études de surveillance systématiques par doppler chez les LMTs démontrent une incidence d’évènements thromboemboliques dépassant les 50%. Toutefois, moins de 20% des patients ont une répercussion clinique. Waring et Karunas ont étudié l’incidence clinique des embolies pulmonaires (EP) et thrombophlébites profondes (TPP) dans une cohorte prospective de 1419 patients atteints de LMT entre 1986 et 1989. Les auteurs ne font pas mention de l’usage de thromboprophylaxie. Leur étude suggère une incidence d’EP de 4,6% et de TPP de 14,5% durant la phase aiguë d’hospitalisation. Le décès suivant l’embolie pulmonaire survient chez 14% des patients quadraplégiques de plus de 40 ans et chez seulement 0,37% des patients paraplégiques de moins de 40 ans.81
Étant donné l’incidence majeure de TPP et d’EP dans la population de LMTs, une thromboprophylaxie avec héparine de bas poids moléculaire est recommandée pour toute la durée de l’hospitalisation aiguë.82 La durée de la thromboprophylaxie devrait s’étendre jusqu’à la fin de la réhabilitation, pour un minimum de 3 mois, à moins d’un risque de saignement majeur. La thromboprophylaxie mécanique avec bas compressifs ou à compression intermittente devrait être débutée dès que possible bien qu’elle ne doive pas être utilisée seule. Le filtre de la veine cave inférieure ne devrait pas être employé de façon systématique.
L’usage d’ultrason de dépistage n’est pas nécessaire de façon systématique mais pourrait avoir une utilité pour les patients pour qui la thromboprophylaxie a été retardée.83
5.2.1.5 Complications cardiovasculaires
La population de LMTs est à risque de complications cardiovasculaires, notamment la dysréflexie autonomique, les arythmies cardiaques et l’hypotension orthostatique.
La dysréflexie autonomique est une manifestation de la réaction anormale à un stimuli nocif sous le niveau lésionnel, le plus souvent une distension vésicale ou intestinale dont le patient n’a pas conscience. Les LMTs supérieures au niveau T6 peuvent présenter des épisodes d’élévation de tension artérielle systolique de plus de 20%, accompagnés d’autres signes ou symptômes d’hyperréactivité autonomique (hypersudation, pylo-érection, rhinorrhée, céphalée, vision embrouillée).
Les lésions cervicales et thoracique hautes privent le mécanisme de conduction intracardiaque de la régulation sympathique. Les troubles du rythme cardiaque, notamment la bradycardie sinusale, s’observent fréquemment durant les premières semaines suivant la LMT. Moins fréquemment, nous observons aussi des anomalies de repolarisation, des blocs auriculo-ventriculaires, des tachycardies supra-auriculo-ventriculaires, des tachycardies ventriculaires et des arrêts cardiaques.
L’hypotension orthostatique est fréquente durant la période d’hospitalisation aiguë et découlerait de la perte du tonus sympathique veineux sous lésionnel, de l’hypovolémie et du déconditionnement cardiovasculaire.
35
Le risque de survenue de ces complications justifie la prise en charge initiale des LMTs par les soins intensifs pour monitorer la thérapie vasopressive, l’usage de réplétion volumique intensive et l’administration de chronotropes.
5.2.2 Facteurs prédicteurs des complications intra hospitalières
La survenue de complications fait partie de l’évolution naturelle sans traitement de lésions médullaires. Toutefois, avec la prise en charge moderne, il devient essentiel d’identifier les patients à risque de complications pour mieux cibler les efforts de prévention. Claxton et al,43 ont étudié les facteurs de risque de mortalité chez 72 patients avec lésion médullaire cervicale entre 1981 et 1994. Ils ont identifié l’âge, le niveau neurologique et le GCS comme facteurs indépendants de prédiction de mortalité.
Wilson et al.67 ont effectué une sous-analyse de 411 patients avec LMT cervicale de la cohorte du STASCIS afin d’établir un modèle prédictif de complications durant la phase aiguë d’hospitalisation. Une sévérité plus importante au score ASIA, un mécanisme de trauma à haute énergie, l’âge et l’absence d’administration de Corticostéroïdes (CS) prédisaient la survenue de complications dans un modèle multivarié. Le délai chirurgical n’a pas été soulevé comme facteur prédictif dans cette étude.
Grossman et al.66 ont étudié la survenue de complications post-opératoires de tout type dans
une base de données de 315 patients avec LMT cervicale, thoracique et lombaire. Parmi tous les patients, 57,8% avaient au moins une complication. Cette proportion atteignait 84,1% chez les ASIA A, mais seulement 25,3% chez les ASIA D. Des études de régression ont identifié le grade ASIA, un traumatisme pénétrant, un GCS <8 points, la présence de traumatisme
thoracique et le tabagisme comme prédicteurs globaux de complications. Le niveau de la lésion cervical, l’âge, le sexe, les comorbidités et l’association d’un traumatisme abdominal ne démontraient pas une tendance significative à la prédiction de complications. L’impact du délai chirurgical n’a pas été adressé dans cette étude.
Dimar et al.84 se sont intéressés à la survenue de complications post-opératoires chez des patients avec traumatisme thoraco-lombaire dont la moitié étaient neurologiquement intacts. La présence de lésion neurologique, l’âge, la présence de comorbidités (CCI) et l’usage de CS à haute dose selon le protocole de NASCIS II prédisaient la survenue de complications dans un modèle multivarié. Le délai chirurgical de plus de 72h ne prédisait pas la survenue de complications dans cette population.
Mc Henry et al.85 ont examiné rétrospectivement 1042 fractures thoraciques et lombaires d’une base de données afin de déterminer les prédicteurs d’insuffisance respiratoire. Environ 30% de ces patients avaient une lésion neurologique. Les patients ayant développé une insuffisance respiratoire étaient plus âgés, avaient un traumatisme plus sévère, plus de traumatismes thoraciques associés et un délai chirurgical plus long. Un âge de plus de 35 ans, un ISS >25 points, un GCS<12 points, un traumatisme thoracique et un délai chirurgical > 2 jours prédisaient le risque d’insuffisance respiratoire dans un modèle multivarié.
À l’opposé Aarabi et al.86 ont étudié 86 patients avec LMT (cervicale, thoracique et lombaire) et n’ont identifié que le grade ASIA comme prédicteur significatif de la survenue de complications pulmonaires. La petitesse de leur échantillon pourrait expliquer l’absence de détection d’autres facteurs prédictifs significatifs.
Lee et al.87 ont révisé 1591 cas de chirurgies spinales diverses afin de déterminer les facteurs de risque de complications avec un suivi minimal de 2 ans. Bien que non applicable à la