HAL Id: dumas-02445833
https://dumas.ccsd.cnrs.fr/dumas-02445833
Submitted on 20 Jan 2020
HAL is a multi-disciplinary open access archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Cartographie des risques en stérilisation : utilisation
d’un nouvel outil avant l’ouverture d’un bâtiment dédié
à la chirurgie
Camille Baronnet
To cite this version:
Camille Baronnet. Cartographie des risques en stérilisation : utilisation d’un nouvel outil avant l’ouverture d’un bâtiment dédié à la chirurgie. Sciences pharmaceutiques. 2019. �dumas-02445833�
UNIVERSITE DE ROUEN NORMANDIE
UFR SANTE – Département PHARMACIE
Année 2019
N°
MEMOIRE DU DIPLOME D’ETUDES SPECIALISEES DE PHARMACIE
option PHARMACIE HOSPITALIERE – PRATIQUE ET RECHERCHE
Conformément aux dispositions de l’arrêté du 8 avril 2013 tient lieu de
THESE
pour le DIPLOME D’ETAT DE DOCTEUR EN PHARMACIE
Présentée et soutenue publiquement le
par
Baronnet Camille
Né(e) le 18/05/1991
à Paris 14
èmePrésident du jury : Pr Rémi Varin, CHU de Rouen, PU-PH Membres du jury : Dr Damien Lannoy, CHRU de Lille, MCU-PH
Dr Marc Laurent, CHU de Rouen, PH
Dr Domitille Meyer, CHU de Rouen, Assistant spécialiste Dr Damien Talon, AP-HP - Hôpital Cochin, PH
Cartographie des risques en stérilisation : utilisation
d’un nouvel outil avant l’ouverture d’un bâtiment
2
Remerciements
A mon jury,
A Monsieur le Professeur Rémi Varin
Pour m’avoir fait l’honneur de présider ce jury, Pour avoir coordonné mes quatre années d’internat,
Soyez assuré de ma reconnaissance et de mon plus profond respect.
A Monsieur le Docteur Marc Laurent
Pour m’avoir dirigé dans ce travail
Merci pour ta disponibilité, et de m’avoir fait confiance, au cours du stage et dans ce travail.
A Monsieur le Professeur Damien Lannoy
Merci d’avoir accepté de faire partie de ce jury de thèse Veuillez trouver ici le témoignage de ma reconnaissance.
A Monsieur le Docteur Damien Talon
Merci de m’avoir fait découvrir le monde de la stérilisation, De m’avoir fait aimer l’hôpital dès mes premiers pas à Cochin, Et enfin merci d’accepter de clôturer ces années à mes côtés.
A Madame le Docteur Domitille Meyer
Merci d’avoir accepté de faire partie de ce jury,
D’avoir été aussi présente lors de mon stage en stérilisation, tout en me permettant de grandir et me préparer à la suite,
3 A ma famille
A ma mère, pour avoir toujours été là pour moi, d’avoir toujours su m’écouter et me conseiller. A mon père, pour m’avoir appris à ne jamais abandonner et à me battre dans l’adversité.
A mes sœurs, Lana et Margot, pour l’amour que vous me donnez malgré la distance, le sourire sur vos visages à chaque fois que je vous vois, et les rires que nous pouvons partager même après plusieurs mois sans se voir. C’est en grande partie grâce à votre maman que nous pouvons partager ces moments, merci Lara de faire de ton mieux pour que nous soyons une famille.
A mes oncles et tantes qui sont venu me soutenir aujourd’hui, mais aussi à ceux qui n’ont pas pu faire le déplacement. Je suis fière et heureuse de faire partie d’une grande famille aussi soudée.
A mes cousins, même si nous ne nous voyons pas assez souvent, notre relation d’enfance est ce que j’ai eu de plus proche de frères et sœurs avant d’en avoir. Et aux plus petits, qui me rappellent à chaque rencontre familiale la magie d’une grande famille.
A ma filleule, Pauline, et à ma marraine, Françoise, pour ces moments privilégiés.
A ma grand-mère, Thérèse, qui me montre chaque jour que, même dans l’adversité, la vie est belle, et que nous sommes des battants nés.
A mes grands-parents défunts, de qui j’ai pu tant apprendre et qui resteront toujours dans mon cœur.
A Julien,
Pour m’apprendre à être toujours positive, pour me soutenir quel que soit mon état de stress ou d’énervement sans jamais ciller, pour savoir exactement quand ta présence est nécessaire.
A mes amis parisiens,
A Margaux, même si les circonstances de notre rencontre restent à débattre, tu as toujours été là pour moi depuis 10 ans, et te retrouver même après plusieurs mois reste toujours dans la même authenticité.
A Momo, pour la naissance d’une amitié pendant les révisions de l’internat, qui j’espère continuera pendant de nombreuses années.
A Chouchi, pour être venue me voir à Rouen si fréquemment, et ainsi m’avoir tant facilité le départ en province
A Pog, pour m’avoir fait me balader au bout du monde pour te retrouver, et pour ta présence dans les moments difficile
A Sandrine, pour m’avoir appris que le travail c’est très important, mais la tchatche aussi, et m’avoir toujours accueillie lorsque j’en avait besoin
A Tipi et Léa, le trio parisien-rouennais, nous devons passer encore plus de moments ensemble. Au reste des semi-hypes : Priscille, Koub, Germain, Yayou, Bro, Chelma, Chloé, Claire, Kevin et Tomtom. Merci pour toutes ces années de fac qui auraient été insipides sans vous.
4 A mes amis rouennais,
A Marion, pour ta bonté, ta gentillesse, ta présence, ton humour, mais aussi et bien sûr tes expressions qui n’existent pas.
A Mathilde, pour ton humour, tes mensonges, ton amour de la Bretagne. Le trio infernal ne serait sans cet équilibre magique que nous avons réussi à entretenir.
A Nini, pour ton rire, ta sensibilité, ton soutien et ton amour de l’alcool le lundi soir. A Audrey et Domitille, une belle amitié est en train de grandir.
Aux amis par alliance, ce magnifique groupe de l’ABCD. Merci à Pilou, Alban, Edgard, Romain, Jules, Mathilde, Laure, Margot et Lucille de m’avoir accueillie dans votre cercle. Un merci spécial à Ben, qui en plus de m’avoir fait une place dans cette amitié pourtant si intime avec Julien, m’a permis de vivre chez lui, de retrouver mon cousin, et de valider mon master.
A tous mes co-internes et collègues,
Tout d’abord aux internes et externes, Eloïse, Claire, Xavier, Gauthier, Marina et Andrew, sans qui une partie de ce travail n’aurait jamais exister.
A mes co-internes, qui ont rendu cet internat si agréable, et qui m’ont fait me sentir chez moi, du premier au dernier semestre.
A tous les chefs avec qui j’ai pu travailler, qui m’ont appris mon futur métier. Un merci spécial à Laurent Mettoudi, qui m’a appris à découvrir aimer la pharmacie,
5
“L’Université de Rouen et l’UFR de Médecine et de Pharmacie de Rouen n’entendent donner aucune approbation ni improbation aux opinions émises dans cette thèse. Ces opinions sont propres à leurs auteurs.”
6 ANNEE UNIVERSITAIRE 2019 – 2020
U.F.R SANTE DE ROUEN ---
DOYEN : Professeur Benoît VEBER
ASSESSEURS : Professeur Michel GUERBET
Professeur Agnès LIARD Professeur Guillaume SAVOYE
I - MEDECINE
PROFESSEURS DES UNIVERSITES – PRATICIENS HOSPITALIERS
Mr Frédéric ANSELME HCN Cardiologie Mme Gisèle APTER Havre Pédopsychiatrie Mme Isabelle AUQUIT AUCKBUR HCN Chirurgie plastique Mr Jean-Marc BASTE HCN Chirurgie thoracique Mr Fabrice BAUER HCN Cardiologie
Mme Soumeya BEKRI HCN Biochimie et biologie moléculaire Mr Ygal BENHAMOU HCN Médecine interne
Mr Jacques BENICHOU HCN Biostatistiques et informatique médicale Mr Olivier BOYER UFR Immunologie
Mme Sophie CANDON HCN Immunologie
Mr François CARON HCN Maladies infectieuses et tropicales Mr Phillipe CHASSAGNE HCN Médecine interne (gériatrie)
Mr Vincent COMPERE HCN Anesthésiologie et réanimation chirurgicale Mr Jean-Nicolas CORNU HCN Urologie
Mr Antoine CUVELIER HB Pneumologie
Mr Jean-Nicolas DACHER HCN Radiologie et imagerie médicale
Mr Stéfan DARMONI HCN Informatique médicale et techniques de communication
Mr Pierre DECHELOTTE HCN Nutrition Me Stéphane DERREY HCN Nerochirurgie Mr Frédéric DI FIORE CHB Cancérologie
7
Mr Fabien DOGUET HCN Chirurgie Cardio Vasculaire
Mr Jean DOUCET SJ Thérapeutique – Médecine interne et gériatrique Mr Bernard DUBRAY CHB Radiothérapie
Mr Franck DUJARDIN HCN Chirurgie Orthopédique – Traumatologique Mr Fabrice DUPARC HCN Anatomie – Chirurgie orthopédique et traumatologique
Me Eric DURAND HCN Cardiologie
Mr Bertrand DUREUIL HCN Anesthésiologie et réanimation chirurgicale Mme Hélène ELTCHANINOFF HCN Cardiologie
Mr Manuel ETIENNE HCN Maladies infectieuses et tropicales Mr Thierry FREBOURG UFR Génétique
Mr Pierre FREGER (surnombre) HCN Anatomie – Neurochirurgie Mr Jean François GEHANNO HCN Médecine et santé au travail Mr Emmanuel GERARDIN HCN Imagerie médicale
Mme Priscille GERARDIN HCN Pédopsychiatrie M. Guillaume GOURCEROL HCN Physiologie Mr Dominique GUERROT HCN Néphrologie Mr Olivier GUILLIN HCN Psychiatrie Adultes Mr Didier HANNEQUIN HCN Neurologie
Mr Claude HOUDAYER HCN Génétique Mr Fabrice JARDIN CHB Hématologie Mr Luc-Marie JOLY HCN Médecine d’urgence Mr Pascal JOLY HCN Dermato – Vénéréologie Mme Bouchra LAMIA Havre Pneumologie
Mme Annie LAQUERRIERE HCN Anatomie et cytologie pathologiques Mr Vincent LAUDENBACH HCN Anesthésie et réanimationchirurgicale Mr Joël LECHEVALLIER HCN Chirurgie infantile
Mr Hervé LEFEBVRE HB Endocrinologie et maladies métaboliques Mr Thierry LEQUERRE HCN Rhumatologie
Mme Anne-Marie LEROI HCN Physiologie Mr Hervé LEVESQUE HCN Médecine interne Mme Agnès LIARD-ZMUDA HCN Chirurgie infantile Mr Pierre Yves LITZLER HCN Chirurgie cardique
Mr Bertrand MACE HCN Histologie, embryologie, cytogénétique M. David MALTETE HCN Neurologie
Mr Christophe MARGUET HCN Pédiatrie
Mme Isabelle MARIE HCN Médecine interne Mr Jean-Paul MARIE HCN Oto-rhino-laryngologie Mr Loïc MARPEAU HCN Gynécologie – Obstétrique
8
Mr Stéphane MARRET HCN Pédiatrie Mme Véronique MERLE HCN Epidémiologie
Mr Pierre MICHEL HCN Hépato-gastro-entérologie M. Benoit MISSET (détachement) HCN Réanimation Médicale Mr Marc MURAINE HCN Ophtalmologie
Mr Christophe PEILLON HCN Chirurgie générale Mr Christian PFISTER HCN Urologie
Mr Jean-Christophe PLANTIER HCN Bactériologie – Virologie Mr Didier PLISSONNIER HCN Chirurgie vasculaire Mr Gaëtan PREVOST HCN Endocrinologie
Mr Jean-Christophe RICHARD (détachement)HCN Réanimation médicale – Médecine d’urgence Mr Vincent RICHARD UFR Pharmacologie
Mme Nathalie RIVES HCN Biologie du développement et de la reproduction Mr Horace ROMAN (disponibilité) HCN Gynécologie – Obstétrique
Mr Jean-Christophe SABOURIN HCN Anatomie – Pathologie Mr Mathieu SALAUN HCN Pneumologie
Mr Guillaume SAVOYE HCN Hépato-gastrologie Mme Céline SAVOYE-COLLET HCN Imagerie médicale Mme Pascale SCHNEIDER HCN Pédiatrie
Mr Lilian SCHWARZ HCN Chirurgie Viscérale et Digestive Mr Michel SCOTTE HCN Chirurgie digestive
Mme Fabienne TAMION HCN Thérapeutique Mr Luc THIBERVILLE HCN Pneumologie
Mr Hervé TILLY (surnombre) CHB Hématologie et transfusion M. Gilles TOURNEL HCN Médecine Légale
Mr Olivier TROST HCN Chirurgie Maxillo-Faciale Mr Jean-Jacques TUECH HCN Chirurgie digestive Mr Jean-Pierre VANNIER (surnombre) HCN Pédiatrie génétique
Mr Benoît VEBER HCN Anesthésiologie – Réanimation chirurgicale Mr Pierre VERA CHB Biophysique et traitement de l’image Mr Eric VERIN Les Herbiers Médecine Physique et Réadaptation Mr Eric VERSPYCK HCN Gynécologie obstétrique
Mr Olivier VITTECOQ HC Rhumatologie Mme Marie-Laure WELTER HCN Physiologie
9 MAITRES DE CONFERENCES DES UNIVERSITES – PRATICIENS HOSPITALIERS
Mme Najate ACHAMRAH HCN Nutrition
Mme Noëlle BARBIER-FREBOURG HCN Bactériologie – Virologie Mr Emmanuel BESNIER HCN Anesthésiologie – Réanimation Mme Carole BRASSE LAGNEL HCN Biochimie
Mme Valérie BRIDOUX HUYBRECHTSHCN Chirurgie Vasculaire Mr Gérard BUCHONNET HCN Hématologie
Mme Mireille CASTANET HCN Pédiatrie
Mme Nathalie CHASTAN HCN Neurophysiologie Mr Moïse COEFFIER HCN Nutrition
Mr Serge JACQUOT UFR Immunologie
Mr Joël LADNER HCN Epidémiologie, économie de la santé Mr Jean-Baptiste LATOUCHE UFR Biologie cellulaire
M. Florent MARGUET HCN Histologie
Mme Chloé MELCHIOR HCN Gastroentérologie Mr Thomas MOUREZ (détachement) HCN Virologie
Mr Gaël NICOLAS UFR Génétique
Mme Muriel QUILLARD HCN Biochimie et biologie moléculaire Mme Laëtitia ROLLIN HCN Médecine du Travail
Mme Pascale SAUGIER-VEBER HCN Génétique
Mme Anne-Claire TOBENAS-DUJARDIN HCN Anatomie Mr David WALLON HCN Neurologie Mr Julien WILS HCN Pharmacologie
PROFESSEUR AGREGE OU CERTIFIE
Mr Thierry WABLE UFR Communication Mme Mélanie AUVRAY-HAMEL UFR Anglais
10
II – PHARMACIE
PROFESSEURS DES UNIVERSITES
Mr Jérémy BELLIEN (PU-PH) Pharmacologie
Mr Thierry BESSON Chimie Thérapeutique
Mr Jean COSTENTIN (Professeur émérite) Pharmacologie
Mme Isabelle DUBUS Biochimie
Mr Abdelhakim EL OMRI Pharmacognosie
Mr François ESTOUR Chimie Organique
Mr Loïc FAVENNEC (PU-PH) Parasitologie
M Jean Pierre GOULLE (Professeur émérite) Toxicologie
Mr Michel GUERBET Toxicologie
Mme Christelle MONTEIL Toxicologie
Mme Martine PESTEL-CARON (PU-PH) Microbiologie
Mr Rémi VARIN (PU-PH) Pharmacie clinique
Mr Jean-Marie VAUGEOIS Pharmacologie
Me Philippe VERITE Chimie Analytique
MAITRES DE CONFERENCES DES UNIVERSITES
Mme Cécile BARBOT Chimie Générale et Minérale
Mr Frédéric BOUNOURE Pharmacie Galénique
Mr Thomas CATANHEIRO Chimie Organique
Mr Abdeslam CHAGRAOUI Physiologie
Mme Camille CHARBONNIER (LE CLEZIO) Statistiques
Mme Elizabeth CHOSSON Botanique
Mme Marie Catherine CONCE-CHEMTOB Législation pharmaceutique et économie de la santé
Mme Cécile CORBIERE Biochimie
Mme Nathalie DOURMAP Pharmacologie
Mme Isabelle DUBUC Pharmacologie
Mme Dominique DUTERTE-BOUCHER Pharmacologie
Mr Gilles GARGALA (MCU-PH) Parasitologie
Mme Nejla EL GHARBI-HAMZA Chimie Analytique
11
Mr Hervé HUE Biophysique et mathématiques
Mme Hong LU Biologie
Mme Marine MALLETER Toxicologie
M. Jérémie MARTINET (MCU-PH) Immunologie
Mme Tiphaine ROGEZ-FLORENT Chimie Analytique
Mr Mohamed SKIBA Pharmacie galénique
Mme Malika SKIBA Pharmacie galénique
Mme Christine THARASSE Chimie thérapeutique
Mr Frédéric ZIEGLER Biochimie
PROFESSEURS ASSOCIES
Mme Cécile GUERARD-DETUNCG Pharmacie officinale
Mme Caroline BERTOUX Pharmacie
PAU-PH
M. Mikaël DAOUPHARS
PROFESSEUR CERTIFIE
Mme Mathilde GUERIN Anglais
ASSISTANTS HOSPITALO-UNIVERSITAIRES
Mme Alice MOISAN Virologie
M. Henri GONDE Pharmacie
ATTACHES TEMPORAIRES D’ENSEIGNEMENT ET DE RECHERCHE
M. Abdel MOUHAJIR Parasitologie
12 LISTE DES RESPONSABLES DES DISCIPLINES PHARMACEUTIQUES
Mme Cécile BARBOT Chimie générale et minérale
Mr Thierry BESSON Chimie Thérapeutique
Mr Abdelslam CHAGRAOUI Physiologie
Mme Elisabeth CHOSSON Botanique
Mme Marie-Catherine CONCE-CHEMTOB Législation et économie de la santé
Mme Isabelle DUBUS Biochimie
Mr Abdelhakim EL OMRI Pharmacognosie
Mr François ESTOUR Chimie organique
Mr Loïc FAVENNEC Parasitologie
Mr Michel GUEBERT Toxicologie
Mme Martine PESTEL-CARON Microbiologie
Mr Mohamed SKIBA Pharmacie galénique
Mr Rémi VARIN Pharmacie clinique
M. Jean-Marie VAUGEOIS Pharmacologie
13
III – MEDECINE GENERALE
PROFESSEUR MEDECINE GENERALE
Mr Jean-Loup HERMIL (PU-MG) UFR Médecine générale
MAITRE DE CONFERENCE MEDECINE GENERALE
Mr Matthieu SCHUERS (MCU-MG) UFR Médecine générale
PROFESSEURS ASSOCIES A MI-TEMPS – MEDECINS GENERALISTE
Mr Emmanuel LEFEBVRE UFR Médecine générale
Mme Elisabeth MAUVIARD UFR Médecine générale
Mr Philippe NGUYEN THANH UFR Médecine générale
Mme Yveline SEVRIN UFR Médecine générale
Mme Marie Thérèse THUEUX UFR Médecine générale
MAITRES DE CONFERENCE ASSOCIES A MI-TEMPS – MEDECINS GENERALISTE
Mr Pascal BOULET UFR Médecine générale
Mme Laëtitia BOURDON UFR Médecine générale
Mr Emmanuel HAZARD UFR Médecine générale
14
ENSEIGNANTS MONO-APPARTENANTS
PROFESSEURS
Mr Paul MULDER (phar) Sciences du médicament
Mme Su RUAN Génie informatique
MAITRES DE CONFERENCES
Mr Sahil ADRIOUCH (med) Biochimie et biologie moléculaire (Inserm 905) Mme Gaëlle BOUGEARD-DENOYELLE (med) Biochimie et biologie moléculaire (UMR 1079) Mme Carine CLEREN (med) Neurosciences (Néovasc)
M. Sylvain FRAINEAU (med) Physiologie (Inserm U 1096)
Mme Pascaline GAILDRAT (med) Génétique moléculaire humaine (UMR 1079) Mr Nicolas GUEROUT (med) Chirurgie expérimentale
Mme Rachel LETELLIER (med) Physiologie
Mr Antoine OUVRARD-PASCAUD (med) Physiologie (Unité Inserm 1076) Mr Frédéric PASQUET Sciences du langage, orthophonie Mme Christine RONDANINO (med) Physiologie de la reproduction Mr Youssan Var TAN Immunologie
Mme Isabelle TOURNIER (med) Biochimie (UMR 1079)
CHEF DES SERVICES ADMINISTRATIFS : Mme Véronique DELAFONTAINE
HCN – Hôpital Charles Nicolle HB – Hôpital de Bois Guillaume
CB – Centre Henri Becquerel CHS – Centre Hospitalier Spécialisé du Rouvray CRMPR – Centre Régional de Médecine physique et Réadaptation SJ – Saint Julien Rouen
15
Table des matie res
Introduction... 21
1. Première partie : Matériel, méthode et état des lieux au CHU de Rouen ... 22
1.1. Définitions ... 22
1.1.1. Gestion des risques et cartographie des risques ... 22
1.1.1.1. Notion de risque ... 22
1.1.1.2. Processus de management des risques ... 23
1.1.1.3. Les méthodes d’analyse des risques ... 23
La méthode AMDEC ... 24
APR/AGR – Analyse Préliminaire des Risques et Analyse Globale des Risques ... 25
L’arbre des défaillances ... 27
La méthode HAZOP (Hazard and Operability Study) ... 28
MOSAR – Méthode Organisée Systémique d’Analyse des Risque ... 29
L’analyse des réseaux de Petri ... 30
1.1.1.4. Critères de sélection des méthodes gestion des risques ... 30
Une méthode systémique ... 30
1.1.2. Un nouvel outil dynamique de cartographie des risques ... 33
1.1.2.1. Fonctionnalités de l’outil ... 33
Onglet « Paramétrages » ... 33
Le formulaire d’ajout des dysfonctionnements ... 34
Onglet « Base de données » ... 34
Onglet « Graphiques » ... 35
Onglet « Algorithme » ... 36
1.1.3. La stérilisation ... 37
1.1.3.1. Processus management – Organisation et règlementation ... 37
Constitution et règlements européens ... 38
Lois et ordonnances ... 38
Décrets et arrêtés ... 39
Circulaires ... 39
Normes ... 40
1.1.3.2. Processus opérationnel – Opérations et contrôles effectués en stérilisation ... 41
Risque prion ... 41
Pré-désinfection ... 44
16
Recomposition ... 48
Conditionnement ... 49
Stérilisation ... 52
Transport des DMR ... 55
Stockage des DMR stériles ... 56
1.1.3.3. Management qualité – Traçabilité ... 57
1.2. La stérilisation centrale du CHU de Rouen ... 59
1.2.1. Organisation actuelle ... 59
1.2.1.1. Activité médico-chirurgicale au CHU de Rouen nécessitant une prestation de stérilisation... 59
1.2.1.2. Les blocs opératoires sur le site de Charles Nicolle ... 59
Circuit du matériel au bloc opératoire ... 60
Communication avec le service de stérilisation ... 61
1.2.1.3. La stérilisation ... 62
Locaux ... 62
Personnel ... 64
Activité ... 64
Circuit du matériel à stériliser ... 65
Cas particuliers ... 67
1.2.2. Le projet Robec ... 68
1.2.2.1. Gestion des arsenaux ... 70
Développement de l’ultra ... 70
Homogénéisation des boites ... 71
1.2.2.2. Packs Opératoires Programmés ... 72
1.2.2.3. Pré-désinfection mécanisée ... 73
1.2.3. Objectifs de la cartographie ... 74
2. Deuxième partie : Résultats ... 75
2.1. Cartographie des risques ... 75
2.1.1. Identification des risques – Approche par processus ... 75
2.1.2. Cotation des risques ... 76
2.1.3. Choix de l’algorithme – sélection des risques ... 78
2.1.3.1. Algorithme 1 ... 79
2.1.3.2. Algorithme 2 ... 79
2.1.3.3. Algorithme 3 ... 80
2.1.3.4. Algorithme 4 ... 81
2.2. Mise en place des actions ... 83
17
2.2.1.1. Résumé des audits déjà réalisés ... 83
2.2.1.2. Evaluation des actions précédentes et mise en place de nouvelles actions ... 85
Mauvaise gestion de l’instrumentation au bloc opératoire ... 85
Locaux et matériel inadaptés ... 86
Non-respect du code couleur MCJ ... 86
Manque de personnel, formation, temps dédié ... 87
Traçabilité de la pré-désinfection... 87
Fiches de codification mouillées ... 88
Port des EPI ... 89
Code barre de chariot mal placé... 89
Procédures d’hygiène absentes ou non respectées ... 90
Mise à disposition de matériel pour le bloc ... 90
Pas de fiches de données de sécurité ... 91
Déclaration difficile des non-conformités ... 92
2.2.1.3. Blocs opératoires déménageant au Robec ... 92
2.2.2. Gestion du risque prion ... 93
2.2.3. Traçabilité de l’étape de lavage ... 95
2.2.3.1. Passage en laveur-désinfecteur ... 95
2.2.3.2. Lavage manuel ... 97
2.2.4. Surpression en zone de conditionnement ... 98
2.2.4.1. Recommandations et bonnes pratiques ... 98
2.2.4.2. Le projet sondes d’environnement ... 99
2.2.5. Non-respect de la marche en avant ... 101
2.2.5.1. Recensement du matériel et bibliographie... 101
2.2.5.2. Matériel passant en Stérilisateur Basse Température ... 101
2.2.5.3. Matériel neuf ... 102
2.2.5.4. Autres spécificités ... 103
2.2.6. Pointage non réalisé des services de soins ... 105
2.2.7. Défaut d’hygiène des mains ... 107
2.2.8. Stérilisateur trop chargé ... 109
2.2.8.1. Mise en place de l’audit ... 109
2.2.8.2. Résultats de l’audit ... 111
2.2.9. Inversion DM/étiquette ... 113
3. Troisième partie : Discussion ... 114
3.1. Cartographie des risques ... 115
3.1.1. Avantages et inconvénients d’une cartographie des risques ... 115
3.1.2. Le nouvel outil dynamique ... 117
18
3.2.1. Actions à mettre en place ... 120
3.2.1.1. Pré-désinfection dans les anciens blocs ... 120
3.2.1.2. Actions abandonnées ... 121
3.2.1.3. Actions en cours d’analyse ... 121
3.2.2. Actions en développement ... 123
3.2.2.1. Traçabilité du lavage manuel ... 123
3.2.2.2. Absence de surpression ... 123
3.2.2.3. Hygiène et sécurité en zone de réception/lavage ... 124
3.2.2.4. Déclaration des non-conformités... 124
3.2.3. Actions finalisées ... 126
3.2.3.1. Au niveau de la stérilisation ... 126
3.2.3.2. Au niveau du bâtiment Robec ... 127
4. Conclusion ... 130
Annexes ... 132
19
Table des figures
Figure 1 - Méthode APR/AGR ...26
Figure 2 - Modèle d'arbre des défaillances ...28
Figure 3 – Méthode MOSAR - Exemple d'un sous-système ...29
Figure 4 - Méthode MOSAR - Relations entre les boites noires ...29
Figure 5 - Liste des risques pour le processus conditionnement ...33
Figure 6 - Formulaire d'ajout d'un dysfonctionnement ...34
Figure 7 - Exemple de diagramme de Kiviat ...35
Figure 8 – Onglet algorithme...36
Figure 9 - Pyramide de Kelsen ...39
Figure 10 - Le cercle de Sinner ...46
Figure 11 - Plan de la stérilisation du CHU de Rouen ...63
Figure 12 - Le futur bâtiment Robec ...68
Figure 13 - Exemple d'emballage ULTRA ...70
Figure 14 - Nombre de dysfonctionnements retrouvés par algorithme ...78
Figure 15 - Liste des FDS sur l'intranet de la Pharmacie ...91
Figure 16 - Porte-broche du service de stérilisation ... 103
Figure 17 - Rampes du service d'hygiène ... 104
Figure 18 - Protocole "Retour des services de soin" ... 106
Figure 19 - Exemple de caisson pédagogique pour l'utilisation du SHA ... 107
Figure 20 - Résultats de l'évaluation Hygiène des mains - 30 mars 2019 ... 108
Figure 21 - Grille d'audit chargement des autoclaves ... 110
20
Table des tableaux
Tableau 1 - Comparaison des méthodes d'analyse des risques ...32
Tableau 2 – Détermination du niveau de risque prion, Instruction 449 – Fiche n°1 .42 Tableau 3 - Définition de la classe ISO 8 selon la norme ISO 14 644-1 ...49
Tableau 4 – Procédés d’emballages selon la norme NF EN ISO 11 607-1 ...50
Tableau 5 - Nombre de risques retrouvés par processus ...75
Tableau 6 - Cotation de la fréquence...76
Tableau 7 - Cotation de la gravité ...76
Tableau 8 - Cotation de la détectabilité et de la maitrise ...76
Tableau 9 - Risques sélectionnés ...82
Tableau 10 - Résumé des audits réalisés entre 2012 et 2017 par la stérilisation du CHU de Rouen ...84
21
Introduction
Le CHU de Rouen construit pour l’horizon 2020 un nouveau bâtiment de chirurgie. Ce bâtiment comprendra un étage entièrement dédié à la chirurgie ambulatoire, et deux étages de chirurgie générale et de spécialités.
Dans ce cadre de remaniements logistiques importants, notamment au niveau du service de stérilisation, il a été décidé de réaliser une cartographie des risques du processus de stérilisation existant, afin de pouvoir mettre en évidence les risques les plus sensibles du processus actuel, les corriger, et pouvoir intégrer ces notions dans la nouvelle organisation.
Nous avons donc décidé de réaliser une cartographie par processus grâce à un nouvel outil dynamique, qui permettra, dans le futur, de la mettre à jour facilement. L’objectif principal de ce travail est de mettre en place à l’issue de cette cartographie des actions principales et des actions secondaires plus rapides à exécuter, de les évaluer et, le cas échéant, les faire évoluer.
Dans une première partie, nous décrirons les différentes méthodologies de cartographies des risques et celle sélectionnée ; l’outil dynamique utilisé lors de ce travail, ainsi que le processus de stérilisation. Nous ferons ensuite un état des lieux de la situation actuelle et future au CHU de Rouen.
La seconde partie développera des méthodes utilisées pour cette cartographie, et la prise en compte des besoins afin de définir les actions. La mise en place des actions sera ensuite décrite, ainsi que leur évaluation.
Dans une dernière partie, nous discuterons des points forts et des limites de cette cartographie, ainsi que des perspectives futures.
22
1. Première partie : Matériel, méthode et état
des lieux au CHU de Rouen
1.1. Définitions
1.1.1. Gestion des risques et cartographie des risques
La gestion des risques est partie intégrante de la certification HAS (Haute Autorité de Santé) (1) et de son manuel qualité (2) depuis 2007. L’objectif de cette pratique est la réduction des risques à son minimum, c'est-à-dire d’en diminuer la survenue et d’en limiter les conséquences (3).
La gestion des risques est un système de management, une activité transversale de l’hôpital dans la prise en charge du patient. C’est une activité d’autant plus importante que l’enjeu de sécurité optimale pour le patient est grand. Elle se révèle primordiale, avec des conséquences pouvant être très graves.
1.1.1.1. Notion de risque
« Le risque est défini comme une incertitude, menace ou opportunité que l’activité doit anticiper, comprendre et protéger, [pour] atteindre les objectifs définis dans le cadre de sa stratégie. » (4).
Le risque se mesure par deux caractéristiques :
La fréquence F, qui mesure l’incertitude de l’occurrence de l’évènement considéré.
La gravité G, qui mesure les conséquences de l’évènement.
Le produit des deux définit la criticité, c’est-à-dire le risque moyen. Elle permet de hiérarchiser les risques.
23 La détectabilité, qui représente l’efficacité du système de surveillance.
La réductibilité, qui traduit la possibilité de mettre en œuvre des mesures de réduction du risque.
La gravité ou le bénéfice de l’effet résiduel, qui prend en compte les conséquences du risque à long terme, une fois la manifestation principale passée.
L’importance de l’activité affectée.
Le taux d’achèvement de l’activité affectée.
1.1.1.2. Processus de management des risques
La norme ISO 9001 définit les critères pour un système de management. Elle repose sur un certain nombre de principes de management de la qualité, notamment la forte orientation client, la motivation et l’engagement de la direction, l’approche processus et l’amélioration continue.
La certification ISO 9001 n’est pas une obligation, mais c’est la preuve de la mise en œuvre de la norme en bonne et due forme (5).
La norme ISO 9001 vise à harmoniser le processus de management du risque et les définitions qui lui sont rattachées, donner des conseils sur la maintenance et la mise en œuvre du système de management (6).
1.1.1.3. Les méthodes d’analyse des risques
Les différentes méthodes d’analyse des risques (4) sont des outils issus du milieu industriel. Il existe deux types de démarches. La méthode déductive (a posteriori), part de l’évènement indésirable et cherche par une approche descendante toutes les causes possibles.
La démarche inductive (a priori), identifie toutes les combinaisons d’évènements élémentaires possibles qui peuvent entrainer la réalisation d’un évènement indésirable.
24
La méthode AMDEC
La méthode AMDEC, l’Analyse des Modes de Défaillance, de leur Effet et de leur Criticité, est une méthode inductive d’analyse de fiabilité d’un système. A partir de la défaillance d’un composant ou d’une structure fonctionnelle, l’étude du lien entre cette défaillance et ses conséquences sur le système est réalisée. Elle permet donc d’identifier les différents modes de défaillance du système, de recenser toutes les causes pour chaque mode et leurs effets sur la mission du système.
L’étude est ensuite complétée par une liste de recommandations et de moyens de détection pour limiter l’effet ou diminuer sa fréquence de survenue. L’objectif est la recherche du mode de défaillance. La notion du mode de défaillance est considérée comme un symptôme qui révèle la défaillance. On analyse donc une fonction et ce qu’il se passerait si cette fonction ne se réalise pas au moment désiré, si elle ne se réalise plus, si elle se dégrade ou si elle se réalise de façon intempestive.
L’établissement des modes de défaillance peut aussi se faire à l’aide de macro-causes répertoriées. On recherche alors les macro-causes, leurs effets, et on évalue les modes de défaillance sur la base de leur criticité (définie au minimum par la gravité et la fréquence de survenue du risque). Les modes de défaillances sont alors hiérarchisés et permettent de définir les priorités pour les actions correctives.
L’AMDEC est un outil intéressant pour détecter les défaillances d’un processus, même les plus inattendues. Cependant, elle ne permet pas d’avoir une vision croisée des pannes possibles et leur conséquence. De plus, l’efficacité de l’AMDEC dépend de la possibilité de déterminer tous les modes de défaillance possibles d’un système. Le volume d’information pour cette analyse est très vite important, et rend la démarche complexe et sujette à erreurs et omissions.
25
APR/AGR – Analyse Préliminaire des Risques et Analyse Globale des Risques
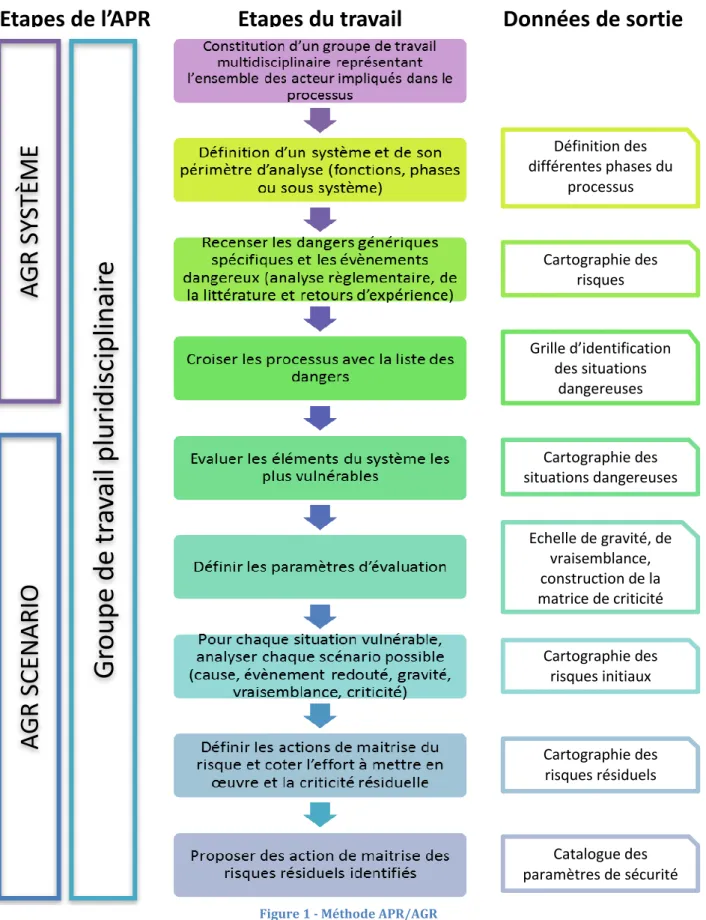
L’Analyse Préliminaire des Risques est une méthode inductive utilisée pour l’identification, l’analyse et le traitement des risques.L’analyse Globale des Risques qui la prolonge et la globalise est une méthode structurée permettant l’identification des situations dangereuses d’un procédé ou d’un système et d’évaluer le potentiel de chacun à engendrer un accident plus ou moins grave. L’AGR vise ainsi à mettre en évidence rapidement les plus importants problèmes susceptibles d’être rencontrés et la façon de les traiter.
La démarche de l’AGR est réalisée en deux étapes : l’AGR système et l’AGR scénario (7).
L’AGR système, dont l’objectif est l’élaboration d’une cartographie des risques, correspond à :
La définition du périmètre d’analyse système. Le système est alors décomposé en phases, sous-systèmes ou en fonctions, sous phases et tâches élémentaires.
L’élaboration de la liste structurée des dangers (génériques et spécifiques propres au système),
L’évaluation des interactions dangers/système,
La détermination de la cartographie des situations dangereuses en priorisant les actions à entreprendre.
L’AGR scénario est une analyse des risques pour chaque situation dangereuse identifiée dans la cartographie comme prioritaire. Les entrées sont la cartographie des situations dangereuses, les échelles de gravité, de vraisemblance, d’effort, et le référentiel d’acceptabilité du risque. Les sorties sont la cartographie des risques initiaux et des risques résiduels sous forme de diagramme et les listes des actions de maitrise de risque.
26
Gr
oup
e de
tr
av
ail
p
luri
discipl
inair
e
A
GR S
YS
TÈM
E
A
GR SCENARIO
Cartographie des situations dangereuses Echelle de gravité, de vraisemblance, construction de la matrice de criticité Cartographie des risques initiaux Cartographie des risques résiduels Catalogue des paramètres de sécurité Définition des différentes phases du processus Cartographie des risques Grille d’identification des situations dangereusesEtapes de l’APR
Etapes du travail
Données de sortie
27 L’AGR est donc une méthode d’analyse inductive et systématique, semi-quantitative et simple d’application. Elle permet une vision globale des risques en intégrant tous les types de dangers, et une flexibilité.
L’arbre des défaillances
L’analyse par arbre des défaillances est déductive : en partant d’un évènement indésirable unique et défini, il s’agit de rechercher les combinaisons d’évènements qui conduisent à l’occurrence de l’évènement. Cette méthode se déroule en quatre étapes :
L’examen du système et la définition des évènements indésirables dont il peut être le foyer. Cela se fait par une analyse globale, ou une AMDE (Analyse des Modes de Défaillance et de leur Effet).
La modélisation du système avec la recherche et la description des évènements qui peuvent avoir lieu. Cette étape implique la fixation des limites de l’analyse des causes.
L’arbre est ensuite établi : le point de départ est l’évènement indésirable défini au préalable. Les évènements intermédiaires (internes ou externes) qui paraissent engendrer l’évènement final sont définis, puis les combinaisons qui lient les évènements intermédiaires à l’évènement final sont représentées graphiquement.
L’appréciation de la fiabilité du système est basée sur la quantification : en partant du principe où la probabilité des évènements de base est connue, la probabilité d’occurrence de l’évènement indésirable est calculable.
Cette analyse permet d’obtenir des actions correctives, basées sur la notion de coupe minimale. La coupe minimale est un ensemble d’évènements, qui, s’ils se produisent ensemble, entrainent l’évènement indésirable.
Cette méthode ne permet de définir que les causes ayant un effet significatif au niveau d’un évènement indésirable. La représentation des modes de défaillance est facilitée par l’utilisation d’un graphique synthétique, mais qui peut rapidement devenir imposant.
28 L’arbre est généralement représenté de haut en bas. La ligne la plus haute ne comporte que l’événement indésirable. Chaque ligne détaille ensuite la ligne supérieure en présentant la combinaison ou les combinaisons susceptibles de produire l’événement de la ligne supérieure à laquelle ils sont rattachés. Ces relations sont représentées par des liens logiques, dont la plupart sont des « ou » et « et », qualifiés de portes logiques (Figure 2).
Figure 2 - Modèle d'arbre des défaillances
La méthode HAZOP (Hazard and Operability Study)
Cette méthode permet d’évaluer le danger potentiel résultant du mauvais fonctionnement ou de l’utilisation incorrecte de certains composants, et leur effet sur le système. Elle est essentiellement utilisée dans l’industrie chimique.
C’est une méthode d’analyse de risque qualitative, reposant sur des mots clefs, et alimentée par une équipe multidisciplinaire lors de réunions.
Lors des sessions de travail, l’animateur applique chacun des mots guides à chacune des parties du système pour identifier les déviations possibles pouvant mener à des conséquences considérées comme dangereuses. Les déviations potentiellement dangereuses sont alors hiérarchisées pour une action future.
29
MOSAR – Méthode Organisée Systémique d’Analyse des Risque
La méthode MOSAR consiste en la décomposition de systèmes à étudier en sous-systèmes, puis en l’étude de chaque sous-système indépendamment ainsi que les interactions possibles entre eux. La première partie du processus est l’étape de vision macroscopique, avec la description du système, l’identification des sources de danger et des évènements indésirables. Chaque sous-système est ensuite représenté sous forme de boite noire (Figure 3), avec les évènements déclencheurs à l’entrée et les évènements non souhaités à la sortie.
Figure 3 – Méthode MOSAR - Exemple d'un sous-système
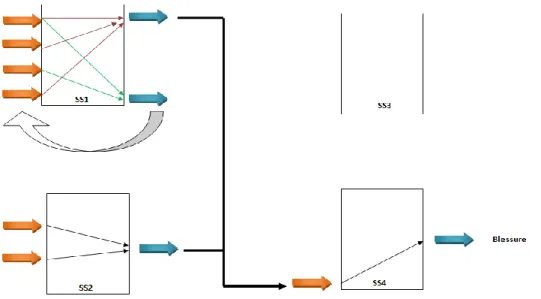
L’analyse se fait ensuite par l’établissement des scénarios d’évènements, non souhaités, correspondant aux connexions entre les différentes boites noires (Figure 4).
Figure 4 - Méthode MOSAR - Relations entre les boites noires
Source : Wikipedia
30 La deuxième partie de l’étude, la vision microscopique, correspond à la représentation des scénarios sous formes d’arbres logiques, de l’évaluation et la hiérarchisation des risques, et de la définition des actions correctives ainsi que leur mise en place.
Cette méthode ressemble beaucoup à l’APR/AGR, mais l’établissement des scénarios non souhaités est beaucoup plus complexe car elle connecte les différents risques et évènements indésirables entre eux, engendrant un très grand nombre de scenarii.
L’analyse des réseaux de Petri
Ils sont utilisés principalement comme outil de modélisation de logiciel. Ce modèle permet de simuler le comportement d’un système complexe et de ses interactions avec son environnement. Il permet de prendre en compte le paramètre temps, et donc de supprimer des séquences impossibles. Il existe de nombreux programmes informatiques d’assistance à l’analyse. Cependant cette méthode est réservée à des spécialistes du fait de sa complexité.
1.1.1.4. Critères de sélection des méthodes gestion des risques
Une méthode systémique
« Le risque et sa maitrise est une préoccupation majeure dans une entreprise. Cette maitrise est d’autant plus difficile que les systèmes techniques, les organisations assurant leur développement, leur production, leur exploitation et leur maintenance ainsi que l’environnement dans lequel les systèmes opèrent sont eux-mêmes de plus en plus complexes. » (8)
L’approche système parait donc nécessaire pour appréhender cette complexité et prendre en compte tous les aspects du risque. Aux risques techniques s’ajoutent les risques systèmes issus des différents niveaux d’interaction et de leur évolution.
31 La maitrise du risque nécessite une approche systémique du fait (6):
De scénarii difficilement prédictibles liés à des aléas d’origines diverses (internes, externes, techniques ou humains),
De dysfonctionnements susceptibles de se produire à cause de la complexité des interactions sur les multiples interfaces (tant techniques qu’organisationnelles),
De la difficulté d’estimer des risques en termes de fréquence et de gravité, De la difficulté d’évaluer l’efficacité et la vulnérabilité des barrières de
protection et de leur combinaison et notamment d’y détecter les maillons faibles.
Ainsi, pour maitriser les risques dans un système, un certain recul s’impose. En effet, intervenir, en apportant des modifications, des ajustements directement sur le système sans un certain niveau de confiance dans les actions à entreprendre présente en soit un risque. Par conséquent, il est nécessaire de raisonner sur des modèles prospectifs du système, pour faire la preuve que les actions à entreprendre vont bien avoir les résultats attendus.
Le Tableau 1 permet de comparer les différentes méthodes d’analyse de risques expliquées ci-dessus. Les systèmes traités peuvent être de pilotage, d’information, ou système opérant.
32 Tableau 1 - Comparaison des méthodes d'analyse des risques
Méthode Objectif principal Nature de la méthode Défaillances envisagées Système traité* Domaine d'application AMDEC
Identifier les effets des modes de défaillance des composants sur le système Inductive, quantitative Indépendantes Système opérant Tout type d'industrie APR/AGR Identifier les scénarios d'accident en présence de danger Inductive, semi-quantitative Indépendantes Approche globale, tous les systèmes Tout type d'industrie Arbre des défaillances
Identifier les causes combinées à partir d'un évènement Déductive, quantitative Combinées Système opérant, système d'information Tout type d'industrie HAZOP
Identifier les dangers suite à une déviation des paramètres d'un
procédé Inductive, qualitative Indépendantes Système opérant Industries de procédés (chimie) MOSAR
Identifier les risques techniques d'une installation humaine Inductive, qualitative Combinées Approche globale, tous les systèmes Tout type d'industrie Réseau de Pétri Simuler le comportement d'un système complexe et ses interactions Inductive, scholastique Combinées Système opérant, système d'information Installations industrielles/ informatiques
La méthode APR/AGR parait la plus adaptée à l’activité de stérilisation. En effet, c’est une méthode systémique, inductive, prévisionnelle et semi-quantitative, qui permet d’intégrer tous les types de dangers et couvre ainsi tout le système et son environnement. Elle permet d’analyser les activités présentant à la fois des risques nouveaux et des risques connus.
A ce titre, elle peut remplacer la méthode AMDEC dans la mesure où un mode de défaillance est un danger structurel ou conjoncturel et présente donc un facteur de risque (6).
33
1.1.2. Un nouvel outil dynamique de cartographie des
risques
Pierre Grimaldi (9), pharmacien à l’Assistance Publique – Hôpitaux de Marseille, a mis au point un tableur Excel® (Microsoft©) permettant de réaliser une cartographie des risques selon la méthode APR/AGR de manière facilitée, reproductible et dynamique, spécialement adapté au processus de stérilisation en milieu hospitalier.
1.1.2.1. Fonctionnalités de l’outil
Onglet « Paramétrages »
Un onglet « Paramétrages » (Figure 5) permet de définir le système et le périmètre d’analyse ; afin de recenser les dangers spécifiques génériques et les évènements dangereux. Il regroupe 6 processus : Pré-désinfection, Réception/Lavage, Recomposition, Conditionnement, Stérilisation et Transport ; divisés en sous-processus. Des risques sont ensuite associés à chaque sous-sous-processus. Ces paramètres sont à remplir par l’utilisateur, en fonction de l’activité propre de l’unité de stérilisation dans laquelle il évolue.
Figure 5 - Liste des risques pour le processus conditionnement
Dans cet onglet sont aussi paramétrés les causes (humaine, matérielle, organisationnelles) et les acteurs impliqués.
34
Le formulaire d’ajout des dysfonctionnements
Pour chaque dysfonctionnement ajouté dans la table des processus de l’onglet « Paramétrages », il faut remplir le formulaire (Figure 6). Il est nécessaire d’indiquer l’acteur professionnel impliqué, la cause du dysfonctionnement, sa conséquence, l’existence de mesures correctives, une évaluation de la fréquence et de la gravité sur une échelle de 1 à 5, le coefficient de maîtrise et le coefficient de non-détection du dysfonctionnement. Toutes ces données apparaissent par des menus déroulants grâce aux informations renseignées dans l’onglet précédent.
Figure 6 - Formulaire d'ajout d'un dysfonctionnement
Chaque dysfonctionnement s’incrémente alors dans la base de données.
Onglet « Base de données »
La base de données se présente sous la forme d’un tableur Excel® (Microsoft©) recensant l’ensemble des dysfonctionnements et de tous les paramètres renseignés à l’étape précédente. Les calculs des criticités totales (Fréquence x Gravité), ainsi que des criticités résiduelles en fonction de leur détectabilité et de leur maitrise, pondérés par les coefficients précédemment déterminés sont alors mis en exergue avec un code couleur. La couleur rouge correspond aux criticités fortes, entre 13 et 25 ; la couleur orange aux criticités modérées, entre 7 et 12 ; et la couleur verte aux criticités faibles, entre 1 et 6. Ce tableau permet donc d’avoir une première idée des risques les plus importants.
35
Onglet « Graphiques »
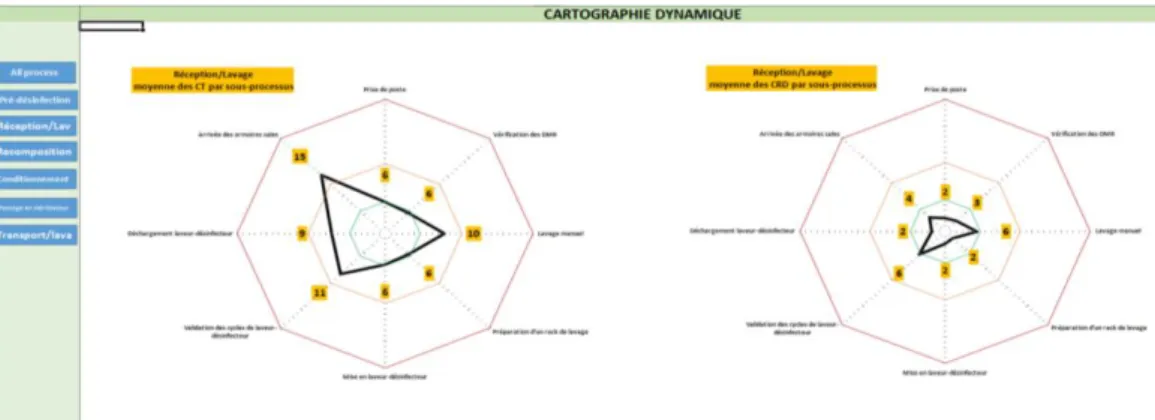
L’onglet « Graphiques » reprend chaque processus, et produit un diagramme de Kiviat (diagramme en radar, Figure 7) des criticités totales, puis pondérées de leur détectabilité et de leur maitrise, en identifiant chaque sous-processus. Cela permet de visualiser facilement les sous-processus les plus à risque pour chaque processus. Les couleurs des différents cercles du diagramme reprennent le code couleur des criticités décrites ci-dessus.
Figure 7 - Exemple de diagramme de Kiviat
La deuxième partie de l’onglet « Graphiques », située sous les diagrammes, reprend le tableur Excel® (Microsoft©) de la base de données correspondant uniquement au processus donné. Les processus sélectionnés par l’algorithme sont mis en surbrillance.
36
Onglet « Algorithme »
L’algorithme (Figure 8) permet de visualiser, tous processus confondus, le nombre de risques critiques, peu maitrisés ou peu détectables. Selon le nombre de dysfonctionnements dans chaque algorithme ou l’exhaustivité voulue, un algorithme est sélectionné, et tous les risques concernés apparaissent alors en surbrillance dans l’onglet précédent.
Figure 8 – Onglet algorithme
Les risques sont alors sélectionnés, et le choix des actions correctives peut débuter. Légende CT : Criticité Totale CRD : Criticité Résiduelle Détectabilité CRM : Criticité Résiduelle Maitrise Rouge : 13 < Criticité < 25 Orange : 7 < Criticité < 12 Vert : 1 < Criticité < 6
37
1.1.3. La stérilisation
Le retraitement des dispositifs médicaux réutilisables (DMR) s’appuie sur quatre processus fondamentaux (10) :
Le processus management qui rappelle la règlementation applicable en France, décrit les responsabilités et les organisations,
Le processus opérationnel qui décrit l’ensemble des opérations et contrôles effectués lors du retraitement des DMR,
Le processus support qui regroupe le personnel, les locaux, la maintenance, les qualifications et les achats,
Le management qualité qui rappelle les principes de qualité applicables et regroupe la gestion documentaire, la gestion des risques et la traçabilité.
1.1.3.1. Processus management – Organisation et règlementation
Dans les établissements de santé, la stérilisation des DMR est soumise à autorisation des Agences Régionales de Santé (ARS) (11). Cette activité est sous la responsabilité du pharmacien assurant la gérance de la Pharmacie à Usage Intérieur (PUI) (12). Les PUI doivent se conformer aux règles décrites dans les Bonnes Pratiques de Pharmacie Hospitalière (BPPH) (13) de 2001, qui sont opposables depuis l’arrêté du 22 juin 2001 (14). La ligne directrice n°1 des BPPH « Préparations des dispositifs médicaux stériles » précise les modalités de prise en charge des DMR :
Elle définit les responsabilités du représentant légal de l’établissement et du pharmacien gérant de la PUI pour les activités ayant trait au processus de stérilisation,
Elle fixe les règles générales relatives au personnel, aux infrastructures de stérilisation, y compris la qualité de l’air et de l’eau, sur les matériels et leurs maintenances ainsi que sur la gestion documentaire,
Elle traite des différentes étapes du processus de stérilisation, de la pré-désinfection jusqu’au stockage,
38 Elle aborde la gestion des risques et le traitement des non-conformités ainsi que les principes à suivre en cas de prise en charge de la stérilisation par une infrastructure tierce (par exemple la sous-traitance).
La mise en place d’un système assurant la qualité et la nomination d’un responsable de ce système par le Directeur Général de l’établissement de santé est obligatoire (13).
Les règles de Droits proviennent de sources et d’autorités différentes. Nous allons donc définir ci-dessous chaque type de règlementation, selon le modèle de la hiérarchie des normes (15).
Constitution et règlements européens
La Constitution annonce ce qui est au domaine de la loi et ce qui est au domaine règlementaire (émanant des administrations). Les règles nationales doivent cohabiter avec les traités internationaux et en particulier avec les textes communautaires.
Dans l’ordre interne, les règlements européens ont une valeur supérieure aux textes nationaux (hormis la Constitution) et ne nécessitent pas de transposition nationale (exemple du nouveau règlement des dispositifs médicaux, (16)).
Les décisions européennes (obligatoires sans transposition), ne concernent que les personnes ou organisations qu’elles identifient.
Les directives sont transposées dans les textes nationaux avant application.
Lois et ordonnances
Les lois (votées par le parlement) s’imposent à tous après publication au journal officiel.
Les ordonnances permettent au gouvernement de demander au parlement de prendre lui-même des mesures relevant normalement du domaine de la loi, afin de mettre en œuvre son programme (article 38 de la Constitution).
39
Décrets et arrêtés
Le décret est un acte règlementaire du gouvernement, qui précise la mise œuvre d’une loi. Il est signé par le Premier Ministre ou le Président de la République.
Les arrêtés sont des décisions administratives à portée nationale ou spécifique à une activité ou une zone géographique. Ils peuvent être pris par les Ministres, les Préfets ou les Maires.
Circulaires
La circulaire permet aux autorités administratives d’informer leurs services. Le plus souvent, elle est prise à l’occasion de la parution d’un texte afin de le présenter aux agents qui vont devoir l’appliquer. Elle doit se contenter d’expliquer le texte et ne peut rien ajouter. Par exemple, la circulaire prion de n°2001-138 (17) est devenue une instruction après sa révision en 2011 par l’instruction 449 (18).
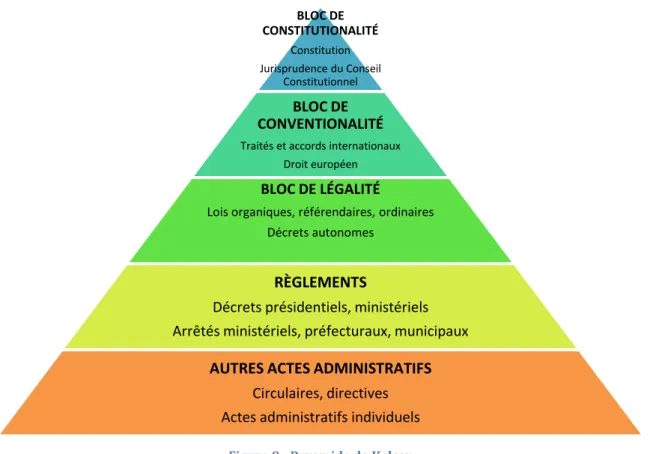
La hiérarchie des différents textes de loi peut être modélisée par la pyramide de Kelsen (Figure 9).
Figure 9 - Pyramide de Kelsen BLOC DE CONSTITUTIONALITÉ Constitution Jurisprudence du Conseil Constitutionnel BLOC DE CONVENTIONALITÉ
Traités et accords internationaux Droit européen
BLOC DE LÉGALITÉ
Lois organiques, référendaires, ordinaires Décrets autonomes
RÈGLEMENTS
Décrets présidentiels, ministériels Arrêtés ministériels, préfecturaux, municipaux
AUTRES ACTES ADMINISTRATIFS Circulaires, directives Actes administratifs individuels
40
Normes
Les normes concernant la stérilisation résultent de consensus internationaux (ISO) ou européens (CEN). Par définition, les normes sont d’application volontaire. Lorsque cela est jugé nécessaire, la France peut rendre obligatoire une norme comme unique moyen de mise en conformité avec une exigence.
Certaines normes sont qualifiées d’opposables, c’est-à-dire que la loi impose l’application du texte par tous.
Une norme doit être apposée du sigle NF pour être valable en France, puis EN si elles sont européennes ou ISO si elles sont internationales.
41
1.1.3.2. Processus opérationnel – Opérations et contrôles effectués en
stérilisation
Le processus de traitement des DMR doit être mis en œuvre selon les recommandations nationales en vigueur et en respectant les instructions du fabricant. Les procédures de traitement du DMR doivent tenir compte de l’évaluation du risque prion et respecter les règlementations en vigueur.
Le traitement s’impose à tous les DMR déconditionnés, qu’ils aient été utilisés ou non, ainsi qu’aux DMR retournés auprès du fabriquant pour maintenance.
Les procédures de traitement applicables à chaque catégorie de DMR sont documentées selon les principes définis par le système de management de la qualité.
Risque prion
Les Agents Transmissibles Non Conventionnels (ATNC), dont les prions, se caractérisent par leur grande résistance aux procédés chimiques ou physiques. En France, l’évaluation du risque prion est obligatoire avant tout acte invasif. Cette évaluation se base à la fois sur le statut du patient, suspect ou atteint, et sur le type de chirurgie réalisé (Tableau 2) (19).
En cas d’utilisation d’un DMR, l’évaluation du niveau de risque est transmise à l’unité de stérilisation afin que les DMR utilisés puissent être traités de façon adaptée.
L’instruction 449 (18) de 2011 a abrogé la circulaire 138 datant de 2001 (17). L’instruction 449 intègre les modifications de la classification du niveau de risque des tissus publiée par l’OMS en 2010 (20). Elle renforce le niveau de traitement appliqué aux DMR.
42 Tableau 2 – Détermination du niveau de risque prion, Instruction 449 – Fiche n°1
Patient ni suspect ni atteint Patient suspect ou atteint d’EST*
Patient
Pas de caractéristique
particulière.
Les patients présentant des
risques individuels d’EST*
(antécédent de traitement par hormone de de croissance d’origine humaine, de greffe de dure-mère d’origine humaine, antécédent d’un cas d’EST* dans la famille génétique)
Diagnostic suspecté sur la présence, d’apparition rapide et sans rémission, d’au moins un signe neurologique associé à des troubles intellectuels ou psychiatriques et après élimination de toute autre cause. Le diagnostic ne peut être confirmé qu’après examen neuropathologique.
Acte à risque pour tous les patients
Actes à risque pour les patients atteints ou suspects de MCJv** Actes à risque Neurochirurgie (à l’exclusion du rachis) Ophtalmologie chirurgicale
touchant la rétine ou le nerf optique
Chirurgie ou endoscopie ORL touchant la muqueuse olfactive
Actes à risque pour tous patients +
Actes invasif chirurgicaux avec contact, biopsie ou curage d’un ganglion, ou contact, biopsie ou exérèse d’une formation lymphoïde organisée, les intubations ou utilisations de masques laryngé, les endoscopies ou échographies passant par le carrefour aérodigestif, les endoscopies par voie rectale.
* EST = Encéphalopathies Spongiformes Transmissibles ** MCJv = variant de la Maladie de Creutzfeld Jakob
Ce classement nécessite une évaluation médicale, parfois spécialisée. Il est important que ce classement apparaisse clairement dans le dossier médical pour chaque patient pour lequel un acte à risque avec utilisation de DMR est programmé, afin que le classement soit connu avant la réalisation de l’acte et que le ou les DMR utilisés puissent faire l’objet d’un traitement adapté.
Quand le niveau du risque patient ne peut être déterminé - en cas d’urgence notamment - il est nécessaire, pour les interventions sur les tissus à haute infectiosité, d’appliquer les procédures de traitement des DMR permettant une inactivation totale, sans séquestrer les DMR (19).
43
Risque prion - Les mesures d’inactivation
L’inactivation peut être effectuée :
Au bloc opératoire par pré-désinfection combinée à une action de nettoyage avec un produit inactivant. Ce traitement remplace alors la pré-désinfection habituelle. Cette technique est peu réalisée.
Lors du lavage à la stérilisation, à l’aide d’un produit inactivant. Pour les patients suspects ou atteints, un trempage manuel est obligatoire, afin de récupérer les effluents. Un laveur-désinfecteur (LD) est néanmoins utilisable en cas de bypass de l’évacuation des eaux de lavage. Pour les actes à risque, l’utilisation d’un LD automatique est autorisée. La liste des produits inactivants est disponible sur le site de l’ANSM (21).
Lors de la stérilisation, si le procédé est reconnu inactivant total. La stérilisation par vapeur d’eau saturée à 134°C pendant 18 minutes possède un pouvoir inactivant, mais qui n’est pas total. Des procédés de stérilisation basse température, seuls ou combinés, présentent également des propriétés inactivantes totales.
Selon la fiche technique n°3 de l’instruction 449, le double nettoyage est requis (22) :
Pour tous les DMR non compatibles à la vapeur d’eau 134°C/18 minutes Pour les DMR utilisés chez un patient suspect ou atteint lors d’un acte à
risque (double nettoyage manuel). Les DMR sont ensuite séquestrés, et selon le diagnostic d’EST, seront détruits ou remis en service.
Il est nécessaire de vérifier auprès du fabriquant la compatibilité du procédé d’inactivation avec la nature du DMR. Si le DMR ne supporte pas le procédé d’inactivation, il sera détruit (par incinération à une température supérieure à 800°C).
Tout DMR en prêt ou de retour de réparation, maintenance ou prêt doit impérativement avoir suivi au préalable la procédure complète de traitement en fonction du risque, et doit être apporté avec l’attestation du traitement effectué (13).
44
Pré-désinfection
La pré-désinfection est la seule étape du processus de retraitement des DMR qui peut se faire en dehors de l’unité de stérilisation (13).
Elle répond à 3 objectifs :
Faciliter l’étape ultérieure de nettoyage en évitant le séchage des souillures Diminuer la population de micro-organismes
Protéger le personnel et l’environnement (23).
Elle doit avoir lieu dès que possible après l’utilisation des DMR, et au plus près du lieu d’utilisation.
La pré-désinfection manuelle par immersion est la technique la plus couramment utilisée. Elle se fait dans un bac dédié à l’aide de détergents désinfectants marqués CE et respectant les normes en vigueur. Dans les blocs opératoires, les bains sont à patient unique et renouvelés après chaque utilisation.
Dans le cas des DMR non immergeables, comme certains moteurs par exemple, il est conseillé d’essuyer soigneusement toutes les surfaces du DMR avec un linge propre imprégné de la solution de prétraitement et d’écouvillonner les parties creuses si besoin.
La pré-désinfection peut être réalisée à l’aide d’un laveur-désinfecteur dédié, on parle alors de pré-désinfection mécanisée. Elle est réalisée au plus près du lieu d’intervention. Elle simplifie le travail des professionnels et améliore leur protection, ainsi que la reproductibilité du prétraitement. Cependant, elle ne dispense pas du lavage en unité de stérilisation.
45
Nettoyage
« On ne stérilise bien que ce qui est propre » (24). Tout DMR doit être préalablement nettoyé avant stérilisation.
Le nettoyage est défini comme l’élimination de la contamination d’un article jusqu’au niveau requis pour son traitement ultérieur et pour l’utilisation à laquelle il est destiné (25). Elle fait la différence avec le lavage : élimination de la contamination sur les surfaces devant être nettoyées au moyen d’un milieu aqueux, contenant ou non des produits chimiques selon les besoins.
Le nettoyage concerne tous les DMR utilisés, ainsi que les DMR déconditionnées (utilisés ou non), périmés, en prêt ou dépôt, neuf ou de retour de réparation.
Sont également concernés par le nettoyage les contenants et paniers utilisés comme emballage de protection, ainsi que les accessoires de transports tels que les armoires.
Le nettoyage mécanisé en laveur-désinfecteur (LD) est préférable dès que possible, car plus reproductible que le nettoyage manuel. Ils associent tous deux une action mécanique à l’action physico-chimique des détergents. Le nettoyage par LD comprend quatre composantes, selon le cercle de Sinner (Figure 10) : une action mécanique (jets), une action chimique (détergents), une action thermique (phase de désinfection thermique du lavage à 93°C pendant 3 à 5 minutes), et le temps, soit la durée du nettoyage.
46 Figure 10 - Le cercle de Sinner
Le choix du procédé de nettoyage, sa mise en œuvre et le choix de produit prennent en compte les recommandations du fabricant du DMR (26) et du fabriquant des produits.
Des mesures spécifiques seront mises en œuvre en fonction de l’évaluation du risque prion, selon l’instruction 499 et le Protocole Standard Prion (21).
Les produits utilisés, ainsi que les laveurs-désinfecteurs doivent être conformes à la règlementation en vigueur (25). Il n’existe pas de normes sur les détergents, mais l’action désinfectante est normée (25) (27).
A l’issue du nettoyage, une vérification du bon déroulement du procédé (validation du cycle de lavage), de la propreté, de la siccité et de la fonctionnalité du DMR est réalisée.
Le processus de nettoyage s’inscrit dans le système de management de la qualité et fait l’objet d’une traçabilité. Les procédures doivent être rédigées et enregistrées dans le fond de gestion documentaire. Elles doivent être connues des personnes responsables de cette étape.
Les procédés doivent être validés (25), et les équipements maintenus et qualifiés.