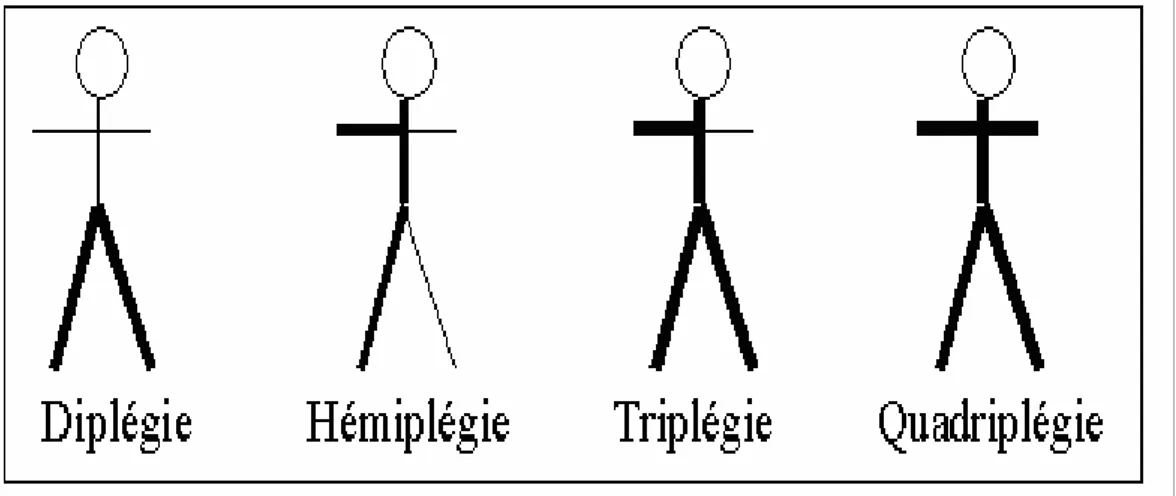
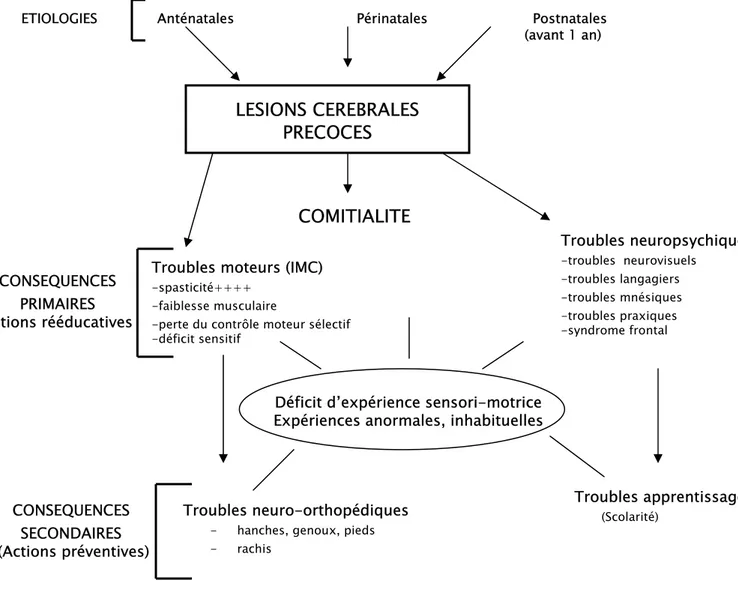
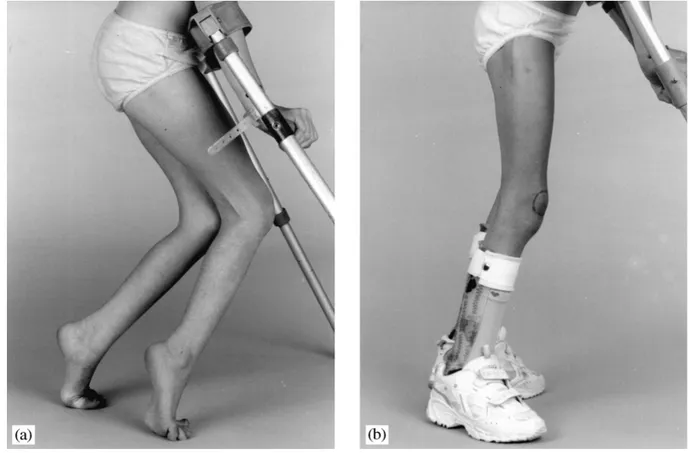
Aspects épidémiologiques, cliniques, thérapeutiques et évolutifs de la diplégie spastique à propos de 40 cas
Texte intégral
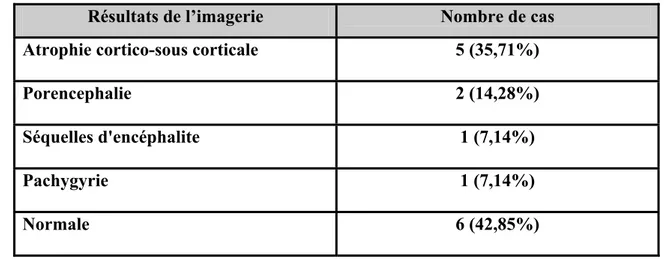
Figure

Documents relatifs
Quatre-vingt pour cent des patients porteurs de pompe a` Baclofe`ne intrathe´cal sont satisfaits et l’insatisfaction provient du fait de complications ou d’effets secondaires et non
Il s’agit d’une étude rétrospective et descriptive sur les fentes labio-palatines, réalisée du 1er Janvier 2011 au 31 Janvier 2013 dans le service d’odontostomatologie de
Nous avons inclus 50 patients opérés de Mal de Pott strictement dorsal à l’Hôpital Militaire de Niamey, à l’Hôpital National de Niamey, et dans certaines structures
Les anticorps anti récepteurs de la TSH ont été recherchés dans 50 cas (16,18%) des patients avec maladie de Basedow.. L’évolution sous traitement médical a été marquée
Au terme de notre étude dont l’objectif était d’étudier les aspects épidémiologiques, cliniques et thérapeutiques des OMA à l’HGD et à l’ HLD, il ressort que
Le traitement orthopédique était indiqué dans 2,5% des cas dans notre étude. Cette méthode de traitement a été utilisée dans les fractures non déplacées et stables,
18 Owing to a lack of studies looking at the use of antacids and mucosal protectants in managing GERD in pediatric patients, the 2018 Pediatric Gastroesophageal Reflux
In cerebral palsy, not all the conserved repertoire can be used; above all, the child is not always able to choose the best motor strategy to carry out a required task in