HAL Id: dumas-01681517
https://dumas.ccsd.cnrs.fr/dumas-01681517
Submitted on 11 Jan 2018HAL is a multi-disciplinary open access archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Diagnostic différentiel des lésions radio-opaques
maxillo-mandibulaires en imagerie dento-maxillo-faciale
Guillaume Taelman
To cite this version:
Guillaume Taelman. Diagnostic différentiel des lésions radio-opaques maxillo-mandibulaires en im-agerie dento-maxillo-faciale. Sciences du Vivant [q-bio]. 2017. �dumas-01681517�
AVERTISSEMENT
Cette thèse d’exercice est le fruit d’un travail approuvé par le jury de soutenance
et réalisé dans le but d’obtenir le diplôme d’État de docteur en chirurgie
dentaire. Ce document est mis à disposition de l’ensemble de la communauté
universitaire élargie.
Il est soumis à la propriété intellectuelle de l’auteur. Ceci implique une
obligation de citation et de référencement lors de l’utilisation de ce document.
D’autre part, toute contrefaçon, plagiat, reproduction illicite encourt toute
poursuite pénale.
Code de la Propriété Intellectuelle. Articles L 122.4
Except where otherwise noted, this work is licensed under
http://creativecommons.org/licenses/by-nc-nd/4.0/
UNIVERSITÉ PARIS DESCARTES
FACULTÉ DE CHIRURGIE DENTAIREAnnée 2017 N° 039
THÈSE
POUR LE DIPLÔME D’ÉTAT DE DOCTEUR EN CHIRURGIE DENTAIRE Présentée et soutenue publiquement le : 10 juillet 2017
Par
Guillaume TAELMAN
Diagnostic différentiel des lésions radio-opaques
maxillo-mandibulaires en imagerie dento-maxillo-faciale
Dirigée par M. le Docteur Benjamin Salmon
JURY
M. le Professeur Louis Maman Président
M. le Docteur Jean-Claude Tavernier Assesseur
M. le Docteur Thông Nguyen Assesseur
Mme. le Docteur Alice Guyon Assesseur
Remerciements
À M. le Professeur Louis Maman
Docteur en Chirurgie dentaire
Spécialiste qualifié en Chirurgie Orale
Professeur des Universités, Faculté de Chirurgie dentaire Paris Descartes Praticien Hospitalier, Assistance Publique-Hôpitaux de Paris
Doyen de la faculté de Chirurgie dentaire Paris Descartes
Qui me fait l’honneur de présider ce jury,
Je vous remercie pour votre soutien et la motivation que vous
m’avez apportée lorsque je vous ai exprimé ma volonté de me
présenter au concours de l’internat pour me former en
chirurgie orale. Veuillez trouver ici l’expression de mon plus
grand respect.
M. le Docteur Jean-Claude Tavernier
Docteur en Chirurgie dentaire
Docteur de l'Université Paris Descartes
Maître des Conférences des Universités, Faculté de Chirurgie dentaire Paris Descartes Praticien Hospitalier, Assistance Publique-Hôpitaux de Paris
Chevalier de l'ordre national du mérite Officier de l'ordre des palmes académiques
Qui m’a fait l’honneur de siéger dans ce jury,
Je vous remercie pour la bienveillance que vous avez eue
envers moi et les autres étudiants au cours de mes années
d’études à la faculté de Montrouge. Vous avez su transmettre
vos connaissances de manière claire et passionnante. Veuillez
trouver ici l’expression de mon plus grand respect.
À M. le Docteur Thông Nguyen
Docteur en médecine
Docteur de l’Université Paris 11
Ancien Interne des Hôpitaux de Bordeaux
Ancien Chef de Clinique-Assistant des Hôpitaux de Bordeaux Spécialiste en Chirurgie Plastique Reconstructrice et Esthétique Spécialiste en Chirurgie Maxillo-Faciale et Stomatologie
Maître des Conférences des Universités, Faculté de Chirurgie dentaire Paris Descartes Médecin Fédéral, Fédération Française du Sport Universitaire
Qui m’a fait l’honneur de siéger dans ce jury,
Je vous remercie de la formation et le soutien que vous m’avez donné lors de mes premiers pas en tant qu’interne en chirurgie orale. Vous avez su me guider et exiger de moi le nécessaire pour devenir un bon chirurgien. L’enseignement de qualité que vous m’avez fourni reste encore dans ma mémoire. Veuillez accepter mes plus sincères remerciements et trouver ici l’expression de mon plus profond respect.
À Mme. le Docteur Alice Guyon
Docteur en Chirurgie dentaire
Spécialiste qualifiée en Chirurgie Orale Ancienne interne des Hôpitaux
Assistante Hospitalo-Universitaire, Faculté de Chirurgie dentaire Paris Diderot
Qui m’a fait l’honneur de siéger dans ce jury,
Je te remercie pour tout le soutien que tu as pu m’apporter tout au long de l’internat. Je me souviens particulièrement du semestre passé comme co-internes à la Pitié-Salpêtrière. J’ai beaucoup apprécié l’aide que tu as eu l’occasion de me fournir lors des difficultés rencontrées.Ta bonne humeur, gentillesse et tes compétences font de toi une excellente enseignante en chirurgie orale. Je te prie de trouver ici, le témoignage de mon amitié et de ma reconnaissance.
À M. le Docteur Benjamin Salmon
Docteur en Chirurgie dentaire
Docteur de l'Université Paris Descartes Spécialiste qualifié en Chirurgie Orale
Maître des Conférences des Universités, Faculté de Chirurgie dentaire Paris Descartes Praticien Hospitalier, Assistance Publique-Hôpitaux de Paris
Qui m’a fait l’honneur de diriger cette thèse,
Je te remercie pour la qualité d’enseignement que tu m’as apporté. De m’avoir accompagné tout au long de ma formation pratique, à Colombes comme à Bretonneau mais aussi pour la rédaction de cette thèse. Ta passion pour la chirurgie orale et l’imagerie m’ont permis d’apprendre avec envie dans une ambiance très sympathique. Je te prie de prie de trouver en ces mots, l’assurance de ma gratitude.
À M. le Docteur Mickaël Samama
Docteur en médecine
Spécialiste qualifié en Chirurgie Orale Ancien interne des Hôpitaux de Paris
Praticien Hospitalier contractuel, Assistance Publique-Hôpitaux de Paris
Qui m’a fait l’honneur de siéger dans ce jury,
Je te remercie pour la motivation que tu m’as apportée au cours de l’internat, l’aide que tu m’as fournie particulièrement à la fin pour les examens et articles. J’ai aimé travaillé avec toi. Tu as selon moi toute les qualités d’un bon chirurgien. . Je te prie de trouver ici, le témoignage de mon amitié et de ma reconnaissance.
À mes parents, Pierre et Yvonne, qui ont toujours été là pour m’aider, me pousser au meilleur depuis le début. Ils ont su me donner la meilleure éducation possible, tout leur amour et ont joué leur rôle de parents à la perfection.
À mes grands-parents, Babcia , Dziadzia, Denise et Edouard, et leur bonne humeur permanente, mais surtout l’amour et le soutien qu’ils m’ont donné depuis toujours.
À ma sœur et mon frère, Marthe ou Mourthe :), têtue comme une mule mais le cœur sur la main. Lorenzo Marrano, plusieurs corde à son arc : architecte, musicien et coiffeur :P. Je vous remercie tous les deux car vous êtes toujours présents à mes côtés quoi qu’il arrive. Vous m’avez aidé à réviser lors de mes concours et donc contribué à mes études.
À mi amor, Matilde, qui partage ma vie, qui a dû supporter toutes les mésaventures avec moi mais m’a toujours soutenu et été de bon conseil. Gracias por estar a mi lado, tus consejos, me encanta la vida contigo.
À Noémi, la future Florence Foresti. Tu me feras toujours rire avec tes blagues.
Au reste de la famille, Thomas, Marion, Yoann, Pauline, Kiki et Titou , Pascale et Claude À Fab, mon deuxième frère, ami depuis toujours. Je pense que tu es le seul ami à nous connaître aussi bien. Trop peu de place pour dire tout ce qu’on a vécu. Je te remercie pour ton amitié fidèle, ta présence quand on a besoin de toi, ton écoute, le nombre incalculable de soirée etc….
À Lord Lancelot, the young pope, en plus d’être un très bon ami, j’apprécie ta détermination lorsque tu entreprends quelque chose.
À Olivier (NN), mon binôme de Créteil et qui m’a suivi dans les études depuis le collège jusqu’à la fac.
À mes compères, Jo (il y a toujours 1-0) et Phiras (et ta force surhumaine), toujours ensemble dans la galère des partiels, internat, Créteil etc…. Je repense à ces longues soirées à réviser et rigoler. À mes co-internes : J’ai eu la chance de vous rencontrer durant l’internat et j’ai pu passer de super moments avec vous. La team Bimax : JB le militaire blagueur , Paul Moulax le meilleur maxillo de Paris !, Marechou, Kikizal, mes ORL préférées : Marine et Sandine La baronne,. Les DescoB….. Alice et Mickael, Arthur, les cafés au ptit bret ! Gillou mon premier co-interne ! , Charles dit : « Albisexy » , Yona, Alexia.
À mes amis de fac : Pauline et superbe voix, Kim, qui a réussi a rattrapé ma boulette sur Saad, Alex, Val, Fafa, le lâcher de Farid !, Chamil et son humour trash, Jool et Sophie , Naila, Ratchouf, Habs et ceux de P1 : Milène, Tabchou, Sam, Eric etc…. toute une époque estudiantine que je n’oublierai jamais…
Aux amis de Sav : Chongky , Poulos et Lucho , Fu, « T’allica for life! » Anne-So , Laguertaïk, Loric , Cynthia, Jamel.
Et enfin merci à tous ceux que je n’ai pas mis et qui m’ont accompagné au cours de mes études ou ont contribué à ma formation.
Table des matières
ABRÉVIATIONS ... 3
INTRODUCTION ... 4
1: APPROCHE DIAGNOSTIQUE ... 5
1.1DESCRIPTION D’UNE IMAGE RADIOLOGIQUE PATHOLOGIQUE ... 5
1.2EVOLUTIVITÉ ET AGRESSIVITÉ DE LA LÉSION ... 6
1.1.1. Destruction et construction osseuse ... 6
1.1.2. Ostéogénèse périostée réactionnelle ... 7
1.1.3 Autres signes d’évolutivité ... 9
1.3ARGUMENTS DU DIAGNOSTIC ÉTIOLOGIQUE ... 9
2 : CLASSIFICATION DES IMAGES RADIO-OPAQUES ... 11
2.1.TUMEURS ET PSEUDO TUMEURS BÉNIGNES ... 11
2.1.1. Tumeurs Bénignes odontogènes ... 11
2.1.2. Tumeurs Bénignes Ostéogéniques ... 24
2.1.3 Tumeurs Bénignes Chondrogéniques ... 31
2.2.LÉSIONS FIBRO-OSSEUSES ... 35
2.2.1. Fibrome cémento-ossifiant = fibrome ossifiant ou cémentifiant ... 35
2.2.2. Dysplasies cémento-osseuses (dysplasies osseuses) ... 37
2.2.3. Dysplasie Fibreuse et Syndrome de McCune–Albright ... 39
2.3.TUMEURS MALIGNES ... 42
2.3.1 Tumeurs Malignes Odontogènes ... 42
2.3.2 Tumeurs Malignes Non Odontogènes ... 44
2.4.NON TUMORALE ... 51
2.4.1 Origine infectieuse : Ostéites et ostéomyélites chroniques ... 51
2.4.2 Origine ischémique : Infarctus osseux ... 55
2.4.3 Origine dystrophique ... 56
2.4.5 Origine iatrogène ... 59
2.5CALCIFICATIONS DES TISSUS MOUS ... 61
2.5.1 Lithiases salivaires ... 61
2.5.2 Calcifications musculaires ... 62
2.5.3 Calcifications vasculaires ... 63
2.5.5 Tonsillolithes ... 64 2.5.6 Calcification du ligament styloïdien : « styloïde longue »... 64
3 : SCHÉMAS DIAGNOSTICS ... 66 CONCLUSION ... 68 TABLE DES FIGURES ... 74 TABLE DES TABLEAUX ... 76 ANNEXES ... 77
Abréviations
DF : Dysplasie Fibreuse
DCO : Dysplasie Cémento-Osseuse
FO : Fibrome Ossifiant
FOA : Fibro-Odontome Améloblastique
FDA : FibroDentinome Améloblastique
FOC : Fibrome Odontogène Central
FOP : Fibrome Odontogène Périphérique
FOJ : Fibrome Ossifiant Juvénile
MO : Myosite Ossifiante
OMS : Organisation Mondiale de la Santé
WHO : World Health Organisation
Introduction
Une image radiographique médicale est obtenue en projetant un faisceau de rayons X sur un corps qui les absorbe différemment selon la nature des tissus traversés. Plus l’organe est dense, plus il apparaitra blanc sur la radiographie, on parle ainsi de radio-opacité tandis que les tissus ou organes mous apparaitront plus noir, désigné sous le nom de radioclarté.
En imagerie dento-maxillo-faciale, les éléments anatomiques radio-opaques sont représentés par les structures minéralisées: les dents, les os mandibulaire et maxillaire, le complexe stylo-hyoïdien, la base du crâne et les vertèbres cervicales. Cependant, le terme « radio-opaque » est fréquemment utilisé uniquement pour nommer des lésions pathologiques impliquant un processus de
minéralisation anormale1.
Des images radio-opaques maxillo-mandibulaires sont souvent découvertes fortuitement lors d’examen de contrôle radiographique de routine, ou, plus rarement suite à une symptomatologie amenant le patient à consulter.
Le diagnostic de ces images denses peut s’avérer plus ou moins difficile du fait de la variabilité de manifestation de certaines lésions, ou encore les similarités d’apparition de plusieurs lésions. En effet, une même pathologie peut créer une image ostéolytique en phase immature et se calcifier au fur et à mesure de son évolution. On observe ainsi, pour une même lésion, différentes images évoluant de la simple lacune osseuse à une image dense uniforme, avec des stades intermédiaires mixtes associant radioclarté à une quantité de radio-opacité variable selon le stade de maturité. De plus, certains processus tumoraux, dysplasiques ou infectieux aboutissent radiologiquement à des images très semblables entrainant une difficulté supplémentaire dans l’analyse de ces lésions. L’objectif de cette thèse est de présenter les éléments radiologiques et une méthodologie
permettant d’orienter le diagnostic vers un type de pathologie. L’ensemble des lésions tumorales, infectieuses, dystrophiques ou à corps étranger pouvant se manifester par une image hyperdense dans les os maxillaires ou mandibulaires seront décrites pour aboutir à des schémas diagnostics récapitulatifs permettant d’orienter le praticien dans la prise en charge d’un patient présentant ce type de lésion.
1 : Approche diagnostique
Les images hyperdenses maxillo-mandibulaires peuvent se présenter sous la forme d’une lésion solitaire, multiple ou diffuse.
La simple image radiologique ne suffit pas toujours pour établir un diagnostic précis d’une lésion. La démarche vise à analyser la lésion afin d’orienter le diagnostic vers une « catégorie » de lésion et ainsi établir la prise en charge de celle-ci.
Après avoir réalisé une description radiologique précise en les associant aux éléments cliniques, cette démarche s’établit en deux temps2 : d’abord, apprécier le degré d’évolutivité, d’agressivité de la lésion puis rechercher les arguments permettant un diagnostic.
1.1 Description d’une image radiologique pathologique
Plusieurs éléments doivent être rapportés afin d’établir une description précise de la lésion.
1- Nombre d’os atteints : polyostotique ou monoostotique :
L’image peut se manifester sur un seul os, elle est alors monoostotique ou tandis que d’autres lésions peuvent atteindre plusieurs os : lésion polyostotique.
2- unicité/multiplicité: Une image unique se présente comme une lésion solitaire isolée mais peut aussi se composer de plusieurs images du même aspect (lésion multiples).
3- Densité : Les images radiographiques pathologiques prennent différents aspect selon leur contenu. Une diminution de la densité se manifeste par une image radioclaire, elle peut être focale : lytique ou généralisé : ostéopénie. Une augmentation de la densité est décrite comme radio-opaque ou sclérose osseuse dont la tonalité varie en fonction de l’importance de la minéralisation de la lésion. Enfin les images mixtes peuvent associer des éléments d’ostéocondensation et d’ostéolyse en quantité variable.
4- Localisation : La lésion siège-t-elle sur l’os maxillaire ou mandibulaire, dans un secteur denté ou édenté, dans la partie postérieur, latérale ou médiane de l’os atteint, périphérique ou intra-osseuse ? 5- Etendue/ Taille : La lésion reste elle confinée à un secteur ou s’étend –t-elle sur l’ensemble de l’os ? Le volume de la lésion nécessite d’être évalué.
2 Nahum, Traité d’Imagerie médicale.
6- Fond : Il peut être homogène ou inhomogène, traversée par des cloisons (nid d’abeille / bulle de savon), ou possédant des calcifications (matrice cartilagineuse, osseuse ou densité dentaire) 7- Limites : Les contours des lésions informent sur l’agressivité de la lésion. Des limites nettes ou bordées d’un liseré d’ostéocondensation orientent vers un processus bénin tandis que des limites floues, mal définies sont signes d’une lésion agressive, de progression rapide, ayant tendance à l’envahissement.
8- Structures anatomiques environnantes : rapport et état
- Dent : Les dents voisines sont-elles déplacées (refoulement par la tumeur)? Les racines sont-elles en rhizalyse ? De nombreuses lésions bénignes et certaines lésions malignes peuvent entrainer une résorption des dents adjacentes. Y-a-t ’il des dents incluses ? La présence d’une tumeur au voisinage des germes peuvent créer un obstacle à son éruption.
L’intimité de la lésion avec les racines dentaires est un élément non négligeable du diagnostic différentiel (exemple : différence entre l’ostéoblastome et le cémentoblastome bénin).
L’état dentaire (présence de carie, délabrement) peut être la cause de certaines lésions (exemple : ostéite condensante).
- Os : l’état de la corticale osseuse doit être défini : soufflure corticale, amincissement ou érosion corticale ou discontinuité (rupture), épaississement cortical, réaction périostée.
- Sinus et fosse nasale
- Canal dentaire inférieure : il peut être intact, refoulé ou envahit.
1.2 Evolutivité et agressivité de la lésion
1.1.1. Destruction et construction osseuseLa réaction de l’os est variable, il peut se détruire (ostéolyse) ou construire
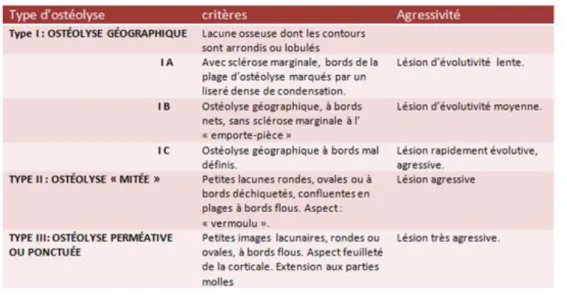
La destruction peut prendre plusieurs aspects décrits par la classification de Lodwick (Tableau 13) utilisée pour évaluer l’évolution et l’agressivité de la lésion.
Lorsque la condensation osseuse est franche et bien délimitée, elle évoque une lésion d’évolution lente tandis que, lorsqu’elle est non homogène, à limites floues et imprécises, elle évoque une évolution rapide. Une couronne de condensation autour d’une ostéolyse focale est signe d’une évolution lente.
Tableau 1 Classification des ostéolyses de Lodwick
Source : Lodwick et al. « Determining growth rates of focal lesions of bone from radiographs, 1980
1.1.2. Ostéogénèse périostée réactionnelle
La réaction périostée ou apposition périostée est une réaction osseuse par ostéogénèse en réponse à une atteinte de la corticale. Cette néo-ossification qui se forme au contact de la corticale, peut prendre différents aspects dépendant de la nature du processus causal, de son agressivité et de la durée d’évolution.
. Réaction périostée homogène pleine, hyperostosante = réaction périostée compacte
Cette réaction entraine un épaississement de l’os cortical sous le périoste (ostéogénèse sous périostée). L’ hyperostose corticale prend l’aspect d’une couche homogène d’os compact incorporé dans la corticale sous-jacente (absence d’espace radioclaire entre la réaction périostée et la corticale). Elle est le signe d’une évolution lente.
Lorsque cette réaction périostée est associée à une ostéolyse géographique endostéale, elle prend le nom d’expansion corticale ou soufflure corticale.
. Réaction périostée unilamellaire
Elle n’est faite que d’une seule couche et prend l’aspect d’une ligne dense parallèle à la surface osseuse, séparée de la corticale par un espace millimétrique hypodense par rapport à la corticale.
Elle correspond à une évolution lente et est quasi pathognomonique d’un processus bénin surtout lorsqu’elle est épaisse. Elle est retrouvée dans l’ostéomyélite aiguë, le granulome éosinophile, l’ostéome ostéoïde, les fissures de stress ou par insuffisance osseuse.
. Réaction périostée lamellaire ou plurilamellaire
Elle est composée de plusieurs couches de tissu osseux parallèles au périoste et prend l’aspect dit « en bulbe d’oignon » (multiples lignes de condensation parallèles à la corticale en regard d’une lésion osseuse).Cette réaction périostée traduit une évolution rapide de la lésion, d’agressivité cependant moins importante que la réaction spiculée.
. Réaction périostée spiculée
Cette réaction périostée se manifeste par des images de densité calcique en spicules condensées perpendiculaires à la surface corticale. La hauteur et l’épaisseur des spicules sont variables. Elle peut prendre différents aspects45:
-« en feu d’herbe » ou « poil de brosse » : les spicules sont perpendiculaire à la surface corticale sur tout le long de la réaction périostée.
- « en coucher de soleil » ou « rayon de soleil » : les spicules divergent du centre vers la périphérie de la réaction périostée.
-« en velours » lorsque les spicules sont courts et serrés.
Les spicules peuvent être disposées de manière irrégulières ou encore mixtes en prenant plusieurs aspects décrits précédemment.
Cette spiculation est un signe d’agressivité de la lésion, d’évolution rapide. Souvent associée à une lésion tumorale maligne (ostéosarcome, sarcome d’Ewing, métastase condensante), elle est aussi observée dans d’autres circonstances comme une infection chronique des tissus mous sous-jacents, le granulome éosinophile, la syphilis osseuse. Cependant elle n’est jamais présente dans
l’ostéomyélite.
. L’éperon périosté ou triangle de Codman
L’éperon périosté correspond à une réaction périostée principalement plurilamellaire interrompue par la destruction corticale et l’envahissement des tissus mous.
4 Arrivé et al., Guide de sémiologie en scanner. 5 Nahum, Traité d’Imagerie médicale.
Il apparait comme une expansion corticale triangulaire discontinue dont le sommet a été détruit. Il est le signe d’une évolution rapide (tumeurs malignes) mais est aussi rencontrés dans d’autres contextes (hématomes sous périosté, ostéomyélite)
. Lésion osseuse étendue aux parties molles
L’envahissement de la tumeur dans les parties molle correspond à une extension par contiguïté d’une lésion osseuse aux tissus mous adjacents. Elle survient lors de lésions agressives.
1.1.3 Autres signes d’évolutivité
D’autres signes peuvent évoquer une évolution lente tel qu’un refoulement des structures anatomiques adjacentes sans destruction, un allongement osseux, une incurvation ou encore un défaut de modelage de l’os6.
1.3 Arguments du diagnostic étiologique
D’autres critères sont à mettre en avant lors de la démarche diagnostic : l’étendue de l’atteinte osseuse, la localisation sur le squelette les calcifications de la matrice tumorale ou encore l’âge, sexe et fréquence7.
. Etendue de l’atteinte osseuse :
Certaines tumeurs restent localisées dans une région tandis que d’autres (ostéomyélite, dysplasie osseuse floride…), ont tendances à s’étendre et envahir rapidement l’os.
. Localisation sur le squelette :
Certaines lésions se localisent préférentiellement sur un os donnés ou encore sur un site spécifique d’un os. Par exemple, les tori siègent sur la corticale interne mandibulaire dans la région
antérolatérale ou dans la partie médiane du palais dur.
. Age, sexe, ethnie, fréquence :
Certaines tumeurs sont rencontrées plus fréquemment chez l’enfant, parmi celles-ci, certaines surviennent préférentiellement à la première décennie ou la deuxième (sarcome d’Ewing).
Inversement certaines tumeurs apparaissent plus tardivement. En effet les ostéosarcomes
6 Ibid.
mandibulaires apparaissent entre la troisième et quatrième décennie. La dysplasie osseuse floride se rencontre principalement chez les femmes noires d’âge moyen.
. Calcification de la matrice tumorale :
Les caractéristiques tomodensitométriques intralésionnelles d’une lésion orientent le diagnostic. On parle de « matrices ».
La matrice cartilagineuse prend l’aspect de petites calcifications denses, ponctiformes ou en grains de tailles irrégulière mais encore de calcifications floconneuses, arciformes ou annulaires. Cette matrice évoque une tumeur cartilagineuse (enchondrome, chondroblastome, chondrosarcome)8. La matrice osseuse ou ostéoïde se présente comme une plage de condensation relativement homogène de tonalité nuageuse, dense compacte ou d’aspect os trabéculaire9.
De nombreuses lésions peuvent prendre cet aspect (ostéochondrome, ostéosarcome parostéal ou ostéogénique, myosite ossifiante au stade d’état, îlot condensant bénin, métastase osseuse condensante).
8 Arrivé et al., Guide de sémiologie en scanner. 9 Ibid.
2 : Classification des images radio -opaques
2.1. Tumeurs et pseudo tumeurs Bénignes
Une tumeur est le nom donné à une production pathologique (prolifération excessive de cellules) constitué par un tissu de nouvelle formation très proche d’un tissu normal. Les tumeurs bénignes ont une évolution lente, composées de cellules normales et ne donnant pas de métastases, elles ne récidivent pas ou rarement après exérèse complète. Les pseudo-tumeurs sont des masses d’origine inflammatoire, dystrophique ou malformatif.
2.1.1. Tumeurs Bénignes odontogènes
2.1.1.1. Tumeurs odontogènes Epithéliales :
Ces tumeurs sont constituées d’un épithélium odontogène avec un stroma fibreux mature, sans ectomésenchyme odontogène
. Tumeur de Pindborg ou tumeur odontogène épithéliale calcifiée
La tumeur de Pindborg est, selon l’OMS10, une néoformation épithéliale odontogène bénigne rare, localement invasive, représentant moins de 1% de toutes les tumeurs odontogènes11.
Elle est composée de cellules épithéliales produisant une substance amyloïde pouvant se calcifier. L’âge d’apparition est variable : entre 20 et 60ans.
Localisation :
Elle se situe majoritairement dans les secteurs postérieurs de la mandibule (deux tiers des cas pour un tiers au maxillaire)12, et peut se présenter comme une tumeur intraosseuse (centrale) ou extra osseuse (périphérique, beaucoup plus rare).
10 Centre international de recherche sur le cancer, Pathology and genetics of head and neck tumours. 11 More et Vijayvargiya, « Intraosseous calcifying epithelial odontogenic (Pindborg) tumor : a rare entity ». 12 Ching et al., « CT and MR imaging appearances of an extraosseous calcifying epithelial odontogenic tumor
Aspect radiologique :
Variable selon le stade de développement, elle apparait principalement comme une image mixte : masse radioclaire et opaque, traversée par de nombreuses petites travées irrégulières donnant un effet «flocon de neige ».Sa taille varie avec l’évolution de la lésion13.
La tumeur peut présenter cinq caractéristiques radiographiques selon Ching and Coll. 200014 : - Radioclarté péricoronaire (associée à une dent incluse).
- Opacité diffuse comportant des zones claires.
- Mixte : mélange de zones radioclaires et de zones opaques, sans relation avec une dent incluse. - Phénomène dit de «neige fraîche » : en majeure partie radioclaire, avec des «flocons» radio-opaques dus aux taches éparses de calcifications.
- Lésion opaque solide
Une modification de la position des dents peut se produire, ainsi que des résorptions radiculaires.
Evolution et pronostic :
C’est une tumeur à croissance lente et la transformation maligne est exceptionnelle. Un diagnostic et énucléation précoce est essentiel pour éviter la déformation et destruction oro-maxillo-faciale15.
Les récidives sont rares mais possibles.
Figure 1. Tumeur de Pindborg mandibulaire droite sur panoramique dentaire et TDM.
Source : More et Vijayvargiya, « Intraosseous calcifying epithelial odontogenic (Pindborg) tumor », 2015
13 More et Vijayvargiya, « Intraosseous calcifying epithelial odontogenic (Pindborg) tumor : a rare entity ». 14 Ching et al., « CT and MR imaging appearances of an extraosseous calcifying epithelial odontogenic tumor
(Pindborg tumor) ».
2.1.1.2 Tumeurs Odontogènes Mixtes
Ces tumeurs sont constituées d’un épithélium odontogène et un ectomésenchyme odontogène, associé ou non à la formation de tissus durs.
. Tumeur odontogène kystique calcifiée ou Kyste de Gorlin
Anciennement nommé kyste odontogène calcifié, il était classé comme tumeur par l’OMS 16 pour être, plus récemment, classé comme kyste (OMS, 2017) et représentait 2% des tumeurs
odontogènes17. Cette néoformation, possédant des caractéristiques histologiques similaires aux kystes et aux tumeurs bénignes odontogènes18, est constituée d’un épithélium bordant semblable à celui de l’améloblastome, ainsi que de « cellules fantômes » pouvant se calcifier. Elle apparait durant la deuxième décennie de vie sans prédilection entre les genres.
Clinique :
Le kyste de Gorlin apparait comme une tuméfaction osseuse indolore sans caractéristique spécifique.
Localisation :
Intra-osseux (le plus souvent) ou extra-osseux, il se situe, dans deux tiers des cas, dans la région antérieure des mâchoires (maxillaire et mandibule de manière équitable) et est souvent associé à d’autres lésions (odontome principalement, améloblastome, fibrome améloblastique)19.
Aspect radiographique :
Les caractéristiques radiographiques ne sont pas pathognomoniques, on observe une image radioclaire ostéolytique généralement uniloculaire, plus rarement multiloculaire avec des calcifications au sein de la lésion dans 30 à 50% des cas20.
16 Centre international de recherche sur le cancer, Pathology and genetics of head and neck tumours. 17 Knezević et al., « Calcifying odontogenic cyst--Gorlin’s cyst--report of two cases ».
18 Centre international de recherche sur le cancer, Pathology and genetics of head and neck tumours. 19 Knezević et al., « Calcifying odontogenic cyst--Gorlin’s cyst--report of two cases ».
20 Khandelwal, Aditya, et Mhapuskar, « Bilateral calcifying cystic odontogenic tumour of mandible: a rare case
Evolution et pronostic :
Bien que histologiquement très proche des tumeurs odontogènes épithéliales calcifiées, elle
présente une croissance moins agressive21Erreur ! Signet non défini.. Après énucléation, il n’y a pas de récidive, hormis pour les formes intra-osseuses.
. Tumeur odontogène adénomatoïde
Elle est décrite comme une tumeur composée d’un épithélium odontogène ayant une architecture variable, intégré dans un tissu conjonctif mature et caractérisé par une croissance lente mais progressive22 . Ce néoplasme, qui représente 2 à7% des tumeurs odontogènes23 est aussi appelée tumeur «deux tiers», car deux tiers touche les jeunes femmes, deux tiers sont localisées dans le maxillaire, deux tiers sont associées à une canine et deux tiers sont associés à une dent incluse24. Il existe plusieurs types de Tumeur Odontogène Adénomatoïde : deux formes intra-osseuses, les plus fréquentes : Folliculaire (73% des cas) entourant une dent, Extra-folliculaire (24% des cas) n’est pas associé à une dent et une forme Périphérique beaucoup plus rare située dans les tissus mous de la gencive antérieure maxillaire principalement25.
Clinique :
Cette tumeur de croissance très lente reste longtemps asymptomatique. En évoluant elle peut se manifester par une tuméfaction osseuse dure non douloureuse ou faiblement douloureuse.
Radiologie26 :
La variante folliculaire intra-osseuse est radiologiquement semblable à un kyste dentigère, elle s’observe comme une image radioclaire uniloculaire bien délimitée entourant la couronne et la racine d’une dent permanente retenue ou incluse.
La variante extra-folliculaire est représentée par une lacune bien délimitée intra-osseuse. La majorité des formes intra-osseuses (deux tiers27) peuvent présenter de discrets foyers de calcifications apparaissant comme des « mouchetures radio-opaques ».
21 Knezević et al., « Calcifying odontogenic cyst--Gorlin’s cyst--report of two cases ».
22 Centre international de recherche sur le cancer, Pathology and genetics of head and neck tumours. 23 Ibid.
24 Dhupar, Akkara, et Khandelwal, « An unusually large aggressive adenomatoid odontogenic tumor of maxilla
involving the third molar: A clinical case report ».
25 Ibid. 26 Ibid.
Evolution, Pronostic :
Cette tumeur bénigne possède une croissance très lente dont la taille est comprise entre 1 et 3 cm. Cependant il existe quelques rares cas de tumeurs agressives atteignant des volumes importants28. La lésion est traitée par énucléation et curetage, les récidives sont très rares.
Figure 2. Tumeur Odontogène Adénomatoïde volumineuse associée à une troisième molaire incluse
Source : OMS « Pathology and Genetics of Head and Neck Tumours. », 2005
Fibro-odontome améloblastique et dentinome
Le fibro-odontome améloblastique est un néoplasme extrêmement rare présentant les
caractéristiques histologiques d’un fibrome améloblastique (conjonctif riche en cellules semblable à la papille dentaire ainsi que d’épithélium odontogène primitif et bourgeon dentaire) associé à la formation de tissus dentaires durs : dentine et émail29, due à des phénomènes d’induction épithélio-conjonctive.
Lorsque le tissu dentaire est constitué de dentine dysplasique, on parle de fibrodentinome améloblastique (FDA) ou dentinome tandis que lorsque le phénomène d’induction est majoré et aboutit à la formation d’émail et dentine, la tumeur prend le nom de fibro-odontome améloblastique (FOA).
28 Dhupar, Akkara, et Khandelwal, « An unusually large aggressive adenomatoid odontogenic tumor of maxilla
involving the third molar: A clinical case report ».
La nature et les interrelations du Fibrome Améloblastique, FOA, FDA et odontomes sont encore controversées. Certains FOA et FDA seraient de nature hamartomateuse et pourraient être un stade immature de l’odontome complexe30.
Cependant, selon la récente classification de l’OMS (2017), le consensus a été que ces tumeurs, une fois la formation de tissus durs produite, sont susceptibles de devenir des odontomes et sont donc classées comme des odontomes en développement et non comme des tumeurs indépendantes31. Ainsi, le fibrome améloblastique serait distinct des autres tumeurs odontogènes mixtes, ne pouvant pas évoluer vers d’autres lésions plus différenciées et ne serait pas à l’origine de ces lésions.
Clinique :
Ces lésions sont observés principalement chez des sujets jeunes (enfance à adulte jeune)32, préférentiellement de sexe masculinet se présente comme une tuméfaction d’évolution lente et asymptomatique33.
Localisation :
Ils se développent majoritairement dans la partie post de la mandibule3435(dans la moitié à deux
tiers des cas36Erreur ! Signet non défini.).
Aspect radiologique :
Ils se présentent comme une image radioclaire uniloculaire dans 90% des cas37 ou multiloculaire, bien circonscrite, associée à différents degré d’opacification, selon l’étendue de la minéralisation38, formant des foyers de calcification de tailles variables.
Une dent incluse ou enclavée est souvent associée à la lésion.
Le diagnostic différentiel entre le FDA, FOA et odontomes complexes est radiologiquement impossible.
30 Buchner, Kaffe, et Vered, « Clinical and radiological profile of ameloblastic fibro-odontoma: an update on an
uncommon odontogenic tumor based on a critical analysis of 114 cases ».
31 Wright et Vered, « Update from the 4th edition of the World Health Organization classification of head and
neck tumours : odontogenic and maxillofacial bone tumors ».
32 Bhargava, Sood, et Rathore, « Ameloblastic fibrodentinoma : report of a case in an infant ». 33 Ibid.
34 Ibid.
35 Giraddi et Garg, « Aggressive atypical ameloblastic fibrodentinoma: Report of a case ».
36 Buchner, Kaffe, et Vered, « Clinical and radiological profile of ameloblastic fibro-odontoma: an update on an
uncommon odontogenic tumor based on a critical analysis of 114 cases ».
37 Ibid.
Evolution et pronostic :
Cette tumeur à croissance lente peut atteindre des dimensions importantes. Elle présente un très faible risque de récidive après exérèse39 .
Le risque transformation maligne (fibrodentinosarcome améloblastique et fibro-odontosarcome améloblastique) est rare40, mais augmente avec les récurrences41, et justifie donc la nécessité de suivi régulier.
Figure 3. Image radiographique d’un fibro-odontome améloblastique
Source : OMS, « Pathology and Genetics of Head and Neck Tumours. » 2005
. Odontomes
Les odontomes sont les tumeurs odontogènes les plus fréquentes (22% de toutes les tumeurs odontogènes42). Il s’agit d’hamartomes (malformations tissulaires d’aspect tumoral) dans lesquels dentine, cément, tissu pulpaire et émail sont présents.
Ils se développent à partir des composants épithéliaux et mésenchymateux de l'appareil dentaire, produisant l’émail et la dentine. Ils sont fréquemment associés à un trouble se déroulant pendant la dentition primaire (traumatisme, inflammation, infection), des anomalies héréditaires (Syndrome de Gardner43 ou Syndrome d’Hermann), une hyperactivité odontoblastique et autres modifications intervenant dans le contrôle de l’odontogénèse44.
Il existe 2 types d’odontomes : complexe et composé.
39 Bhargava, Sood, et Rathore, « Ameloblastic fibrodentinoma : report of a case in an infant ». 40 Ibid.
41 Giraddi et Garg, « Aggressive atypical ameloblastic fibrodentinoma: Report of a case ».
42 Gedik et Müftüoğlu, « Compound odontoma : differential diagnosis and review of the literature ». 43 Macdonald, Oral and maxillo facial radiology : a diagnostic approach.
L’odontome composé récapitule l'organisation d'une dent normale, tandis que l’odontome complexe apparaît comme une masse de tissu désorganisé odontogène dur4546.
Ils peuvent survenir à tout âge mais apparaissent préférentiellement lors des deux premières décennies de vie, avec une fréquence légèrement plus élevée chez les femmes.
Inhibant l’éruption de dents adjacentes, les odontomes sont souvent associés à des dents incluses ou en malpositions.
Cliniquement :
Asymptomatique le plus souvent, on peut tout de même retrouver des anomalies d’éruption des dents lactéales ou permanentes, ainsi que des douleurs et une tuméfaction osseuse.
Parfois, l’odontome peut faire son éruption et être visible à l’examen endobuccal (Figure 4).
Odontome complexe :
Les odontomes complexes se situent dans les zones dentées postérieures des mâchoires, principalement dans la région postérieure mandibulaire. Généralement inférieur à 3 cm, sa taille peut atteindre jusqu’à 6 cm de diamètre47.
Aspect radiologique :
Ils apparaissent comme une masse radiodense de tissus durs entourée d’une zone radioclaire plus ou moins large selon le stade de développement de l’odontome (plus large chez un odontome complexe en développement)
Figure 4. Odontome Complexe ayant fait sont éruption (orthopantomogramme et clinique)
Source : Bagewadi et al., « Unusually large erupted complex odontoma »,2015
45 Ibid.
46 Macdonald, Oral and maxillo facial radiology : a diagnostic approach.
Odontome composé :
L’odontome composé est la plus commune de toutes les tumeurs odontogènes. Il se situe préférentiellement dans la région antérieure du maxillaire.
Le diamètre se situe entre 1 et 2 centimètres avec possibilité d’atteindre 6 centimètres dans certains cas48.
Aspect radiologique :
Il se présente comme une collection de structures semblables à des dents (odontoïdes) entourée d’une zone radioclaire49.
Cet ensemble de structure odontoïde est retrouvé macroscopiquement, entouré d’un capsule fibreuse permettant d’établir le diagnostic final après exérèse à la vue de l’odontome composé50.
Figure 5. Odontome Composé provoquant la rétention de la première prémolaire mandibulaire gauche
Source : Kale et al., « Management of a Massive Compound Odontoma in a 9-Year Child »,2016
Pronostic et évolution :
La croissance des odontomes composés et complexes est lente et s’arrête lorsque l’odontome arrive à maturité. Très rarement, ils peuvent faire leur éruption dans la cavité buccale.
Il n’y a pas de récidive lorsque l’exérèse a été complète.
. Odonto-améloblastomes
Aussi dénommé odontome améloblastique, cette tumeur odontogène mixte survient très rarement. Elle possède les caractéristiques de l’odontome et de l’améloblastome combinées51. Elle atteint des patients jeunes. 48 Ibid. 49 Ibid. 50 Ibid. 51 Ibid.
Elle se localise au maxillaire comme à la mandibule, préférentiellement en distale des canines, dans les régions prémolaire/molaire52.
Clinique :
Au départ se présente comme une masse indolore. Le volume de la tumeur entraine l’apparition de signes cliniques : tuméfaction osseuse, déplacements dentaires, retard d’éruption, douleurs sourdes.
Aspect radiologique :
L’odonto-améloblastome apparait comme une image radioclaire uniloculaire ou multiloculaire bien circonscrite à l’intérieur de laquelle se trouve une quantité variable de radio-opacité. Des dents incluses et résorptions radiculaires à proximité de la lésion peuvent être observées.
La distinction avec le fibro-odontome améloblastique et l’odontome complexe est très difficile, et nécessite l’appui de l’analyse histologique.
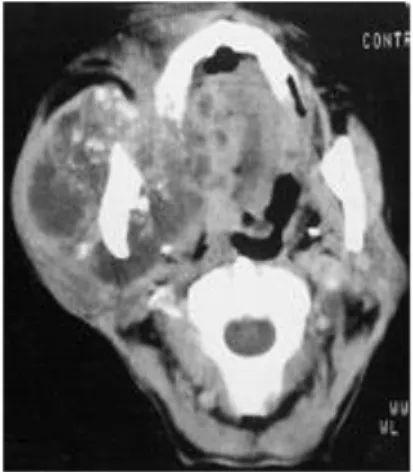
Figure 6. Odontoaméloblastome ( Image TDM et panoramique dentaire) : image lytique uniloculaire avec calcification intralésionnelle et dent incluse.
Source : Kudoh et al., « Massive odontoameloblastoma arising in the maxilla »,2015
Pronostic et évolution :
Cette tumeur possède un comportement similaire à l’améloblastome, elle est localement agressive, les récidives sont fréquentes (Mosqueda-Taylord and coll en 2002 rapporte 2 récurrences sur 12 cas dont un cas de récurrence double53) et la transformation maligne est possible. De ce fait elle
nécessite d’être traitée de la même manière que l’améloblastome avec une large excision et un suivi à long terme (minimum 5ans)54.
52 Kudoh et al., « Massive odontoameloblastoma arising in the maxilla: a case report ».
53 Mosqueda-Taylor et al., « Odontoameloblastoma. Clinico-pathologic study of three cases and critical review of
the literature ».
2.1.1.3 Tumeurs odontogènes conjonctives :
Ces tumeurs sont composées d’un mésenchyme et/ou ectomésenchyme odontogène avec ou sans épithélium odontogène.
. Fibrome odontogène
Le fibrome odontogène est une tumeur extrêmement rare (0 ,1% des tumeurs odontogènes55) caractérisée par une quantité variable d’épithélium inactif incorporé dans un stroma fibreux mature56. Il en existe deux types : fibrome odontogène simple ou pauvre en cellule épithéliale et fibrome odontogène type O.M.S ou riche en cellules épithéliales57.
Sa localisation peut être intra-osseuse : Fibrome odontogène central (FOC) ou extra-osseuse : Fibrome odontogène Périphérique (FOP), situé dans la muqueuse gingivale.
Clinique :
Le FOP apparait comme un nodule sessile recouvert de muqueuse semblable à la muqueuse gingivale environnante.
Le FOC entraine une expansion corticale indolore.
Radiologie :
Il se présente comme une image radioclaire uniloculaire, parfois multiloculaire, bien circonscrite entourée d’une bordure sclérotique. Rarement mixte avec des petits flocons radio-opaques présents au sein de la lésion.
La forme périphérique n’est pas systématiquement visible radiologiquement sauf si des calcifications sont présentes.
55 El Harti, Oujilal, et El Wady, « Central odontogenic fibroma of the maxilla ».
56 Centre international de recherche sur le cancer, Pathology and genetics of head and neck tumours. 57 Ibid.
Pronostic :
Le pronostic est excellent après énucléation et curetage, malgré une possibilité de récidive plus élevé chez le FOP que le FOC58.
. Cémentoblastome ou cémentome vrai
Un cémentoblastome est un néoplasme rare ayant pour origine une prolifération de cémentoblastes produisant du cément désorganisé (cément acellulaire) autour de la racine d’une dent5960.
Très similaire histologiquement à l’ostéoblastome, il s’en différencie car il reste attaché à la racine d’une dent et séparé de l’os par une continuation du desmodonte61.
Touche aussi bien les hommes que les femmes.
Les cémentoblastomes sont situés dans la mandibule dans plus de 70% des cas62, liés à la première molaire permanente principalement. Exceptionnellement ils peuvent être associés à une dent temporaire.
On retrouve dans la littérature quelques rares situations de cémentoblastomes des dents maxillaires pouvant impliquer le sinus maxillaire et même encore le plancher de l’orbite63.
Clinique :
Les signes les plus fréquents sont une tuméfaction intra-buccale douloureuse64 mais ils peuvent être asymptomatiques. Les dents impliquées sont vitales.
D’autres complications peuvent survenir plus rarement, telles que des fractures mandibulaires ou paresthésies labiales inférieures.
58 El Harti, Oujilal, et El Wady, « Central odontogenic fibroma of the maxilla ».
59 Centre international de recherche sur le cancer, Pathology and genetics of head and neck tumours. 60 Dadhich et Nilesh, « Cementoblastoma of posterior maxilla involving the maxillary sinus ».
61 Ibid.
62 Brannon et al., « Cementoblastoma: an innocuous neoplasm ? A clinicopathologic study of 44 cases and review
of the literature with special emphasis on recurrence ».
63 Dadhich et Nilesh, « Cementoblastoma of posterior maxilla involving the maxillary sinus ». 64 Xu et al., « Analysis of clinical and imaging findings in cementoblastoma ».
Radiologie :
Il se présente comme une masse radio-opaque circulaire bien circonscrite accolée à la racine d’une dent (premières molaires et prémolaires mandibulaires surtout), bordée d’une zone radioclaire mince et uniforme65. L’image peut être de densités mixtes lorsque la lésion est immature.
La perte du contour radiculaire (par oblitération de l’espace desmodontal au niveau de la lésion) est spécifique et permet notamment de le différencier de l’ostéoblastome6667.
D’autres caractéristiques moins fréquentes peuvent être retrouvées tel que : des résorptions des racines adjacentes, accolement à 2 racines adjacentes, perforation de la corticale68.
Figure 7 Cémentoblastome Bénin : associé à la première prémolaire mandibulaire gauche dont la moitié apicale du contour radiculaire n’est plus objectivable.
Source : Pynn « Benign Cementoblastoma »,2001
Pronostic et évolution :
Sa croissance est lente mais évolue constamment. Des récidives sont fréquentes si l’exérèse n’est pas complète. Par conséquent, Brannon et Fowler, 2002 69 recommandent d’éliminer l’ensemble de la lésion avec la dent associée suivi d’un curetage ou ostectomie périphérique.
65 Ibid.
66 Centre international de recherche sur le cancer, Pathology and genetics of head and neck tumours. 67 Dadhich et Nilesh, « Cementoblastoma of posterior maxilla involving the maxillary sinus ».
68 Ibid.
69 Brannon et al., « Cementoblastoma: an innocuous neoplasm ? A clinicopathologic study of 44 cases and review
. Fibrome cémento-ossifiant (Cf : Lésions fibro-osseuses)
Le fibrome cémento-ossifiant était anciennement classé dans les lésions relatives à l’os70 mais l’OMS a classé la forme classique dans les tumeurs odontogéniques71 pour le distinguer des formes juvéniles.
2.1.2. Tumeurs Bénignes Ostéogéniques
2.1.2.1. Ostéomes
L’ostéome est une tumeur bénigne ostéoformatrice à croissance lente caractérisée par une prolifération d’os mature spongieux et/ou compact recouvert de périoste. Il existe 3 variantes d’ostéome selon leur localisation72 :
-les ostéomes périphériques : proviennent du périoste, se présentent comme une masse dure attachée à l’os cortical.
-les ostéomes centraux : beaucoup plus rares, proviennent de l’endosteum (fine couche de tissu conjonctif tapissant la surface de la cavité médullaire des os longs) restent intra-osseux.
-les ostéomes extra-squelettiques se développent dans les tissus mous, plus particulièrement les muscles.
Des ostéomes multiples des mâchoires sont fréquemment associés au Syndrome de Gardner.
Localisation :
Les ostéomes peuvent être unique ou multiples, centrale ou à la surface osseuse.
Leurs localisations cranio-faciales sont principalement les sinus frontaux et éthmoïdaux. Les ostéomes mandibulaires impliquent plus fréquemment l’angle que le condyle, le bord inférieur du corps et la table linguale7374. Hormis dans les cas d’ostéomes du sinus maxillaire ou de syndrome de Gardner, l’os maxillaire est rarement impliqué.75
70 Centre international de recherche sur le cancer, Pathology and genetics of head and neck tumours.
71 Wright et Vered, « Update from the 4th edition of the World Health Organization classification of head and
neck tumours : odontogenic and maxillofacial bone tumors ».
72 Nilesh, Bhujbal, et Nayak, « Solitary central osteoma of mandible in a geriatric patient: report and review ». 73 Tenório de França et al., « Solitary peripheral osteomas of the jaws ».
74 Karandikar et al., « Osteoid osteoma of mandible ».
Clinique :
Ils se présentent comme une masse dure sessile ou pédiculée de 1 à 4 cm de diamètre76. Les ostéomes sont souvent asymptomatiques et découverts de façon fortuite par examen
radiographique de routine. Cependant, selon leur volume et leur localisation, ils peuvent entrainer des douleurs, asymétrie faciale, céphalée, dysfonctions occlusales, limitation de mouvement mandibulaire ou plus rarement des paresthésies par compression nerveuse77.
Aspect radiologique :
L’ostéome forme une image radio-opaque arrondie ou ovalaire bien circonscrite. Dans les cas d’ostéomes périphérique, cette masse radio-opaque est fixée par une base large ou un pédicule à l’os cortical affecté78. Ceux-ci sont radiologiquement très semblables aux exostoses.
Les caractéristiques cliniques sont nécessaires pour différentier les ostéomes périphériques des exostoses. En effet, les exostoses sont généralement multiples et situées dans des zones de
muqueuse gingivale. Les exostoses solitaires sont rares et se produisent fréquemment associés à un traumatisme local ou dans des régions ayant reçu une greffe gingivale ou cutanée79.
Figure 8. Ostéome Périphérique de l’angle mandibulaire droit (panoramique dentaire et tomodensitométrie)
Source : Dr Lalo Jacques, Hopital Saint-Antoine, Paris, 2016
Evolution et pronostic :
Les ostéomes ont une croissance très lente et ne présentent pas de risque de dégénérescence maligne. 76 Ibid. 77 Ibid. 78 Ibid. 79 Ibid.
Les ostéomes de petit volume et asymptomatiques ne nécessitent pas de traitement, cependant ils nécessiteront un suivi toutes les une à deux années80 afin d’évaluer l’évolution de la lésion. L’exérèse chirurgicale est indiquée pour les lésions volumineuses, symptomatiques et entrainant un déficit fonctionnel ou esthétique81. Les récidives sont extrêmement rares après exérèse82.
2.1.2.2. Syndrome de Gardner ou polypose adénomateuse familiale 83 :
Ce syndrome est une affection héréditaire rare à transmission autosomique dominante, résultant d’une anomalie de développement des trois feuillets embryonnaires primitifs. Il apparait entre l’adolescence et le début de vie adulte. Il est caractérisé par une polypose rectocolique disséminée associés à d’autres tumeurs : ostéomes multiples (localisation principalement crânienne et
maxillaire), kystes épidermoïdes, des tumeurs fibreuses ou musculaires rétropéritonéales ou intramésentériques, lipomes sous cutanés, tumeurs thyroidienne, fibrome cutanés et tumeurs desmoïdes.
La transformation carcinomateuse de ces polypes colorectaux est inéluctable (100% de cancers colorectaux avant 40ans) d’où la nécessité de diagnostic et prise en charge précoce.
Clinique :
Les symptômes gastro-intestinaux, diarrhée sanglante et douleurs abdominales sont associés aux diverses manifestations des multiples tumeurs dont le patient peut être atteint.
Aspect radiologique :
Ce syndrome se manifeste par des images radio-opaques multiples d’ostéomes situées
principalement à la mandibule. Il n’est pas rare d’observer des odontomes ou dents surnuméraires associés à ces ostéomes.
80 Nilesh, Bhujbal, et Nayak, « Solitary central osteoma of mandible in a geriatric patient: report and review ». 81 Ibid.
82 Karandikar et al., « Osteoid osteoma of mandible ». 83 Panjwani et al., « Gardner’s syndrome ».
Figure 9. Ostéomes multiples d’un syndrome de Gardner
Source : Panjwani et al., « Gardner’s Syndrome »,2011
Pour le chirurgien-dentiste, la présence d’ostéomes multiples associés ou non à des anomalies dentaires (dents surnuméraires, inclusion dentaire, hypercémentose) est un indice pouvant faire suspecter un syndrome de Gardner.
2.1.2.3. Ostéome ostéoïde
L’ostéome ostéoïde est une tumeur bénigne ostéoformatrice douloureuse, de petite taille (inférieur à 2cm généralement) et croissance limitée caractérisée par la formation d’une cavité, le nidus,
constitué tissu ostéoïde, pouvant se calcifier, entouré d’une zone d’ostéocondensation réactionnelle.
Il est histologiquement très proche de l’ostéoblastome. De prédominance masculine, il apparait principalement dans les deuxièmes et troisièmes décennies de vie84.
Localisation :
Il est intracorticale le plus souvent mais peut aussi être médullaire, sous-périosté ou intra-articulaire. Tous les os du squelette peuvent être impliqués excepté le sternum. Il siège dans 80% des cas dans les os longs85 (fémur proximal, tibia surtout), tandis qu’il se situe très rarement dans les mâchoires (moins de 1% des cas avec la mandibule plus affectée que le maxillaire86).
84 Karandikar et al., « Osteoid osteoma of mandible ». 85 Ibid.
Clinique : La douleur est le symptôme principal, elle est typiquement intermittente avec
exacerbations nocturne (voir uniquement nocturne) et calmée efficacement par les salicylés ou autres anti-inflammatoire non stéroïdien87. Rarement, on peut observer une petite tuméfaction.
Imagerie :
L’image typique de l’ostéome ostéoïde est représentée par une petite plage d’ostéolyse arrondie ou ovalaire (le nidus), entouré d’une zone d’ostéosclérose et contenant au centre une zone de
calcification radio-opaque88.
Figure 10. Ostéome Ostéoïde de l’angle mandibulaire gauche
Source : Karandikar et al., « Osteoid osteoma of mandible », 2011
Figure 11. Ostéome Ostéoïde de l’humérus (tomodensitométrie) : le nidus, radioclaire avec son centre radio-opaque , entouré d’un os présentant une sclérose dense
Source : Fletcher et al., , OMS, « Pathology and Genetics of Tumours of Soft Tissue and Bone »,2002
87 Fletcher, Unni, et Mertens, Pathology and genetics of tumours of soft tissue and bone. 88 Karandikar et al., « Osteoid osteoma of mandible ».
Évolution et pronostic :
L’ostéome ostéoïde possède un potentiel de croissance qui reste limité, il n’y a donc pas d’extension. Dans certain cas, il peut y avoir une régression spontanée de la lésion ou un passage à une forme inactive89. Il n’y a pas de risque de transformation maligne.
Les ostéomes ostéoïdes sont traités par ablation chirurgicale du nidus (curetage ou exérèse) ou par thermoablation transcutanée (laser, radiofréquence) scanoguidée. Les récidives sont rares.
2.1.2.4 Ostéoblastome
L’ostéoblastome est une tumeur ostéoformatrice rare (environ 1% de toutes les tumeurs osseuses90), qui correspond histologiquement à un ostéome ostéoïde de taille supérieure à 2cm. Il apparait généralement avant 30ans et affecte principalement les adolescents et adolescent de sexe masculin. Il existe 2 entités d’ostéoblastome : la forme classique, bénigne, à potentiel de croissance limité, dont la taille reste inférieure à 4cm et la forme agressive, plus rare, de croissance localement agressive, atteignant des dimensions supérieures à 4cm9192.
Localisation :
Les sites principalement atteints sont les vertèbres (éléments postérieurs) et le sacrum puis, dans le squelette appendiculaire, le fémur distal et le tibia proximal93 et les os du tarse (talus, calcaneus). Moins de 10% des ostéoblastomes affectent les os crânio-faciaux94, cependant dans les cas d’ostéoblastome des mâchoires, la mandibule (corps mandibulaire, région postérieure) est plus impliquée que le maxillaire9596.
Clinique :
L’ostéoblastome des mâchoires peut entrainer une tuméfaction et des algies, mais peuvent aussi être asymptomatique.
À la différence de l'ostéome ostéoïde, la douleur est rarement nocturne et non soulagée par les salicylates.
89 Fletcher, Unni, et Mertens, Pathology and genetics of tumours of soft tissue and bone.
90 Mardaleishvili et al., « Benign osteoblastoma of the mandible in a 12-year-old female: a case report ». 91 Ibid.
92 Kaur et al., « Aggressive osteoblastoma of the mandible : a diagnostic dilemma ». 93 Fletcher, Unni, et Mertens, Pathology and genetics of tumours of soft tissue and bone. 94 Kaur et al., « Aggressive osteoblastoma of the mandible : a diagnostic dilemma ». 95 Ibid.
Aspect radiologique :
Sur les radiographies standard, il forme une plage lytique ovalaire ou arrondie supérieure à 2cm, bien délimitée, entourée d’une fine coque de sclérose. Cette plage peut aussi apparaitre mixte ou
ostéocondenscante selon l’importance des calcifications intra-tumorales.
A la mandibule : il se présente avec centre calcifié cerné par un halo radiotransparent bien limité. Ces caractéristiques sont semblables au cémentoblatome, à la différence qu’il n’est pas accolé à la racine d’une dent.
Les formes agressives peuvent provoquer une rupture de la corticale et s’étendre aux tissus mous. Le diagnostic différentiel avec l’ostéome ostéoïde (plus petit avec une condensation plus importante) et l’ostéosarcome est aussi difficile du fait des similitudes de manifestation radiologique.
Evolution et pronostic :
Les ostéoblastomes peuvent être traités par curetage ou , pour les lésions de plus grande taille, par excision locale. Le pronostic est excellent, le faible risque de récurrences est lié à des situations d’exérèse incomplète9798. Les formes agressives ont plus tendance à la récidive99. De plus, le risque de transformation maligne existe, bien qu’il soit très faible.
2.1.2.5 Torus mandibulaire et palatin
Les tori sont des formes particulières de tumeurs ostéoformatrices, relativement fréquente, siégeant long de la crête longitudinale du palais dur (torus palatin), ou situées sur la face linguale de la
mandibule au-dessus de la ligne mylo-hyoïdienne (torus mandibulaire). Ils sont définis comme des exostoses orales bien qu’ils soient distincts des ostéochondromes (Cf. 2.1.3.2 Ostéochondrome ou
exostose).
En effet, terme d’exostose est aussi utilisé comme terme générique pour désigner une tumeur bénigne formée de tissu osseux qui se développe à la surface de l’os. L’ostéochondrome serait, ainsi, une forme particulière d’exostose : l’exostose ostéogénique.
97 Fletcher, Unni, et Mertens, Pathology and genetics of tumours of soft tissue and bone.
98 Mardaleishvili et al., « Benign osteoblastoma of the mandible in a 12-year-old female: a case report ». 99 Kaur et al., « Aggressive osteoblastoma of the mandible : a diagnostic dilemma ».
Cliniquement asymptomatique, ils se manifestent comme une tuméfaction dure longitudinale du palais osseux pouvant être plate, nodulaire, fusiforme ou lobulaire. Les tori mandibulaires se
retrouvent au niveau de la table osseuse linguale en regard des canines et prémolaires 100 unilatérale ou beaucoup plus souvent bilatérale (80% des cas).
L’imagerie montre une masse radio-opaque dense bien délimitée formant une excroissance visible sur les clichés occlusaux ou tomodensitométrique.
Evolution et traitement :
Les tori sont d’évolution bénigne à croissance lente et ne nécessitent généralement pas d’intervention. Seule la surveillance de leur croissance est nécessaire.
Cependant, dans certains cas, ils peuvent entrainer une gêne fonctionnelle, esthétique (torus volumineux) ou des difficultés dans la réhabilitation prothétique d’édentements (prothèse amovible).Dans ces conditions, il peut être indiqué de réaliser une résection chirurgicale.
2.1.3 Tumeurs Bénignes Chondrogéniques
Les tumeurs bénignes chondrogéniques sont très rarement localisées dans les mâchoires. Les principales sont les chondromes, l’ostéochondrome, le chondroblastome et le fibrome chondromyxoïde.
2.1.3.1 Chondromes
Les chondromes forment un groupe de tumeurs bénignes d’origine cartilagineuse qui contient les enchondromes (tumeur cartilagineuse hyaline bénigne de la médullaire) et les chondromes périostés beaucoup plus rares101.
Ces tumeurs se situent principalement dans les petits os tubulaires (mains et pieds) principalement suivi des os tubulaires plus volumineux (humérus et fémur)102. La localisation crânio-faciale est exceptionnelle.
100 Cavézian, Imagerie dento-maxillaire: approche radio-clinique.
101 Fletcher, Unni, et Mertens, Pathology and genetics of tumours of soft tissue and bone. 102 Ibid.
Radiologiquement, ils se présentent comme une lacune intramédullaire, bien limitée, sans ostéocondensation périphérique, présentant des foyers de calcifications irréguliers en quantité variable103. Les chondromes périostés se trouvent à la surface de l’os, provoquant une érosion de la corticale.
L’enchodromatose ou Maladie d’Ollier est caractérisée par la présence d’enchondromes multiples. Lorsqu’elle est associée à des hémangiomes, il s’agit du Syndrome de Maffucci. Ces pathologies nécessitent une surveillance et une prise en charge rigoureuse du fait des risques important de transformation maligne des lésions.
2.1.3.2 Ostéochondrome ou exostose
Selon l’OMS, 2005104 , « une exostose est une excroissance osseuse sessile ou pédonculée présentant une coiffe cartilagineuse. La composante osseuse (corticale et os spongieux) est en continuité avec l’os sous-jacent. » C’est est la plus commune des tumeurs osseuses105.
Les lésions peuvent être uniques ou multiples plus rarement (syndrome des ostéochondromes multiples ou maladie des exostoses multiple : héréditaire), atteignent plus fréquemment les femmes que les hommes.
Localisation :
Les ostéochondromes se retrouvent communément au niveau de la métaphyse des os long tels que le fémur, l’humérus le tibia et la fibula. Les os plat sont moins fréquemment impliqués.
La localisation maxillo-faciale est inhabituelle, et se situe quasi exclusivement au niveau du processus coronoïde et le condyle mandibulaire106107 et n’est pas rencontrée dans les formes héréditaire multiples.
103 Taupin et al., « Tumeurs cartilagineuses bénignes des mâchoires ».
104 Centre international de recherche sur le cancer, Pathology and genetics of head and neck tumours. 105 Fletcher, Unni, et Mertens, Pathology and genetics of tumours of soft tissue and bone.
106 Taupin et al., « Tumeurs cartilagineuses bénignes des mâchoires ».