Effet de la douleur sur la plasticité corticospinale induite
par une déafférentation ou un entraînement moteur
Thèse
Nicolas Mavromatis
Doctorat en médecine expérimentale
Philosophiae doctor (Ph. D.)
Québec, Canada
Effet de la douleur sur la plasticité corticospinale
induite par une lésion ou un entraînement moteur
Thèse
Nicolas Mavromatis
Sous la direction de :
Ré sumé :
Introduction :
En réadaptation, un nombre important de patients devront réapprendre certains mouvements ou ont subi des lésions entrainant des déficits sensorimoteurs. Ces évènements impliquent la mise en place de mécanismes mettant en jeu la neuroplasticité. Cette neuroplasticité est définie comme la capacité du système nerveux central à se modifier pour s’adapter aux changements internes ou externes. De plus, une majorité des patients en réadaptation souffrent de douleur dont la présence est associée à une moins bonne récupération. De récentes études ont révélé que la douleur est capable d’influencer l’état d’excitabilité du cortex moteur. Étant donné que la neuroplasticité est influencée par l’état du système, l’objectif de cette thèse a été de tester, à l’aide de deux protocoles connus pour induire une plasticité, l’influence d’une douleur expérimentale sur la plasticité corticospinale.
Méthodologie :
Deux expérimentations ont été réalisées. Un devis intra-sujet nécessitant que les participants prennent part à deux sessions expérimentales (Douleur, NonDouleur) a été utilisé lors de la première expérimentation. La seconde étude a quant à elle utilisé un devis inter-sujets afin que le modèle de plasticité employé (entraînement moteur) ne puisse influer sur les comparaisons entre les deux conditions expérimentales (présence (groupe Douleur) ou absence de douleur (groupe NonDouleur)).
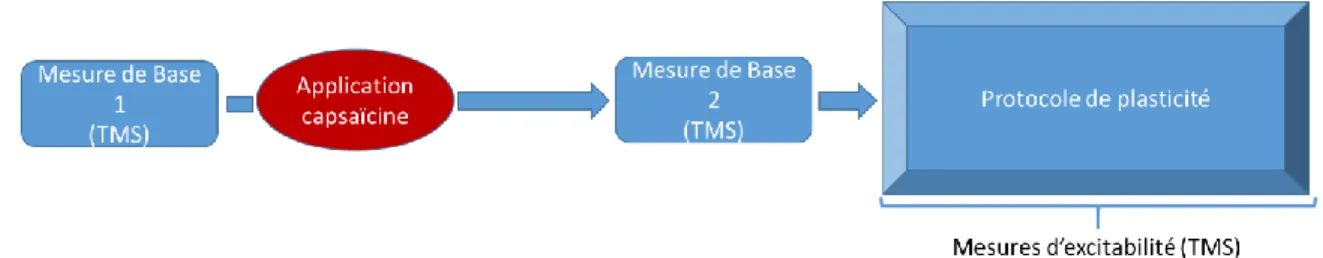
Dans chacune des expérimentations, le niveau d’excitabilité corticospinale de base de chaque participant a été mesuré via l’enregistrement des potentiels moteurs évoqués (MEP) par stimulation magnétique transcrânienne (TMS). Ensuite, selon le groupe ou la séance, la douleur expérimentale était induite via l’application topique de crème de capsaïcine au niveau de la main. Après cette application, une seconde mesure de base était effectuée afin de s’assurer que les mesures neurophysiologiques entre groupes ou sessions demeuraient comparables avant l’exposition au protocole de plasticité.
Dans la première expérimentation, le protocole permettant d’induire une plasticité corticospinale consistait à appliquer une déafférentation ischémique transitoire en présence ou absence de douleur selon la session expérimentale. L’influence de la douleur sur l’inhibition interhémisphérique a également été évaluée en mesurant la période de silence ipsilatérale. Lors de la seconde expérimentation, la plasticité était induite via la réalisation, en présence ou absence de douleur, d’un entraînement moteur. Des mesures de l’excitabilité corticospinale et de l’inhibition intracorticale à courte latence ont été effectuées afin de caractériser l’influence de l’entraînement et de la douleur sur ces variables.
Des analyses de variance (ANOVAs) comparant les mesures neurophysiologiques effectuées avant et après l’application des protocoles de plasticité et entre les conditions ont été réalisées pour caractériser l’effet de la douleur.
Résultats :
Les deux expérimentations ont démontré un effet modulateur de la douleur sur la plasticité induite par un évènement subséquent. Cette modulation s’est traduite, dans la première expérimentation, par une augmentation de l’excitabilité corticospinale des muscles proximaux plus importante lorsque la déafférentation est appliquée en présence de douleur. Dans la seconde expérimentation, la réalisation de l’entraînement moteur a induit chez le groupe contrôle une augmentation de l’excitabilité corticospinale du muscle utilisé dans la tâche au milieu de l’entraînement, avant que cette excitabilité ne revienne à son niveau de base dans la seconde moitié de l’entraînement. Les participants ayant réalisé l’entraînement en présence de douleur n’ont, en revanche, pas montré de variation de leur excitabilité corticospinale. Pourtant, ces derniers ont présenté de meilleures performances comportementales, notamment une plus grande précision lors de la réalisation de la tâche. Dans l’ensemble des expérimentations, la douleur n’a pas influencé les mesures interhémisphériques ou intracorticales.
Conclusion :
Les résultats présentés dans cette thèse confirment l’hypothèse formulée selon laquelle la douleur possède la capacité de moduler la plasticité se développant en réponse à un
évènement tel qu’une déafférentation ou un entraînement moteur. Ces résultats supportent les observations rapportées chez les patients souffrant de douleur chronique (e.g. amputés) présentant une organisation corticale altérée. La seconde expérimentation suggère également que si la présence de douleur n’a pas d’effet délétère sur les performances motrices lors d’un entraînement, elle peut tout de même influencer les modifications de l’excitabilité corticospinale qui lui sont associées. Les résultats obtenus au terme de ce projet permettent d’éclaircir les liens qui relient douleur, système moteur et plasticité et ouvrent la voie à de nouvelles recherches qui pourront à terme amener à proposer des soins optimaux aux patients présentant de la douleur.
Abstract :
Introduction:
In rehabilitation, a large number of patients have to relearn certain movements or have suffered injuries leading to sensorimotor deficits. These events trigger or rely on neuroplasticity mechanisms. Neuroplasticity can be defined as the ability of the central nervous system to change itself in order to adapt to internal or external changes. Moreover, a majority of rehabilitation patients suffer from pain, and the presence of pain is associated with poorer recovery. Recent studies have shown that pain can influence the state of excitability of the motor cortex. Since neuroplasticity is influenced by the state of the system, the objective of this thesis was to test the influence of experimental pain on corticospinal plasticity using two protocols known to induce plasticity.
Methodology:
Two experiments were realized. An intra-subject design requiring participants to take part in two experimental sessions (Pain, NoPain) was used during the first study. The second study used an inter-subject design (Pain group or NoPain group)), as the model of plasticity used (motor training) could have involve carry-over effects.
In each of the studies, transcranial magnetic stimulation (TMS) was used to assess the corticospinal excitability by recording motor evoked potentials (MEP). Subsequently, depending on the group or session, experimental pain was induced via the topical application of capsaicin cream on the hand. Afterward, a second baseline measurement was performed to ensure that neurophysiological measurements between groups or sessions remained comparable prior to exposure to the plasticity protocol.
In the first study, corticospinal plasticity was induced by applying transient ischemic deafferentation in the presence or absence of pain. The influence of pain on interhemispheric inhibition was also assessed by measuring the ipsilateral silent period. In the second study, corticospinal plasticity was induced by performing a motor training, in the presence or absence of pain. Measurements of corticospinal excitability and
short-latency intracortical inhibition were performed to characterize the influence of training and pain on these variables.
Analyzes of variance (ANOVAs) were performed on the neurophysiological variables to assess the effect of the plasticity protocols (before vs. after) and the effect of pain (inter-condition or inter-group comparison).
Results:
Both experiments demonstrated a modulating effect of pain on the plasticity induced by a subsequent event. In the first study, a greater increase in the corticospinal excitability of the proximal muscles was observed when the deafferentation was applied in the presence of pain. In the second study, the motor training induced an increase in the corticospinal excitability of the muscle used in the task at mid-training in the NoPain group, but excitability returned to baseline level before the end of the training. However participants who performed training in the presence of pain did not show any significant change in their corticospinal excitability throughout the motor task. Importantly, participants performing the task in the presence of pain presented a better behavioral performance, including a greater accuracy when performing the task. In all experiments, pain did not influence interhemispheric or intracortical measures.
Conclusion:
The results presented in this thesis confirm the hypothesis that pain has the ability to modulate plasticity occurring in response to an event such as deafferentation or motor training. These results support findings obtained in patients with chronic pain (e.g. amputees) who show altered cortical organization. Results from the second study also suggest that if the presence of pain has no deleterious effect on motor performance during training, it may still influence the changes in corticospinal excitability associated with it. Overall the results presented in this thesis provide new insights into the links between pain, motor system and plasticity.
Tablé dés matié rés:
Résumé : ... III Abstract : ... VI Liste tableaux : ... XI Liste figures : ... XII Liste des abréviations ... XIII Avant-propos ... XIV Remerciements ... XVI
Chapitre I : Introduction ... 1
1.1 Introduction générale ... 1
1.2 La neuroplasticité ... 2
1.2.1 La plasticité des cartes corticales ... 3
1.2.2 Plasticité des cartes corticales chez l’humain ... 8
1.2.3 Plasticité induite par un apprentissage... 13
1.3 Le phénomène de la douleur ... 18
1.3.1 L’expérience de la douleur ... 18
1.3.2 Neurophysiologie de la douleur ... 20
1.3.3 Interaction entre douleur et système moteur ... 22
1.4 Douleur et Neuroplasticité ... 28
1.4.1 Concept de métaplasticité ... 28
1.4.2 Moduler artificiellement la plasticité ... 29
1.4.3 Douleur et plasticité post-lésionnelle ... 31
1.4.4 Douleur et apprentissage moteur ... 34
1.5 Objectifs et hypothèse de recherche ... 39
1.5.1 Objectif général ... 39
1.5.2 Hypothèse de travail ... 40
Chapitre II : Méthodologie générale ... 43
2.1 Devis expérimental ... 43
2.2 Protocoles de plasticité ... 45
2.2.1 La déafférentation ischémique transitoire ... 45
2.2.2 La tâche d’apprentissage moteur ... 45
2.3 Stimulation magnétique transcranienne : Mesure de la plasticité ... 47
2.3.1 Positionnement de la bobine et intensité... 48
2.3.2 Neuronavigation ... 53
2.4 Modèle de douleur expérimentale ... 54
Chapitre III: Experimental tonic hand pain modulates the corticospinal plasticity induced by a subsequent hand deafferentation ... 55
3.1 Résumé ... 56 3.2 Abstract ... 57 3.3 Introduction ... 58 3.4 Methods ... 59 3.4.1 Subjects ... 59 3.4.2 Experimental Design ... 60
3.4.3 EMG recording and TMS stimulation ... 60
3.4.4 Data analysis ... 61
3.5 RESULTS ... 62
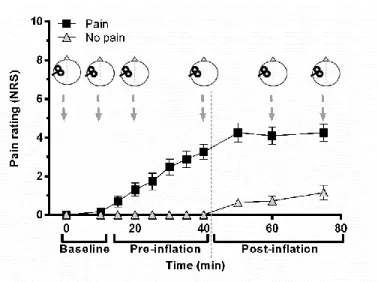
3.5.1 Pain levels throughout experimental phases ... 62
3.5.2 MEP amplitude changes in forearm muscles ... 63
3.5.3 Background EMG levels throughout experimental phases ... 64
3.6 Discussion ... 64
Chapitre IV : Inhibition interhémisphérique ... 69
4.1 Rappel ... 69
4.2 Méthode ... 69
4.2.1 Analyse statistiques ... 70
4.3 Résultats ... 70
4.4 Discussion ... 72
Chapitre V: Effect of experimental hand pain on training-induced changes in motor performance and corticospinal excitability ... 75
5.1 Résumé ... 76
5.2 Abstract ... 77
5.3 Introduction ... 78
5.4 Experimental Design & Motor Task ... 81
5.4.1 Experimental pain model ... 83
5.4.2 EMG recording and Neurophysiological measures ... 84
5.4.3 Data analysis ... 85 Behavioral variables ... 85 Neurophysiological variables ... 86 Statistical analysis ... 87 5.5 Results ... 88 5.5.1 Group characteristics ... 88 5.5.2 Pain rating ... 88 5.5.3 Behavioral outcomes ... 89 5.5.4 Neurophysiological outcomes ... 90
5.5.5 Correlational analyses between initial performance and training-related changes ... 92
5.5.6 Background EMG levels throughout the experiment ... 92
5.6 Discussion ... 93
6.1 Effet de la douleur sur l’excitabilité corticospinale ... 100
6.2 Modulation de la plasticité induite par une déafférentation ... 102
6.3 Modulation de la plasticité induite par un apprentissage moteur ... 104
6.3.1 Mesures comportementales ... 104
6.3.2 Mesures neurophysiologiques ... 107
6.4 Influence de l’attention sur la modulation de l’excitabilité corticospinale ... 110
6.5 Mécanismes sous-jacents à l’effet modulateur de la douleur ... 111
6.5.1 Mécanismes sous-tendant la modulation de l’excitabilité corticospinale ... 112
6.5.2 Implication des systèmes inhibiteurs ... 113
6.5.3 Implication des systèmes facilitateurs ... 114
6.5.4 Influence de la composante spinale ... 114
6.6 Perspectives de recherche ... 115
6.7 Perspectives cliniques ... 117
6.8 Forces et limites des travaux réalisées ... 118
Chapitre VII : Conclusion ... 121
Bibliographie ... 122
Annexe I : Questionnaire de contre-indication – Étude 1 ... 152
Annexe II : Annonce diffusée pour le recrutement – Étude 1 ... 154
Annexe III : Questionnaire de contre-indication – Étude 2 ... 155
Listé tabléaux :
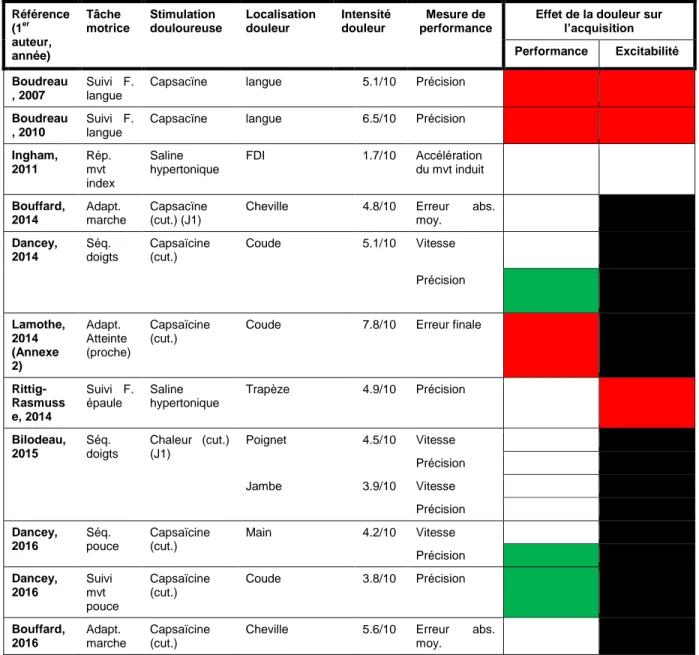
Tableau 1 : Effets de la douleur expérimentale sur la performance et l’excitabilité corticospinale lors de l’acquisition d’une tâche motrice. ... 37 Tableau 2 : Durée et latence de la période de silence mesurée dans les deux conditions expérimentales. ... 71
Listé figurés :
Figure 1 : Évolution de l’excitabilité corticospinale du FDI (first dorsal interosseous) et du biceps lors
de l’application d’une déafférentation ischémique transitoire au niveau de l’avant-bras. ... 12
Figure 2 : Activation cérébrale des représentations motrices des doigts... 16
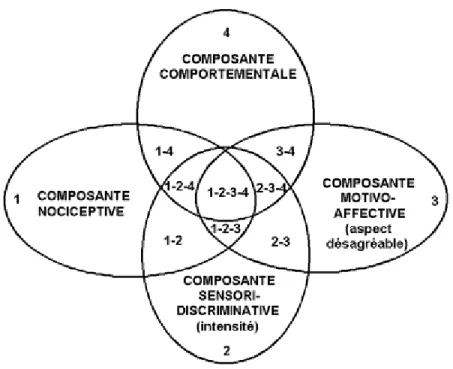
Figure 3 : Modèle circulaire de la douleur ... 20
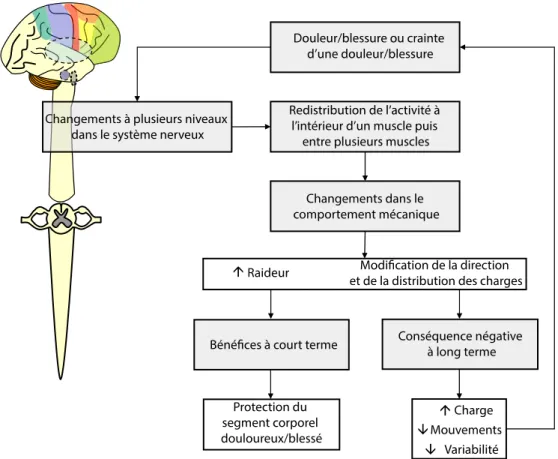
Figure 4 : Modèle d'adaptation à la douleur de Hodges et Tucker ... 24
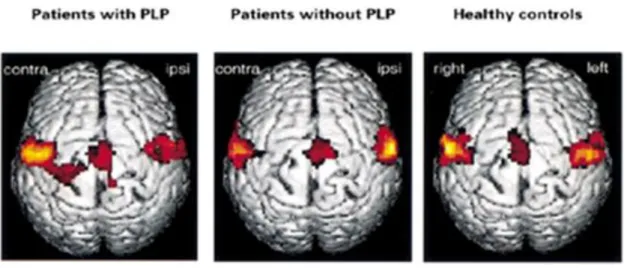
Figure 5 : Activation cérébrale lors d’un mouvement des lèvres chez 3 catégories de participants. 33 Figure 6 : Devis expérimental proposé dans l’ensemble des études réalisées dans le cadre de ce projet de thèse. ... 44
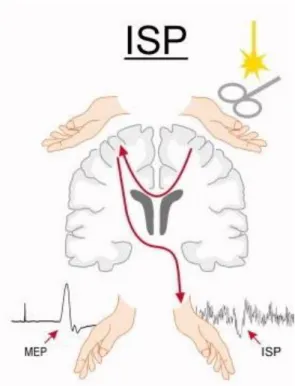
Figure 7 : Mesure de l’inhibition interhémisphérique via l’iSP. ... 51
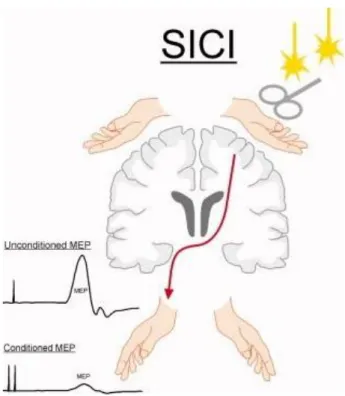
Figure 8 : Mesure de l’inhibition intracorticale via la SICI ... 53
Figure 9 : Time course of pain ratings ... 63
Figure 10 : Change in MEP amplitude relative to baseline and raw MEP traces. ... 64
Figure 11 : Tracés EMG et période de silence détectées chez un sujet représentatif. ... 71
Figure 12 : Durée de l’iSP entre nos deux conditions expérimentales. ... 72
Figure 13: Experimental design... 82
Figure 14 : Description of the motor task. ... 83
Figure 15 : Time course of pain ratings. ... 89
Figure 16 : Changes in behavioral and neurophysiological variables over time for each group. ... 90
Figure 17 : Association between Skill Measure during Early training and (A) improvement in Skill Measure from Early to Late training; (B) changes in MEP amplitude (%) at Mid training relative to Early training... 92
Listé dés abré viations
ANOVA : Analyse de Variance APB : Abductor pollicis brevis
CIRRIS : Centre interdisciplinaire de recherche en réadaptation et intégration sociale CRPS : Syndrome de douleur régionale complexe
CRSNG : Conseil de recherches en sciences naturelles et en génie du Canada EEG : Électroencéphalographie
EMG : Électromyographie FDI : Premier interosseux dorsal
FDS : Fléchisseur superficiel des doigts
FCR : Fléchisseur radial du carpe fléchisseur superficiel des doigts FRQS : Fond de la recherche Québec – Santé
GABA : acide γ-aminobutyrique Hz : Hertz
IHI : Inhibition interhémisphérique
IRDPQ : Institut de réadaptation en déficience physique de Québec ISI : Intervalle inter-stimuli
iSP : Période de silence ipsilatérale
IRM : Imagerie par résonnance magnétique
IRMf : Imagerie par résonnance magnétique fonctionnelle LTD : Dépression à long terme
LTP : Potentialisation à long terme M1 : Cortex moteur primaire MEG : Magnétoencéphalographie MEP : Potentiel moteur évoqué MT : Seuil moteur
mV : Millivolt
MVC : Contraction isométrique maximale NMDA : acide N-méthyl-D-aspartique
rTMS : Stimulation magnétique transcranienne répétitive SEM : Erreur standardisée de la moyenne
SI : Cortex somesthésique primaire SICI : Inhibition intracorticale SNC : Système nerveux central
tDCS : Stimulation transcranienne à courant continu TES : Stimulation électrique transcranienne
TEP : Tomographie par émission de positron TMS : Stimulation magnétique transcranienne
Avant-propos
Cette thèse de doctorat présente les résultats obtenus à la suite de la réalisation de deux études. Ces deux études sont présentées sous forme d’articles aux Chapitres 3 et 5. Des résultats complémentaires obtenus lors de la première étude, mais non inclus lors de la rédaction de l’article, sont également présentés au Chapitre 4.
La première étude s’intitulant « Experimental tonic hand pain modulates the corticospinal plasticity induced by a subsequent hand deafferentation » constitue le Chapitre 3 de cette thèse et a été publiée dans Neuroscience. La réalisation de cette étude a été effectuée sous la supervision du Dre Catherine Mercier, professeure au Département de réadaptation de la Faculté de médecine de l’Université Laval. Cette étude a été réalisée avec la contribution de Martin Gagné, Karen Reilly et Julien Voisin, ayant participé à l’élaboration de l’étude ainsi qu’à la rédaction de l’article.
Le Chapitre 4 rapporte des mesures d’inhibition interhémisphérique réalisées lors de cette première étude. Dû à l’absence d’effets significatifs concernant ces variables et afin d’assurer à la fois une meilleure cohérence dans les résultats présentés dans l’article et d’alléger celui-ci, il a été décidé de ne pas les inclure dans l’article. Cependant, comme ces mesures représentent le travail effectué et les compétences acquises, elles ont été incluses comme un chapitre complémentaire (Chapitre 4) et ont été utilisées pour alimenter les réflexions présentées dans la Discussion.
La seconde étude s’intitulant « Effect of experimental hand pain on training-induced changes in motor performance and corticospinal excitability» constitue le Chapitre 5 de cette thèse et a été publiée dans la revue Brain Science. La réalisation de cette étude a été effectuée sous la supervision du Dre Catherine Mercier. Martin Gagné et Cécilia Neige ont activement participé à l’ensemble des étapes de l’étude, de la conception à la rédaction de l’article. Karen Reilly a contribué à l’analyse des données obtenues, l’interprétation des résultats ainsi qu’à la rédaction de l’article.
Les études réalisées dans ce projet ont été rendues possibles par le support financier du Centre interdisciplinaire de recherche en réadaptation et intégration sociale (CIRRIS) qui m’a octroyé une bourse. Les travaux de recherche ont également été supportés par une subvention du Conseil de recherches en sciences naturelles et en génie du Canada (CRSNG) ainsi que par un appui salarial du Fond de la recherche Québec – Santé (FRQS) à ma directrice de recherche.
Étude 1 (Chapitre III)
Titre : Experimental tonic hand pain modulates the corticospinal plasticity induced by a subsequent hand deafferentation
Auteurs : Mavromatis N, Gagné M, Voisin JIAV, Reilly KT, Mercier C Paru le : 25 Aout 2016 dans Neuroscience.
Étude 2 (chapitre V)
Titre : Effect of experimental hand pain on training-induced changes in motor performance and corticospinal excitability
Auteurs : Mavromatis N, Neige C, Gagné M, Reilly, KT, Mercier C
Rémérciéménts
Avant de plonger dans le cœur des travaux réalisés dans le cadre de ce projet, il convient de s’arrêter un premier temps pour remercier ceux qui ont rendu ce travail possible. Tout d’abord je voudrais remercier le Dre Catherine Mercier. C’est grâce à Catherine et son soutient que cette thèse a été rendue possible. Elle m’a également permis de découvrir le Québec et la recherche dans un centre aussi agréable et avancé que le CIRRIS. Réaliser cette thèse aux côtés du Dre Catherine Mercier m’a je pense, sincèrement, permis de grandir « fortement » sur le plan professionnel (et personnel). Cette thèse a été l’occasion d’apprendre énormément et Catherine constitue sans aucun doute le meilleur objectif professionnel à viser.
J’aimerai également remercier tout particulièrement Dr Martin Gagné qui m’a accompagné tout au long de ces presque 4 années. Que ce soit pour le soutien professionnel tout au long des projets développés ou pour les questions plus personnelles ou hors « travail ». Tu as toujours été disponible et répondu à mes multiples (multiples) interruptions à ton bureau ! Ces années à tes côté m’ont beaucoup appris et particulièrement le fait que tu dois surement être une des personnes les plus patientes que je connaisse !
Si une thèse, ce n’est pas forcément un travail facile, le cadre dans lequel elle est réalisée a vraiment la capacité de bonifier cette expérience. J’ai eu la chance d’être entouré de personnes réellement agréables et superbes sur le plan humain. Que ce soit autour de discussion de bureau, lors des vendredis étudiants ou des journal club, j’ai toujours eu la chance d’avoir des collègues et camarades qui m’ont soutenu et m’ont permis de m’améliorer. Une énorme pensée à ceux qui ont partagé avec moi cet épisode de ma vie. Une pensée particulière à Jason, qui a été un modèle lors de mon arrivé au CIRRIS. À Charles également, qui a été mon modèle d’intégration professionnel (arrivé quelques temps après moi et au bout de quelques mois, un poste de professeur, efficace !) À Mélanie, Stéphanie et Isabelle qui ont partagé leur bureau avec moi. Bien sûr un merci qui n’est que trop peu à mes deux « petites sœurs » du H-602, Clémentine et Cécilia, qui m’ont épaulé et égayé mes journées. Vous avez fait de ce bureau un cadre de vie, plus que de travail, idéal et où il était bon de se retrouver. Merci à Ludo pour ses retours toujours constructifs, son
humour (des fois); je te laisse avec les filles, prends en soin (et bon courage !). Merci à la bande du « bureau élargie » : Anne, Benoit, Céline, Charline, Mick, … pour leur bonne humeur et leur soutien. Merci à l’équipe « de l’autre côté du couloir », William, Antoine, François, Marine et Jérôme (Jérôme ****!) pour le support et les ‘dredi brasserie. Merci à Karen pour son extrême gentillesse, sa bonne humeur et son aide quant aux études réalisées dans ce projet. Merci aux chercheurs qui composent cette fabuleuse équipe : Laurent Bouyer, Jean-Sébatien Roy, Bradford McFadyen, Katia Turcot, Andreanne Blanchette pour leurs conseils avisés et leur gentillesse. Merci également à Steve pour son soutien technique primordial et ses sauvetages de dernière minute lors de la réalisation des expérimentations.
D’un point de vue plus personnel, je souhaiterai souligner le soutien de ma famille et mes proches. Malgré la distance, j’ai toujours été supporté et ce, malgré mon pessimisme légendaire ! Merci à mes parents qui continuent à croire en moi et à me pousser. Trente années maintenant que vous me supportez, vous êtes, vous aussi, de formidables modèles. Merci à ma sœur Laure, à Anthony et Esteban pour leur soutien et leur sourire. Merci à Marylise pour son attention, sa patience et la confiance qu’elle me témoigne en me laissant kidnapper sa fille si loin ! Merci Fanny, Xavier et Lulu pour leur support (et les souvenirs de leurs voyages). Merci à Sarah, Eve, Bastien (de Harvard) et Rakib pour leur amitié, elle m’ait précieuse et me réconforte quand j’observe que la distance ne peut atténuer les liens lorsqu’ils sont si forts.
Enfin, un dernier merci mais pas le moindre. Merci « Didine » d’être assez folle pour partager depuis maintenant 10 ans ta vie avec moi. Merci d’avoir la folie (ou l’inconscience ?) d’avoir traversé la France pour me rejoindre puis d’avoir carrément traversé l’atlantique pour me suivre. Cette « aventure » s’est faite à deux (elle se continuera peut être à plus ?) et il est certain que je n’aurai pu réussir sans toi.
J’espère que cette étape de vie qui se termine n’est que le début d’une autre opportunité. «Tant qu’on s’ait ».
À tous,
Chapitré I : Introduction
1.1 Introduction générale
La plasticité cérébrale ou neuroplasticité est un phénomène essentiel grâce auquel notre système nerveux central est capable de s’adapter à différents évènements internes ou externes (Pascual-Leone et al., 2005). En réadaptation, le concept de neuroplasticité est important puisqu’il est associé aux changements se mettant en place à la suite des lésions subies et des entraînements moteurs qui sont proposés aux usagers.
Les études réalisées récemment ont permis de mieux comprendre les mécanismes par lesquels cette plasticité se développe. Dans les deux précédentes décennies, il a notamment été révélé que la capacité d’un système neuronal à développer une plasticité était dépendante de son état, on parle alors de plasticité state-dependent (Huang et al., 1992; Abraham and Bear, 1996; Abraham, 2008). Il est ainsi possible en altérant l’excitabilité de réseau de favoriser ou au contraire d’inhiber le développement d’une plasticité. Or, les dernières recherches ont montré que la douleur avait un effet inhibiteur sur le cortex moteur primaire (Valeriani et al., 1999; Farina et al., 2001; Le Pera et al., 2001). Il avait déjà été révélé que la douleur influe sur le système moteur d’un point de vue comportemental. Elle entraîne notamment une réduction de la contraction maximale volontaire (Graven-Nielsen et al., 2002; Farina et al., 2005), de l’endurance (Bengtsson et al., 1994; Graven-Nielsen et al., 1997; Ciubotariu et al., 2004) et de la coordination lors d’une tache motrice (Arendt-Nielsen et al., 1996). Ces observations reflètent les liens étroits existant entre la douleur et le système moteur.
La prise en compte de la présence de la douleur lors du développement d’une plasticité est un facteur important dans le contexte de la réadaptation. Cette importance résulte du fait qu’une part importante des usagers souffre de douleurs et que cette dernière est associée à une récupération fonctionnelle inférieure à celle des usagers ne présentant pas de douleur (Jonsson et al., 2006; Lundstrom et al., 2009; Reitsma et al., 2011). Si la douleur peut moduler l’excitabilité de M1 et que la plasticité est dépendante de l’état du réseau/système,
il convient de s’interroger sur la capacité de la douleur de moduler la mise en place de la plasticité. Par conséquent, la potentielle influence de la douleur lors du développement d’une neuroplasticité serait alors un élément important à considérer en réadaptation que ce soit, notamment, au moment où une lésion survient ou lors des entraînements moteurs proposés. C’est en s’appuyant sur cette réflexion que les travaux de cette thèse ont été conçus. Nous nous sommes interessés particulièrement à l’influence de l’application d’une douleur expérimentale sur plasticité induite au niveau de M1 par un modèle de lésion périphérique transitoire (étude 1) et lors d’un entraînement moteur (étude 2).
Avant de développer plus en détails ces travaux, les parties suivantes de l’Introduction exposeront l’état actuel des connaissances. La première partie ce chapitre sera dédiée au concept de neuroplasticité en exposant sa découverte ainsi que son développement à la suite d’une modification des afférences sensorielles ou de l’acquisition d’un entraînement moteur. La seconde partie, quant à elle, abordera le concept de douleur et sa relation avec le système moteur. La dernière partie se penchera finalement sur les interactions existantes entre la neuroplasticité et la douleur. Une emphase particulière sera portée sur l’influence de la douleur sur la plasticité se développant à la suite d’une lésion périphérique et d’un entraînement moteur.
1.2 La neuroplasticité
À la fin du 19ième siècle, l’utilisation de microélectrodes a été une des premières méthodes d’investigation du système nerveux in vivo. La microstimulation du cortex (Kita and Wightman, 2008) a permis de montrer qu’il existait, d’abord chez le chien et le singe, une région corticale qui, lorsque stimulée, générait le mouvement d’un membre controlatéral (Fritsch; Ferrier, 1873). Il a fallu cependant attendre le début de 20ième siècle pour qu’à partir de ces observations, Sherrington établisse une véritable cartographie du cortex moteur montrant par la même occasion que chaque membre du corps mais également les mouvements lié à ces membres y était représenté selon une véritable somatotopie (Grunbaum and Sherrington, 1903; Sherrington, 1918; Kakei et al., 1999).
Chez l’homme, l’existence de cette somatotopie a été démontrée par Penfield qui a procédé à des stimulations corticales durant la réalisation d’opérations chirurgicales chez des patients souffrant d’épilepsie. L’utilisation de microélectrodes permet également de mesurer des différences de potentiel (entre deux électrodes ou bien entre le potentiel d’un neurone et le milieu extracellulaire). L’enregistrement de l’activité neuronale via cette technique à la suite de stimulations périphériques a ainsi permis l’élaboration d’homoncule sensitif. Cette technique a prouvé qu’à l’image de cortex moteur primaire (M1), le cortex somesthésique primaire (S1) contient de manière organisée les représentations corticales des différents segments du corps (Penfield and Boldrey, 1937). À cette époque, ces représentations corticales étaient perçues comme stables et étant incapables de se modifier à la suite de différentes manipulations. Pourtant l’étude approfondie de ces cartes corticales lors de la seconde moitié de 20ième siècle a permis de remettre en question ce point de vue.
1.2.1 La plasticité des cartes corticales
Pour la communauté scientifique du siècle dernier, la plasticité du système nerveux central (SNC) était un concept qui se limitait à la période durant laquelle ce dernier se développait et le cerveau mature était vu comme un organe « rigide ». L’observation chez certains patients atteints de lésions cérébrales d’une certaine récupération fonctionnelle laissait cependant supposer que le cerveau était, d’une manière ou d’une autre, capable de compenser les modifications induites par les lésions subies. Il manquait pourtant l’explication des bases physiologiques de cette capacité d’adaptation, qui fût éventuellement révélée par l’étude des altérations des cartes sensorimotrices (Merzenich et al., 1984; Garraghty and Kaas, 1992).
Les premières observations de la plasticité des cartes sensorimotrices chez l’adulte furent réalisées chez l’animal à l’aide de matrices de microélectrodes. Dans un premier temps, Merzenich et ses collègues se sont intéressés à la façon dont la topographie des cartes somesthésiques réagissait à une suppression des afférences sensorielles chez le singe. Ils ont pour cela sectionné puis ligaturé le nerf médian (afin d’empêcher sa repousse) et ont observé les changements induits de 2 à 9 mois plus tard au niveau du cortex somesthésique (Merzenich et al., 1983). La déafférentation de la région innervée par le nerf médian
entraine une réorganisation topographique des cartes corticales somatosensorielles: la surface corticale préalablement activée par les afférences cutanées issues de ce nerf répond dorénavant à des stimulations des régions cutanées adjacentes. Cette première observation d’une plasticité induite par une lésion périphérique va être par la suite répliquée au sein de nombreuses espèces animales (Kelahan and Doetsch, 1984; Sanes et al., 1988; Welker et al., 1989).
Si une suppression des afférences entraine un remaniement des cartes corticales, une augmentation de la stimulation des afférences est également capable de moduler la représentation des membres. Une zone cutanée « sur-stimulée » (via le maintien des doigts sur un disque en rotation munie de différentes surfaces) voit ses champs récepteurs rétrécir et sa représentation corticale somatosensorielle se développer (Jenkins et al., 1990; Merzenich and Jenkins, 1993). Ces observations confirment que la manipulation des afférences (en les supprimant ou en les stimulant) est capable de produire des modifications d’organisation du SNC et ont été le point de départ permettant d’étendre le concept de neuroplasticité au cerveau adulte. Cette plasticité correspond à l’ensemble des mécanismes permettant au cerveau, et au SNC en général, d’adapter son fonctionnement à l’environnement. Elle se définit comme étant la capacité à créer, défaire ou réorganiser les réseaux de neurones et les connexions entre ces neurones (Pascual-Leone et al., 2005).
Les cortex sensoriel et moteur primaires sont des régions fortement interconnectées (Jones, 1986; Mao et al., 2011) et la modifications des afférences sensorielles va entrainer une modifications des cartes corticales qui ne se limitera pas au seul cortex sensoriel. En effet en 1988, Sanes et son équipe montrèrent que quelques heures seulement après une lésion d’un nerf facial du rat adulte, le cortex moteur se réorganise de manière à ce que la stimulation du cortex moteur préalablement dédié à la vibrisse entraîne, à la suite de la lésion, la production de mouvements des paupières et / ou de la patte (Sanes et al., 1988). Cette première observation de la réorganisation du cortex moteur à la suite d’une lésion périphérique est par la suite répliquée par Donoghue (Donoghue et al., 1990). Donoghue et son équipe observent les modifications induites par deux type de lésion chez le rat: 1- une section du nerf facial fonctionnellement relié aux vibrisses et 2- l’amputation d’une patte. Seulement quelques heures après la dénervation, l’activation corticale par stimulation
électrique directe des régions du cortex moteur activant auparavant la zone des vibrisses va entrainer une activation des muscles de la patte avant. La carte corticale de la patte avant au niveau du cortex moteur étant contiguë à celles des vibrisses, ces données indiquent que la représentation corticale de la patte avant s’est étendue au niveau de celle des vibrisses (décalage d’environ 1mm). L’amputation de la patte entraine quant à elle une réorganisation du cortex moteur qui se traduit par une augmentation de la taille des sites corticaux dont la stimulation entraine l’activation des muscles de l’épaule ainsi qu’une diminution du seuil moteur des muscles de l’épaule comparativement à des rats contrôles. À la vue de ces résultats, Donoghue suggère que la déafférentation entraine une modification des cartes corticales adjacentes au dépend de celle du membre déafférenté.
Pour expliquer la rapidité avec laquelle ces modifications de la représentation corticale sensorimotrice se mettent en place, il a été proposé que les mécanismes sous-jacents fassent appel à des connexions neuronales préexistantes plutôt qu’à des modifications d’ordre structurel tel que le « sprouting » (bourgeonnement axonal) ou la synaptogénèse, qui nécessitent un décours temporel plus long pour se mettre en place (Wall and Wolstencroft, 1977; Kaas et al., 1983). Ces modifications des représentations corticales reposeraient davantage sur des modifications de l’équilibre existant entre excitation et inhibition au sein des réseaux neuronaux et plus précisément sur du processus impliquant le GABA. Le GABA est le principal neurotransmetteur inhibiteur du système nerveux central, et l’injection locale de bicuculline (un antagoniste du récepteur GABAa) au niveau du cortex moteur chez le rat entraine une modification des représentations corticales similaires à celles observées à la suite d’une déafférentation (Jacobs and Donoghue, 1991). Cette observation corrobore les résultats obtenus par Welker (Welker et al., 1989) montrant une diminution de la GAD (enzyme permettant la synthèse du GABA) à la suite de l’ablation d’un follicule de vibrisse de souris. Ces résultats confortent l’hypothèse que l’organisation des cartes corticales est maintenue de manière dynamique en fonction de l’équilibre excitateur et inhibiteur existant au sein du réseau neuronal et qu’une modification des afférences a la capacité de modifier cet équilibre (Garraghty et al., 1991; Garraghty and Kaas, 1992; Jones, 1993; Donoghue, 1995)
Le suivi à long terme des lésions induites chez les modèles animaux a permis de démontrer la mise en place de phénomènes plastiques de nature différente de ceux que l’on observe rapidement suite à l’induction de la lésion. Comme nous l’avons vu précédemment, les changements rapides faisant suite à une lésion périphérique reposent essentiellement sur le changement d’activité de connexions déjà établies. Si la lésion est maintenue (par amputation ou encore par ligature du nerf empêchant la repousse par exemple), l’ampleur du remaniement des cartes corticales somatosensorielle augmente (Garraghty and Kaas, 1991; Xerri, 1998; Jain et al., 2008). En plus de ce remaniement plus important, il est également observé que la la taille des champs récepteurs de la représentation du membre contigüe diminue, ce qui reflète la mise en place d’une représentation corticale plus fine et détaillée du membre (Florence et al., 2000).
Les mécanismes permettant le développement à long terme d’une plasticité sont complexes. Pour expliquer les mécanismes qui sous-tendent le développement de la plasticité à long terme, Hebb émit la théorie que lorsque deux neurones reliés par une synapse s’activent de manière synchrone, la force de leur lien synaptique est renforcée. De manière inverse, lorsque les deux cellules sont activées de manière asynchrone, leur force synaptique diminue (Hebb, 1949). Cette théorie a été confortée par des études réalisées chez l’animal ayant révélées l’existence de deux mécanismes sous-tendant la plasticité à long terme (Bliss and Lomo, 1973; Clark and Kandel, 1984; Nicoll et al., 1988).
a) La potentialisation à long terme
La potentialisation à long terme (LTP, de l’anglais long-term potentiation) désigne un renforcement durable de l’efficacité de la transmission synaptique liant deux neurones. Elle fût mise en évidence pour la première fois par Bliss et Lomo en 1973 (Bliss and Lomo, 1973) qui observèrent qu'après une stimulation de haute fréquence de neurones issues de tranche d’hippocampe de rongeur, la réponse synaptique de certains neurones se trouvait augmentée et ce, pour une période prolongée. La découverte du phénomène de LTP fait écho au postulat qu’Hebb émit en 1949 selon lequel l’activité synchrone entre deux neurones renforce la synapse les reliant (Hebb, 1949). Au niveau cellulaire, ce renforcement synpatique passe par une libération massive de glutamate au niveau de la fente synaptique. Le glutamate va alors se lier aux récepteurs post-synaptiques AMPA et
NMDA. Lors d’une stimulation à haute fréquence, l’activation soutenue des récepteurs AMPA va entraîner une dépolarisation du neurone post-synaptique suffisante pour expulser l’ion magnésium bloquant l’entrée du canal NMDA et va ainsi permettre l’entrée massive de calcium dans le neurone post-synaptique (Nicoll et al., 1988; Malenka and Nicoll, 1993). Cette entrée de calcium va entraîner l’activation d’enzymes phosphorylantes qui auront pour effet de prolonger l’ouverture des récepteurs AMPA ou la fabrication de nouveaux récepteurs AMPA (via l’activation de la protéine CREB) ce qui aura pour effet d'augmenter l'efficacité synaptique. L’utilisation d’un antagoniste au NMDA a permis de montrer que les mécanismes de LTP intervenaient notamment dans la seconde phase de la plasticité post-déafférentation correspondant à la modification des champs récepteurs (Garraghty and Muja, 1996; Myers et al., 2000). La LTP serait également le support des apprentissage moteurs : l’étude de l’excitabilité de neurones ayant été impliqués dans un apprentissage montre que ces derniers présentent une diminution de leur capactité à développer davantage de LTP (Rioult-Pedotti et al., 2000; Monfils and Teskey, 2004). Cette diminution de la capacité à produire de la LTP serait le marqueur d’un effet de saturation et reflèterait un mécanisme prévenant la réalisation d’un apprentissage subséquent (Rioult-Pedotti et al., 2000). Des mécanismes similaires se retrouvent également au sein du cortex moteur humain (Ziemann et al., 2004).
b) La dépression à long terme :
La dépression à long terme (LTD, de l’anglais long term depression) se développe lorsque deux neurones ne déchargent pas ou peu de façon synchrone ce qui résulte en une réduction de l’efficacité synaptique entre ces deux neurones. La concentration faible de calcium au niveau du neurone post-synaptique va entraîner l’activation d’enzymes qui vont déphosphoryler les récepteurs AMPA. La LTD va également entraîner la réinternalisation de récepteurs AMPA qui étaient auparavant au niveau de la fente synaptique diminuant ainsi la sensibilité au glutamate libéré par le neurone présynaptique (Man et al., 2000; Chung et al., 2003).
1.2.2 Plasticité des cartes corticales chez l’humain
L’exploration des mécanismes cérébraux de manière non-invasive chez l’humain s’est développée à la suite de la création d’outils de neuroimagerie. Il est ainsi devenu possible de mesurer l’activité cérébrale par le biais de l’enregistrement de l’activité électrique des neurones (via l’électroencéphalographie (EEG)), du champ magnétique émit par leur activation (magnétoencéphalographie (MEG)), via leur consommation d’oxygène (l’imagerie par résonnance magnétique fonctionnelle (IRMf)) ou de substance au préalable marquée avec un traceur radioactif (tomographie par émission de positron (TEP)). Il est également possible de cartographier les représentations corticales motrices en stimulant le cortex moteur et en enregistrant les activations musculaires qui en résultent (via la stimulation magnétique transcranienne (TMS, de l’anglais transcranial magnetic
stimulation)). La TMS permet également d’explorer de manière non invasive l’état et les
variations d’excitabilité de la voie motrice corticospinale (Wassermann et al., 2008).
Une des premières études ayant permis de révéler l’existence d’une plasticité similaire à celle observée par Merzenich et son équipe chez l’homme adulte a été réalisée sur une population particulière: les patients souffrant de syndactylie, i.e. d’une fusion des doigts entre eux (Mogilner et al., 1993). L’activité cérébrale a été mesurée au niveau de la représentation corticale de la main chez deux de ces patients avant et à la suite d’une opération chirurgicale visant à séparer les doigts de leur main. Grâce à la MEG, il a été montré que les patients possédaient, avant l’opération, une représentation corticale altérée comparativement à des sujets sains se traduisant par une fusion des représentations des doigts (Mogilner et al., 1993). À la suite de la chirurgie, on observait une individualisation de la représentation des doigts (Mogilner et al., 1993). Cette première observation chez l’homme a démontré que le cerveau humain adulte est lui aussi capable de réorganiser ses réseaux corticaux. Cette plasticité des cartes corticales chez l’homme adulte faisant suite à une modification périphérique se retrouve également à la suite d’une amputation. Pascual-Leone et son équipe ont par exemple eu l’occasion de réaliser une cartographie des représentations corticales chez un sujet à l’aide de la TMS peu de temps avant que ce dernier ne subisse accidentellement une amputation de l’avant-bras (Pascual-Leone et al., 1996). Il a donc été possible de comparer les cartes corticales au sein d’un même hémisphère avant et après l’amputation. Les cartographies successives de M1 réalisées sur
plusieurs mois ont révélé que les représentations voisines des muscles de la face et du moignon « envahissaient » graduellement celle de la main amputée. Quatre mois après l’amputation, la stimulation de l’aire corticale liée auparavant au contrôle de la main entraînait maintenant une activation des muscles de la face et du moignon ainsi qu’une perception du membre amputé (Pascual-Leone et al., 1996).
Il faut noter toutefois que l’élargissement des cartes corticales voisines au membre déafférenté ne semble pas entraîner la disparition de sa représentation corticale. Il a par exemple été montré que la réalisation de mouvements avec le membre fantôme entraîne une activation corticospinale spécifique aux mouvements exécutés suggérant qu’une commande motrice volontaire corticale persiste pour exécuter ces mouvements du membre fantôme (Reilly et al., 2006; Gagne et al., 2009). De même, lors d’une déafférentation transitoire de la main, l’enregistrement du nerf ulnaire ou médian au niveau du coude révèle que la réponse motrice induite par une stimulation magnétique transcranienne demeure similaire à celle enregistrée avant l’application de la déafférentation (McNulty et al., 2002). La persistance de la représentation du membre déafférenté est également confirmée par l’observation qu’une stimulation de la représentation corticale du membre déafférenté est capable d’induire une inhibition interhémisphérique mesurée via l’étude de la période de silence ipsilatérale (Roricht and Meyer, 2000).
Cette importante capacité à se réorganiser en fonction de la modulation des afférences est aussi mise de l’avant dans des études qui se sont intéressées à des patients amputés ayant subi une greffe de la main. Ainsi, les modifications plastiques se développant à la suite d’une déafférentation ne sont pas figées une fois mises en place puisque la réalisation d’une greffe de main chez une personne amputée va de nouveau entraîner une réorganisation des cartes corticales faisant émerger de nouveau en quelques mois la représentation corticale de la main greffée (Giraux et al., 2001; Vargas et al., 2009).
Cette plasticité des représentations corticales des différents membres a également été rapportée dans des pathologies liées au mouvement comme chez les patients souffrant de dystonie (Bara‐Jimenez et al., 1998; Elbert et al., 1998). Chez ces patients, l’utilisation soutenue d’un membre ou la réalisation de mouvements répétitifs vont induire un
déplacement des cartes corticales avec une augmentation de la taille des représentations des membres dystoniques (Bara‐Jimenez et al., 1998; Elbert et al., 1998). Ces observations suggèrent que la surutilisation d’un membre est capable d’induire le développement d’une plasticité maladaptative qualifiée d’« usage-dépendante ». Le développement de cette plasticité maladaptative se retrouve également au sein de la population ayant subi un accident vasculaire cérébral. Chez ces patients souffrant d’hémiparésie, il est suggéré que la surutilisation du membre sain induit le développement d’une plasticité maladaptative qui retarde la récupération motrice du membre hémiparétique (Takeuchi and Izumi, 2012; Jang, 2013). L’utilisation de thérapie basée sur la contrainte du membre valide vise d’ailleurs à améliorer la récupération motrice en favorisant une plasticité « usage-dépendante » du membre lésé (Liepert et al., 1998; Kopp et al., 1999; Levy et al., 2001).
a) Plasticité à court terme
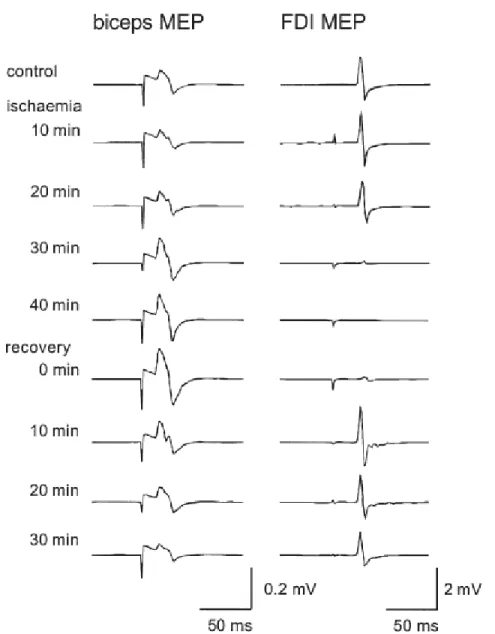
Il est également possible d’induire une plasticité des cartes corticales de manière expérimentale chez l’individu sain. L’application d’un bloc compressif pour induire une déafférentation ischémique transitoire permet simuler expérimentalement une amputation et entraîne le développement d’une plasticité des cartes corticales de M1 (Brasil-Neto et al., 1992; Brasil-Neto et al., 1993a; Tinazzi et al., 1997). L’utilisation de ce modèle expérimental permet d’observer les changements plastiques se mettant en place dès les premières minutes après la déafférentation. Comme le montre la Figure 1, la mesure de l'excitabilité corticospinale par TMS à la suite de l’application d’une déafférentation ischémique transitoire au niveau de la main révèle une augmentation de la taille des potentiels moteurs évoqués (MEP de l’anglais Motor Evoked Potential) au niveau des muscles proximaux à la déafférentation (Brasil-Neto et al., 1992; Ziemann et al., 1998b). Il est également possible avec la TMS de montrer une augmentation du nombre de sites sur le scalp qui, lorsque stimulés, provoquent une activation de ces muscles proximaux, reflétant ainsi une augmentation de la taille des représentations corticales (Brasil-Neto et al., 1993a; Ridding and Rothwell, 1995). Toutefois, cette augmentation de la taille des cartes ne peut être clairement dissociée du changement d’excitabilité corticospinale (Gagne et al., 2011). L’absence de modulation des réponses obtenues à la suite de stimulations électriques transcrânienne ou spinales suggèrent cependant que les changements observés avec la TMS sont liés à des processus prenant place au niveau de M1 plutôt qu’à des niveaux
sous-corticaux (Brasil-Neto et al., 1993a). Des études pharmacologiques ont été réalisées afin de mieux comprendre les mécanismes supportant le développement d’une plasticité induite par une déafférentation. En testant diverses substances et leurs effets sur les changements induits par une déafférentation ischémique transitoire, Ziemman et ses collaborateurs (Ziemann et al., 1998b) ont montré que l’augmentation de l’excitabilité corticospinale observée était bloquée par la prise de Lorazepam (agoniste du GABA) et était donc liée à des mécanismes GABAergiques. Cette observation suggère que l’augmentation de l’excitabilité corticospinale des muscles proximaux résulterait d’une levée d’inhibition issue en temps normal des neurones des représentations voisines (ici du membre déafférenté) et entraînerait la mise en action de synapses latentes via un phénomène de « démasquage » conformément aux observations réalisées dans les études animales (Welker et al., 1989; Garraghty et al., 1991; Jacobs and Donoghue, 1991).
Figure 1 : Évolution de l’excitabilité corticospinale du FDI (first dorsal interosseous) et du biceps lors de l’application d’une déafférentation ischémique transitoire au niveau de l’avant-bras.
(McNulty et al., 2002). L’application de la déafférentation ischémique entraine une baisse graduelle de l’excitabilité corticospinale du FDI se traduisant par une diminution de l’amplitude des potentiels moteurs évoqués (MEP). À l’opposé, l’excitabilité corticospinale des muscles situés en amont de la déafférentation (ici le biceps) augmente graduellement durant la déafférentation. Une fois la déafférentation interrompue (recovery), l’excitabilité corticospinale des muscles testés retourne à son niveau de base.
b) Plasticité à long terme
Afin d’explorer la plasticité se développant à plus long terme à la suite d’une déafférentation, la recherche s’est notamment intéressée aux patients ayant subi une amputation depuis plusieurs années. En explorant les modifications de l’excitabilité de la voie corticospinale sur ces patients à l’aide de la TMS, il a été possible de montrer que cette
déafférentation à long terme entraîne une augmentation de la taille des MEPs des muscles proximaux au site de l’amputation et une diminution de leur seuil moteur au repos (Cohen et al., 1991; Fuhr et al., 1992; Röricht et al., 1999; Gagne et al., 2011). Enfin, en comparant la taille de la réponse électromyographique (EMG) à la réponse M (correspondant à la réponse à une stimulation directe des fibres motrices), Cohen et al. ont estimé qu’une même stimulation recrute un plus grand nombre de motoneurones au niveau des muscles proximaux au site de l’amputation comparativement au côté sain (Cohen et al., 1991). Les modifications du seuil moteur sont absentes lorsqu’on étudie une désafférentation à court terme (Chen et al., 2002), suggérant qu’elles requièrent plus de temps pour se mettre en place. Cette plasticité qui se développent à long terme chez les patients amputés reposeraient alors sur des mécanismes liés à l’activité des canaux sodiques puisqu’il est possible d’augmenter le seuil moteur par l’utilisation de drogue qui bloque les canaux sodiques (Ziemann et al., 1996a) tandis que ceux rapidement mis en jeux après une déafférentation, reposent plutôt sur le système GABAergique (Ziemann et al., 1998b). L’utilisation de la neuroimagerie a également permis de mettre en lumière l’étendue des réorganisations corticales se développant à la suite d’une amputation. Notamment, il a été observé qu’une déafférentation entraine, au sein de cortex sensorimoteur, une réduction de la connectivité fonctionnelle interhémisphérique (Makin et al., 2013; Xie et al., 2013) montrant qu’une déafférentation entraine des réorganisations qui ne sont pas limitées au cortex sensorimoteur controlatéral (Schwenkreis et al., 2003b; Simões et al., 2012). Il a également été montré en utilisant la TMS que la déafférentation peut entrainer une modification du centre de gravité des cartes corticales ipsilatérales ainsi qu’une diminution de l’inhibition interhémisphérique (Werhahn et al., 2002; Schwenkreis et al., 2003b). Par conséquent, les interactions interhémisphériques sont une composante à prendre en compte lorsque l’on s’intéresse à la plasticité induite par une lésion.
1.2.3 Plasticité induite par un apprentissage
Le système nerveux central est donc capable de se réorganiser en réaction à l’apparition de lésions périphériques. Mais la plasticité peut également se développer en dehors de toutes atteintes de l’organisme, par le biais, par exemple, de l’apprentissage moteur.
L’apprentissage moteur réfère aux processus par lesquels un mouvement est exécuté plus précisément et rapidement avec de l’entraînement ou la répétition (Willingham, 1998). Il est habituellement découpé en trois composante : 1) l’acquisition, qui correspond au processus par lequels les performances s’améliorent au fil de l’apprentissage; 2) la rétention, qui correspond au phénomène permettant le maintien des habiletés; 3) le transfert ou la généralisation de cet apprentissage à d’autres tâches ou segments corporels (Adams, 1987).
a) Études chez l’animal
Afin d’étudier l’hypothèse qu’un apprentissage moteur est associé à une plasticité corticale, Kleim et son équipe ont entrainé des rats adultes à effectuer une tâche d’atteinte (ou
reaching en anglais) (Kleim et al., 1998). Selon le groupe auquel les rats appartenaient, ils
devaient atteindre leur nourriture placée sur une plateforme rotative soit en passant la patte à travers une fente (skilled reaching) ou simplement en pressant une barre (unskilled
reaching). La comparaison de la cartographie corticale des membres réalisée avant et après
l’entraînement a montré que les rats ayant effectués le skilled reaching présentaient une représentation corticale du poignet et des doigts significativement plus étendue comparativement à ceux du groupe unskilled reaching. La réalisation d’un entraînement moteur a donc induit une réorganisation corticale des membres impliqués dans la réalisation de la tâche, supportant l’idée de la mise en place d’une plasticité « usage-dépendante ». L’étude des réflexes a permis de démontrer que la plasticité pouvait également se développer au sein de la moelle épinière. L’étude du réflexe H permet par exemple, de mesurer l’excitabilité des motoneurones au sein de la moelle épinière (Pierrot-Deseilligny and Mazevet, 2000; Misiaszek, 2003). Le réflexe H est un réflexe monosynaptique consistant à appliquer une stimulation électrique directement sur le nerf afin d’activer les fibres sensorielles Ia ce qui va entraîner une réponse motrice (Pierrot-Deseilligny and Mazevet, 2000). À l’aide d’une tâche de conditionnement opérant, Wolpaw et son équipe ont montré que l’amplitude du réflexe H chez le singe peut être modulée. L’enregistrement des motoneurones de la moelle épinière a permis de montrer que l’augmentation de l’amplitude du reflexe H était due à une levée de l’inhibition du motoneurone tandis qu’une
diminution du réflexe H était liée à une augmentation du seuil d’activation des motoneurones (Carp and Wolpaw, 1994, 1995).
Il est intéressant de noter que la nature de l’entraînement va influencer la plasticité qui va se développer, et ceci, tant au niveau cortical qu’au niveau spinal. Ainsi l’entraînement à une tâche d’habileté induit non seulement une réorganisation des cartes corticales, mais aussi une augmentation de la densité dendritique (Greenough et al., 1985; Withers and Greenough, 1989) et du nombre de synapses par neurone (Kleim et al., 1996; Kleim et al., 2004; Adkins et al., 2006). En revanche, un entraînement moteur focalisant sur la force entraine une diminution du potentiel moteur maximal évoqué par la TMS et n’entraine aucune modification des cartes corticales (Remple et al., 2001; Adkins et al., 2006). Ces différences de phénomènes plastiques mis en jeu selon le type d’apprentissage se retrouvent également au niveau spinal. Par exemple, un entraînement nécessitant de la force et non le développement d’habiletés va accroitre le nombre de synapses excitatrices connectées aux motoneurones innervant le muscle impliqué dans la tâche (Remple et al., 2001).
Dans l’ensemble, ces observations dénotent une caractéristique importante de la plasticité se développant à la suite d’un apprentissage moteur : le type d’apprentissage moteur (force ou habileté) dicte la nature et la localisation de la plasticité induite.
b) Études chez l’humain
Les modifications plastiques liées à un apprentissage moteur observées chez l’homme présentent des similarités avec celles observées chez l’animal (Weinberger, 1993; Karni et al., 1995; Draganski et al., 2004). Des études utilisant des outils de neuroimagerie tel que l’IRMf et la TEP montrent que l’apprentissage d’une tâche motrice va mettre en jeu un nombre important de structures cérébrales. Doyon et Ungerleider ont par exemple proposé un modèle d’apprentissage reposant sur l’existence de deux circuits mettant en relation structures corticales et sous-corticales que sont les circuits striatal et cortico-cérébelleux (Doyon et al., 2002; Doyon et al., 2003). Ces deux systèmes agiraient de manière couplée lors de la première phase rapide d’apprentissage mais se dissocieraient lors de la phase plus lente (voir Doyon and Benali, 2005; Doyon et al., 2011).
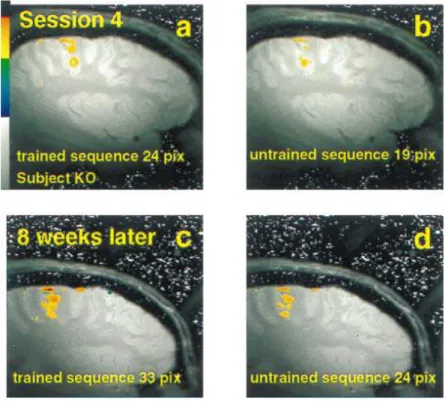
Si l’activité d’un grand nombre de structures a été mise en cause dans les phénomènes d’apprentissage, le cortex moteur primaire a été une des premières régions cérébrales dont l’implication a été révélée (Grafton et al., 1992; Floyer-Lea and Matthews, 2005). Dès 1995, Karni montre qu’après plusieurs jours ou semaines d’apprentissage d’une séquence de mouvements de doigts, les sujets entrainés présentent une activité cérébrale plus importante au sein du cortex moteur primaire que les sujets non entrainés (cf. Figure 2), et cette différence augmente encore après 8 semaines d’entraînement (Karni et al., 1995). Cette augmentation de l’activité cérébrale est corrélée avec l’amélioration des performances.
Figure 2 : Activation cérébrale des représentations motrices des doigts.
(Karni et al. PNAS 1995, Copyright (1998) National Academy of Sciences, U.S.A). Activation cérébrale des doigts chez des participants ayant effectué (trained sequence) ou non (untrained sequence) un entraînement à une tâche séquentielle. L’entraînement cause une augmentation significative de la représentation corticale des doigts après huits semaines chez les sujets appartenant au groupe trained.
c) Études utilisant la TMS
La TMS a été particulièrement utile afin de comprendre l’implication de M1 lors de l’apprentissage moteur en permettant la mesure l’excitabilité corticospinale via l’enregistrement de l’amplitude de la réponse EMG produite par le stimulation. Il est également possible de mesurer différents marqueurs neurophysiologiques au sein de M1. Par exemple, le recours à des protocoles de stimulations pairées permet de tester l’état des systèmes inhibiteurs et facilitateurs de M1. En observant la variations des ces différentes mesures, il est possible d’explorer plus en détails les mécanismes sous-jacents à la plasticité se développant au sein de M1 (Chen, 2000; Chen and Udupa, 2009).
Une des premières études ayant utilisé la TMS pour explorer les modifications induites par un apprentissage moteur sur le cortex moteur primaire a été réalisée par Pascual-Leone et son équipe en 1994. À l’aide de la TMS, ils ont effectué une cartographie du muscle de l’index (FDI, de l’anglais first dorsal interosseus) avant et durant l’apprentissage d’une tâche séquentielle implicite mesurant le temps de réaction (Pascual-Leone et al., 1994a). Les résultats ont montré que l’apprentissage de la tâche entraine une amélioration des performances qui s’accompagne de l’élargissement de la carte corticale du FDI. En revanche, lorsque la séquence devient explicite pour le participant, on observe une rétraction de la carte corticale du FDI, celle-ci revenant à sa taille initiale. Cette expérience fût l’une des premières à montrer les modifications transitoires induites par un apprentissage moteur au niveau de M1. Les études suivantes ayant également utilisées la TMS pour explorer la plasticité induite par un apprentissage moteur ont permis de montrer plusieurs changements physiologiques liés à la réalisation d’un apprentissage moteur. Cependant, la grande variété des paradigmes utilisés rend complexe la liaison systématique entre variation de performance et changement plastique. Ainsi, alors que Pascual-Leone rapporte un retour au niveau d’excitabilité de base à la suite de l’entraînement, la majorité des études rapporte une augmentation de l’excitabilité corticospinale qui se maintient pendant toute la phase d’apprentissage (Muellbacher et al., 2001; Svensson et al., 2003b; Koeneke et al., 2006; Svensson et al., 2006; Bagce et al., 2013). Certaines études révèlent aussi une diminution du seuil moteur des muscles impliqués dans la tâche (Pascual-Leone et al., 1995; Jensen et al., 2005). L’augmentation de l’excitabilité observée est également accompagnée d’une diminution de l’inhibition intracorticale (Gallasch et al., 2009; Smyth
et al., 2010; Coxon et al., 2014). En revanche, lorsque Holland et ses collaborateurs mesurent l’excitabilité avant et après la réalisation de blocs d’apprentissage moteur, ils observent non pas une augmentation de l’excitabilité mais au contraire une diminution (Holland et al., 2015) répliquant une observation déjà réalisée par McDonnell et Ridding (McDonnell and Ridding, 2006). Smyth et son équipe montrent quant à eux une augmentation de la tailles des réponses motrices évoquées, mais elle n’apparait que lors de la phase de rétention et est absente lors de l’acquisition de la tâche. Le type de tâche motrice demandé semble également influer sur les modifications de l’excitabilité engendrées par l’apprentissage puisqu’un entraînement en force ou nécessitant l’application graduelle d’une force n’entrainera pas de modification de l’excitabilité corticospinal (Muellbacher et al., 2001; Jensen et al., 2005).
À l’aide de techniques de stimulation cérébrale non-invasive telle que la stimulation magnétique transcranienne répétitive (rTMS) ou la stimulation transcraienne à courant continue (tDCS), il est possible de moduler l’état d’excitabilité de M1. La modification de l’état de M1 va alors déteriorer les performances issues de l’apprentissage (Nitsche et al., 2003; Boggio et al., 2006; Reis et al., 2009) confirmant le rôle prépondérant de M1 dans les processus d’apprentissage moteur.
L’ensemble de ces observations permet de démontrer que M1 est une structure clé dans les mécanismes d’apprentissage lors d’un entraînement à une nouvelle tâche motrice, notamment lorsque cette tâche implique des habiletés motrices fines. La plasticité résultant d’un entraînement moteur implique des mécanismes complexes et reposants sur des changements d’ordre fonctionnel. La nature de la tâche tout comme les conditions dans lesquelles l’entraînement se déroule influencent la plasticité.
1.3 Le phénomène de la douleur
1.3.1 L’expérience de la douleur
Tout individu a un jour ou l’autre fait l’expérience de la douleur, définie par l’Association Internationale pour l’Étude de la Douleur (IASP, de l’anglais International Association for