UNIVERSITÉ
DU
QUÉBEC À MONTRÉAL
RÉACTIONS
IPSO-OXYDATIVES,
CYCLOADDITIONS
DÉSAROMA
Tl SANTES ET
SYNTHÈSE FORMELLE
DE LA
STRYCHNINE
THÈSE
PRÉSENTÉE
COMME ÉXlGENCE
PARTIELLE
DU
DOCTORAT EN CHIMIE
P
A
R
GU
IL
LAU
M
E
J
ACQ
U
E
MOT
Avertissement
La
diffusion de cette thèse se fait dans le respect des droits de son auteur, qui a signé le
formulaire
Autorisation de reproduire et de diffuser un travail de recherche de cycles
supérieurs
(SDU-522 - Rév.01-2006). Cette autorisation stipule que
«conformément
à
l'article
11 du Règlement no 8 des études de cycles supérieurs, [l'auteur] concède
à
l
'
Université du Québec
à
Montréal une licence non exclusive d'utilisation et de
publication de la
totalité
ou d'une partie importante de [son] travail de recherche pour
des fins pédagogiques et non commerciales
.
Plus précisément
,
[l'auteur] autorise
l'Université
du Québec
à
Montréal
à
reproduire
,
diffuser
,
prêter, distribuer ou vendre des
copies
de [son] travail de recherche
à
des fins non commerciales sur quelque support
que ce soit, y compris l
'
Internet. Cette licence et cette autorisation n'entraînent pas une
renonciation de [la) part [de l
'
auteur]
à
[ses) droits moraux ni
à
[ses) droits de propriété
intellectuelle. Sauf entente contraire
,
[l
'
auteur] conserve la liberté de diffuser et de
commercialiser ou non ce travail dont [il] possède un exemplaire.»
REMERCIEMENTS
Je
souhaiterais
tout d
'
abord
remercier chaleureusement
le Pr.
Sylvain Canesi
de m
'avo
ir
donné 1
'opp01tunité de
faire
mon doctorat dans
son
laboratoire
.
Ces
trois
années ont été très
enrichissantes et
il
a toujours été
présent lorsque j
'
en
avais besoin.
Sa créativité
sa
ns limites,
ses
conseils avisés et son expérience ont été essentiels à la réussite de mon doctorat.
Je
voudrais également
remercier le Pr.
Livain Breau,
direct
e
ur du département
,
ainsi
que le
Pr. Huu
Van Tra,
directeur du progamme de doctorat
,
pour leur travail
au sein
du
département durant ces trois
années.
J'aimerais aussi
remercier mes
collègues
du laboratoire
sans
qui
ces années de
recherche
s
scientifiques
n'
auraient
pas
été aussi
agréables. Marc-André,
Gaëtan,
Chantal,
Sam
,
Marco,
Chloé, Amandine, votre soutien ainsi
que les moments
agréables passés au
laboratoire ou en
dehors resteront des
souvenirs
inoubliables
.
Je remercie tout particulièrement Marco
et Chloé
pour leur fantastique travail afin de developper les réactions de cycloaddition et de
couplage.
Je tiens
également à exprimer
toute ma
gratitude à Alexandre Arnold
pour
so
n
expe1tise
RMN
,
ainsi
que Lemme Oh! und
et Vladimir Kriuchkov
pour leurs analyses HRMS
.
Je
voudrais aussi
remercier tous les
amis et
membres de
s
laboratoires du département de
chimie de I'
UQAM pour leur sympathie.
Je
tiens
également à remercier particulièrement
ma
famille pour tout ce qu
'
elle
a
fait
pour
moi
tout au
lon
g
de mon
parcours académique. Son soutien, aussi bien
moral
que financier
m'a permis d
'
a
ll
er au
bout de mes
études et
d'avan
cer dans
l
a vie.
Enfin
,
je
voudrais
remercier de tout mon
cœur
Pauline pour
so
n
soutien
,
sa capacité à
me
supporter ainsi
que tout
ce
qu
'e
ll
e
m
'a
pporte au
quotidien.
TABLE DES MATIÈRES
LISTE DES FIGURES
...
.
....
..
..
.
..
..
..
.
..
.
...
..
....
.
..
...
..
....
..
..
..
...
....
.
...
..
...
..
...
.
... v
ii
LISTE DES
ABRÉVIATIONS,
SIGLES
ET
ACRONYMES
...
..
....
....
.
...
..
...
..
...
i
x
RÉSUMÉ ...
.
...
.
.
.
.
...
.
...
...
.
..
.
...
...
..
..
..
.
..
.
...
....
.
..
.
..
.
..
.
.
..
.
....
.
.
.
.
..
..
...
..
..
...
.
...
..
..
...
.
. x
iii
ABSTRACT ....
..
...
.
..
.
...
..
.
...
.
.
..
.
...
.
..
.
.
.
...
.
.
...
.
...
.
...
.
..
...
.
.
..
.
.
.
..
.
..
..
.
.
.
...
.
...
.
.
...
.
.
..
...
.
.
...
.
...
.
.
.
. xv
INTRODUCTION
...
.
.
...
.
...
..
.
..
.
...
.
.
..
.
..
.
.
.
.
.
...
.
.
.
...
.
.
.
..
..
..
.
..
..
.
...
.
..
..
...
..
..
.
...
.
...
.
1
O
.
1
.
I
ode
hyp
erva
l
ent
...
..
....
....
..
....
...
..
...
...
...
...
...
..
....
...
1
O.
2.
Umpolung
et
Oxydation à
l
'
iode
h
yperva
l
ent..
...
..
....
..
...
..
....
...
..
..
..
..
..
....
....
..
..
..
...
4
O.
3.
Réactions ipso ...
..
..
..
..
....
..
...
.
...
..
....
....
.
.
....
.
..
...
...
..
..
...
....
...
..
.
.. 8
O
.
4
.
Cyc
1
oad
dition
s ...
..
.
..
....
....
..
...
...
....
.
..
...
....
..
....
....
....
...
..
...
...
...
1
2
O.
5. Sy
nth
èse
de Strychnine ...
.
...
.
....
..
..
..
..
.
..
...
..
..
...
..
...
..
....
1
6
CHAP
IT
RE
I
RÉACTIONS
IP
SO
-OXYD
A
TIVES
ET SYNTHÈSE
DE
LA SCELÉTÉNONE ..
..
..
..
... 21
1
.
1. Introduction
...
..
...
...
...
...
..
.
...
...
..
....
..
..
...
.
...
..
...
..
.
.
..
....
..
...
...
..
.
..
... 2
1
1
.
2.
Informations
s
uppl
é
m
e
nt
aires ...
..
...
..
..
...
..
...
...
..
...
.
.
...
..
..
2
1
1
.
3. Conc
lu
sio
n
...
....
..
..
...
....
..
.
.
...
...
...
..
....
..
.
..
...
..
..
..
...
..
...
..
.... 22
CHAP
I
TRE
li
RÉACTIONS
DE
CYCLOADDITIONS OXYDATIVES ET
DE
COUPLAGES SUR
DES
DÉRIVÉS
AROMATIQUES
NON-ACTIV
É
S
...
...
..
.... 2
3
2. 1
.
Introduction ..
.
.
...
...
.
.
....
...
..
..
...
.
...
.
...
...
...
..
.
..
..
.
.
.
.
.
...
.
.
....
.
.
.
.
..
.
...
..
... 23
2
.
2
.
Inf
o
rmation
s
supplémentair
es ...
...
..
...
...
..
..
...
...
..
..
..
...
....
..
..
..
..
.
..
..
...
... 2
4
2. 3.
Co
n
c
lu
s
i
o
n .
...
...
..
.
...
..
...
.
...
...
.
.
.
...
.
..
.
...
.
...
..
....
.
...
..
.
.
..
.
...
.
...
...
..
...
.
.
.
.
24
CHA
PI
TRE
III
SYNTH
È
S
E
FORM
E
L
LE
D
E LA
STRY
C
HNIN
E
..
..
..
...
.
....
..
..
....
...
..
...
....
....
..
.
25
3.
1. In
t
roduction
..
.
.
.
...
.
..
.
...
.
...
.
...
..
.
...
...
..
..
..
...
.
..
.
...
.
...
.
...
.
.
..
...
.
..
...
... 25
3
.
3
.
Perspectives et travaux futur
s
.
.
.
.
..
.
.
..
...
.
...
.
....
..
.
..
...
.
...
.
.
.
...
.
...
..
.
..
..
..
.
....
.
..
...
.
.
.
..
.
...
.
. 26
3
.
4
.
Conclusion
.
.
.
.
...
..
.
.
..
.
.
....
.
.
.
...
.
..
.
.
.
.
....
.
.
...
...
.
..
.
.
.
...
.
.
.
..
.
..
...
...
..
.
..
....
.
.
.
..
..
..
..
.
...
..
.
.
.
...
.
...
.
...
.
27
CONCLUSION
.
...
..
..
.
.
..
.
...
...
.
.
.
..
...
.
.
.
.
.
...
.
..
.
.
.
....
.
..
.
.
.
.
..
.
.
.
..
.
...
..
...
.
....
..
...
...
.
..
.
.
....
.
...
.
..
...
..
.
29
ANNEXE A:
....
..
...
..
..
...
..
..
...
..
...
....
..
..
..
..
.
..
...
..
..
..
...
.
..
..
...
...
..
..
..
..
..
..
..
..
31
"
OXYDA TIVE /P
S
O-REARRANG
E
MENT PERFORMED
BY
A HYPERVAL
E
NT
IODINE
REA G
E
NT AND ITS APPLI
C
ATION
"
ARTICL
E
..
....
....
....
..
..
..
..
..
...
..
....
..
..
..
...
..
.
31
ANNEXE B : .
..
...
.
..
...
..
..
.
...
.
...
.
.
..
.
.
..
..
.
....
.
..
..
..
..
..
.
.
...
..
..
.
.
...
...
..
..
.
....
.
..
.
..
.
..
...
.
.
...
..
..
.
.
..
.
.
.
.
...
... 39
"
OXYDATIVE /P
S
O-REARRANG
E
MENT PERFORMED
BY
A HYPERVALENT
IODINE
REA GENT AND ITS APPLICATION
"
SUPPORTING
INFORMATION
...
..
... 39
ANNEXE C
:
...
.
..
....
.
.
....
.
...
.
.
.
....
.
.
.
.
.
.
..
...
.
...
...
.
...
.
...
..
...
..
.
.
..
..
..
..
...
.
.
.
.
..
.
.
.
.
..
..
.
.
.
...
..
.
85
"
OXIDA TIVE CYCLOADDITION AND
C
ROSS-COUPLING PROCESSES ON
UNACTIV ATED BEN
Z
ENE DERIVATIVES
"
ARTICLE
....
...
..
..
..
..
..
..
..
..
...
..
..
..
..
...
.
85
ANNEXE D
: .
...
..
..
..
...
....
...
...
..
...
..
....
..
..
.
..
...
...
.
...
..
..
...
...
..
... 93
"OXIDA TIVE CYCLOADDITION AND CROSS-COUPLING
PROCESSES
ON
UNACTIVAT
E
D B
E
NZENE DERIVATIV
E
S
"
SUPPORTING INFORMATION
...
93
ANNEXEE :
....
..
.
..
.
.
..
.
.
..
..
...
.
....
...
.
..
.
...
...
...
....
..
...
.
...
.
....
.
..
..
..
.
...
..
...
..
.
...
...
.
..
2
15
"
A CONCISE FORMAL SYNTH
E
SIS OF STRYCHNINE
"
ARTICLE ..
..
..
..
....
..
...
..
..
..
..
. 2
15
ANNEXEF
:
..
..
..
.
...
...
..
.
...
....
..
...
..
...
..
....
..
..
.
..
...
....
..
...
..
...
....
..
..
...
.. 2
19
"
A CONCISE FORMAL SYNTHESIS OF STRY
C
HNINE" SUPPORTING
INFORMATION
.
....
..
...
....
...
..
..
..
....
..
....
...
..
..
....
...
...
...
..
....
... 219
RÉFÉRENC
E
S
...
.
.
..
..
..
...
.
.
..
..
.
.
..
.
...
..
..
..
.
...
..
.
.
.
..
..
.
..
.
.
.
..
.
.
.
..
...
.
.
.
.
.
.
.
.
.
.
.
.
...
...
.
.
.
..
.
..
..
..
.
...
.
..
.
...
..
.
.
2
4
3
Figure
0
.
1
0.
2
0.3
0.4
0
.
5
0
.
6
0.
7
0
.
8
0
.9
0
.
10
0
.
11
0
.1
2
0
.
1
3
0
.
14
0.15
0.16
0
.
17
0.
1
8
0.
1
9
0.20
0
.2
1
0
.
22
0.2
3
0
.
2
4
0
.
25
0.26
LISTE DES
FIGURES
Page
Réac
tifs à base
d
'
iode
h
yperva
l
e
n
t...
.
.
..
.
.
..
...
..
..
..
.
.
.
..
..
....
..
.
.
.
..
..
...
.
.
...
...
...
...
....
...
..
.. l
Structures des réactifs à
l
'
iode
h
yperva
l
e
nt
..
..
..
.
..
....
.
..
.
...
..
...
...
..
...
..
2
Réactions de fo
n
ct
io
nn
a
li
sation à
l
'
iode
h
yperva
l
ent
...
..
...
..
...
..
... 2
Mécani
s
m
es poss
ibl
es
d
'
oxydati
o
n
de phé
nol
s ....
..
..
..
..
....
..
..
...
..
..
..
..
....
..
...
....
3
Oxydatio
n
de phéno
l
s par
IB
X ..
...
...
..
....
...
..
..
....
...
...
...
...
..
..
..
....
..
... .4
Désaromat
isati
ons énantionsé
l
ectives cata
l
yt
iques en iode hyp
e
rva
lent ..
...
..
..
..
..
.4
Réac
tions d
'
Umpo
lu
ng Seebach et Co
rey ..
..
..
..
....
...
..
....
..
..
...
..
..
....
... .4
Réac
tion de co
nd
e
n
satio
n
be
n
zoïne ...
....
...
..
....
...
...
..
....
..
..
..
..
...
..
....
..
...
.
. 5
Réac
tion de Stetter
...
...
....
..
..
....
.
....
...
.
....
..
...
..
..
...
..
..
..
..
..
..
....
..
...
....
...
..
...
...
.
5
Addition asymétriqu
e d
'
é
n
a
l
s sur des
nitro-alcènes cata
l
ysée
par des carbènes
N-hétérocyc
liqu
es ..
....
..
...
.
...
....
.
...
..
....
..
..
.
.
..
...
...
..
...
..
...
..
... 5
Addition asymétriqu
e d
'
h
omoé
no
l
ate
s s
ur des acy
l
phosph
onate
s
cata
l
ysée
par des carbè
n
es N-hétérocyc
liques
.
...
.
....
....
...
..
....
.
..
...
..
..
.
...
.
...
.
...
.
.
..
.
...
. 6
Méca
nisme radi
ca
l
aire d
'
oxydation à
l
'
iode
h
yperva
l
e
n
t ....
..
..
..
...
...
..
...
....
..
.. 7
Addition
nu
c
l
éophile s
ur
un phé
n
o
l
ou une s
ulf
onamide
...
..
.
..
..
...
.
..
...
..
..
..
..
8
Réaction de substituti
o
n I
pso ..
..
....
..
....
...
..
...
...
..
...
..
..
..
..
...
..
....
..
...
....
..
..
.
..
..
.
8
Applicabilité des s
ub
stitutions
Ip
so a
u
x oxydatio
n
s
à
l'
i
ode hyperva
l
ent
....
...
....
.
9
Réacti
o
n
s de Friede
l
et C
r
afts oxydatives
...
...
..
....
..
..
..
..
..
..
....
...
...
...
9
Application
à
la synthèse de
l
a Mésembrine ...
..
....
...
....
..
...
..
....
....
.
... 9
Trans
positio
n 1
,
2 de ty
pe Wa
g
ner-Meerwein
..
..
..
..
....
....
....
....
..
...
..
....
..
....
..
..
..
..
.
10
T
ran
s
position 1
,
3 et application
à
la
s
ynthèse de 1
'
Ac
é
ty
l
as
pid
o
albidine
..
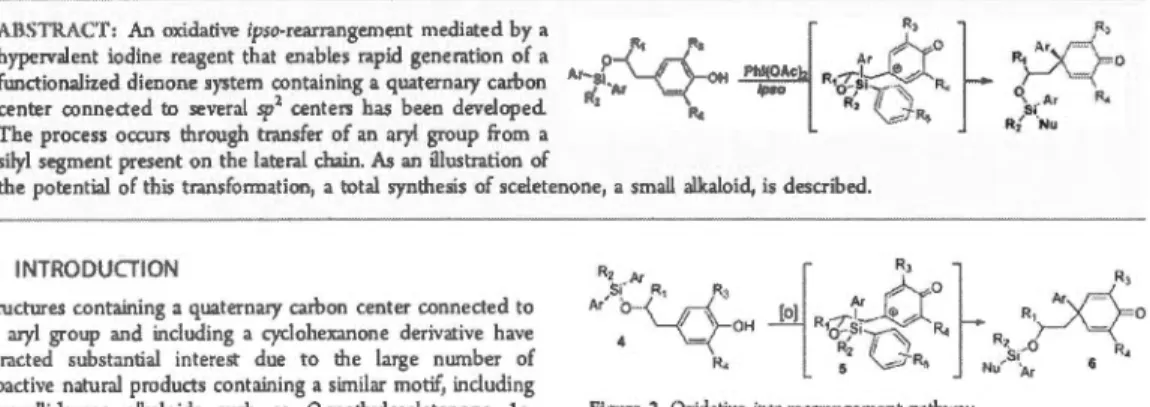
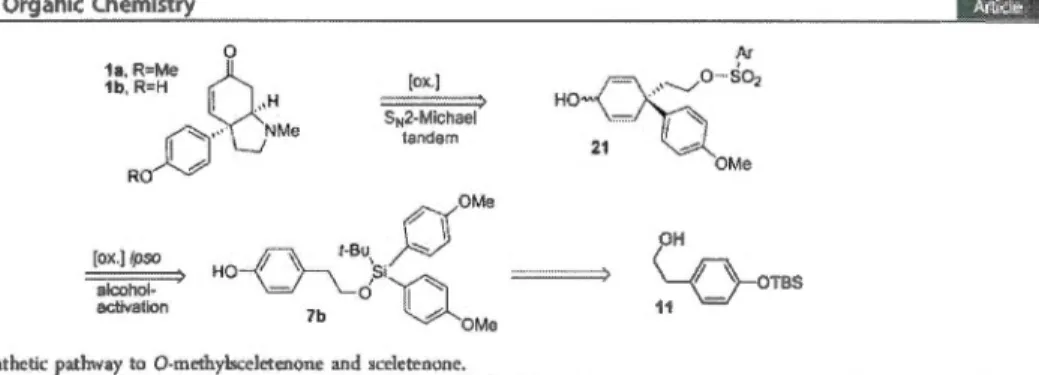
... 10
Méca
nisme des réactions ip
s
o-oxydatives
..
..
..
...
....
...
..
..
....
....
...
..
..
..
..
....
..
11
App
lication à la synth
ès
e de l
a
Scel
é
t
é
none
....
..
....
..
...
..
...
..
..
..
..
..
..
..
..
...
1
2
Réact
ion de cycloaddi
t
ion
1
,
3 dipôlaire ..
..
....
..
..
.
..
....
..
..
...
...
...
.. 12
O
rbit
a
l
es
mol
é
culair
es e
t int
é
r
a
ti
o
n
s
H
O
/
B
V ....
..
..
...
....
...
...
....
...
..
...
1
2
Exe
mpl
es
d
e
Dip
ô
l
es
1
,
3
..
..
...
..
..
...
..
..
..
..
..
..
....
...
..
...
..
... 13
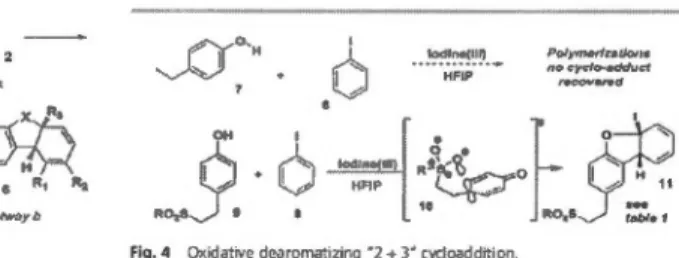
Cy
cloaddition [
2+
3]
d
e
ph
é
nol
e
t d
e
furane en pr
ése
nc
e
d
'
iod
e
h
y
p
e
r
v
alent ..
..
. 1
3
App
lication au
x
s
y
nthè
s
e
s
du (
±
)
-
panacène et du (
±
)-de
s
bromopanacène
..
..
....
.
13
0.27
Cycloaddition [2+3] asymétrique et synthèse de I
'
Aflatoxin 82
...
.
.
.
.
.
.
.
.
..
..
....
.
14
0
.
28
Réactions de couplage de N-aryl méthanesulfonamides et de thiophènes
..
.
.
.
.
...
14
0
.
29
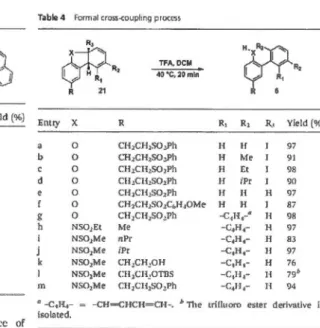
Réactions de Cycloadditions et de Couplages ....
.
...
.
...
..
.
...
.
..
...
..
.
..
.
...
.
.
.
.
.
..
.
..
....
15
0.30
Mécanisme des cycloadd itions désaromatisantes
...
.
..
..
...
..
...
.
.
...
..
.
..
.
.
.
..
..
.
.
...
15
0.31
Alcaloïdes du genre Strychnos ...
...
.
....
.
...
.
..
..
...
.
...
.
..
.
...
..
.
.
..
....
.
.
.
...
.
.
..
.
..
.
16
0.32
Biosynthèsede la Strychnine ..
...
.
.
....
.
...
.
...
..
..
.
.
.
.
.
.
.
..
.
....
.
.
..
...
.
..
...
...
..
..
..
.
.
...
17
0
.
33
Rétrosynthèse de Woodward .
..
...
..
...
.
...
.
..
..
.
.
....
..
...
.
.
..
.
....
.
...
.
.
..
.
..
.
....
.
..
..
.
.
..
.
1
8
0
.
34
Rétrosynthèse de Rawal ...
.
.
..
...
...
.
.
..
..
..
....
.
.
..
.
.
.
.
.
...
.
..
.
...
.
.
...
.
.
...
..
..
19
0
.
35
Schéma rétro
s
ynthétique ....
..
.
..
...
.
...
.
...
.
...
...
...
...
..
..
...
..
.
..
...
.
..
.
..
.
..
.
..
.
.
..
.
.
..
...
20
LISTE DES AB
RÉ
VIA TI ONS
,
SIGLES ET ACRONYMES
A
Ang
s
trom
Ac
Acétyle
AcOH
Acide
acétique
A cO
Et
Acétate d
'é
thyle
Ali
Allyle
aq.
Aqueux
Ar
Aryle
Bn
Benzyle
BBr
3
Tribromure
de bore
Br
Brome
BuLi
Butyl lithium
BV
Basse
vacante
CCM
Chromatographie
sur couche mince
CHCb
C
hloroforme
Cl
Chlore
DCM
Di
ch
lorométhane
DEAD
Diéthylazodicarboxylate
DIB
(Diacétoxy )iodobenzène
DIBAL-H
H
y
drure de Diisobutylaluminium
DMAP
Diméthylaminopyridine
DMF
Diméthylformamide
DMP
Dess-Martin
p
ér
iodinan
e
E
É
l
ect
r
ophi
l
e
El
É
liminati
on El
Et
Éthy
le
Et
3
N
Triéthylamine
EtOH
Éthanol
Et
2
0
Glc
H
H
2
HFIP
HO
HRMS
IBX
K
2
C0
3
KHMDS
LiAlH4
Me
MeOH
NaH
NaBH4
NaCN
Na
2
C0
3
NaHC0
3
Na
2
S04
Na
2
S
2
0
3
NH
2
Me
NH4Cl
NMO
NsCl
N
u
0[0]
0
3
Os04
p
Pd
Diéthyl
éther
Glucose
Hydrogène
Di-Hydrogène
Héxafluoroisopropanol
Haute occup
é
e
Sprectroscopie
de Masse
Haute
Résolution
acide 2-iodoxybenzoïque
Carbonate
de potassium
Héxaméthyldisilazane
de potassium
Hydrure de lithium
alumium
Méthyle
Méthanol
Hydrure de
sodium
Borohydrure
de
sodium
Cyanure
de
sodium
Carbonate
de
sodium
Hydrogénocarbonate de
sodium
Sulfate
de
sodium
Thiosulfate
de
sodium
Méthylamine
Chlorure
d
'
ammonium
Oxyde
de
N-méthylmorpholine
Chlorure
de nos
y
le
N
u
c
l
éo
phil
e
Ort
h
o
Oxydation
Ozone
Tetroxyde
d
'
osmium
Para
Palladium
Pd
/
C
Ph
Phl
2 +Phl(OAc)2
PIB
PIFA
PPh3
i-Pr
RMN
RT
sat.
SET
S
N
2
SOCb
sl
TBAF
t-Bu
t-BuSiCh
TBDPS
TBDPS-Cl
TBS
TBS-Cl
TFA
TFE
THF
TLC
TMS
To
i
Tp
TPAP
Zn
Palladium
sur
charbon
Phényle
Iode hypervalent
(Diacétoxy )iodobenzène
B
is(pivalate )iodobenzène
bis(trifluoracétoxy)iodobenzène
Triphénylphosphine
iso-propyle
Résonance
Magnétique Nucléaire
"
Room temperature"
(température
pièce)
Saturée
Transfert d'électron célibataire
Substitution
nucléophile d'
ordre 2
Chlorure
de thionyle
Hybridation
sl
Fluorure
de tetrabutylammonium
tert-buty
le
tert-butyltrichlorosilane
tert-butyldiphénylsilyle
Chlorure
de tert-butyldiphénylsilyle
tert-butyldiméthylsilyle
Chlorure
de
tert-butyldiméthylsilyle
Acide trifluoroacétique
Trifluoroéthanol
Tétrah
y
drofurane
"
Thin La
y
er Chromato
g
raph
y
"
(
C
hromatographie sur couche mince)
Triméthylsilyle
To
l
y
l
e
T
e
mpérature pièc
e
P
é
rruth
é
nat
e
d
e
t
e
tr
a
p
ro
p
y
lammonium
Z
inc
RÉS
U
M
É
D
e
n
o
u
ve
ll
es
r
éa
cti
o
n
s
d
'
oxy
dati
o
n d
e
ph
é
n
o
ls
e
t d
'
a
ry
l-
s
ulf
o
n
a
mid
es
p
a
r d
es
r
éac
ti
fs
d
'
i
o
d
e
h
y
p
e
rv
a
l
e
nt
o
nt
é
t
é
d
é
v
e
l
o
pp
ées, a
in
s
i que d
es
appli
ca
ti
o
n
s e
n
sy
nth
èse
t
o
t
a
l
e
d
e
pr
o
dui
ts
n
a
tur
e
l
s.
Les
r
éac
ti
o
n
s
I
pso
-
ox
yd
a
tiv
es à
1
'
iod
e
hypervalent permett
e
nt la
gé
n
é
rati
o
n r
a
pid
e
d
'
un
e
di
é
n
o
n
e
f
o
n
c
ti
o
nn
a
li
sée co
nten
a
nt un c
a
rbon
e
quat
e
rnair
e co
nn
ec
t
é à
plu
s
i
e
ur
s ce
ntr
es
sp
2.Ce
pr
océ
d
é a
li
e
u p
a
r l
e
tr
a
n
s
f
e
rt d
'
un
g
roup
e
m
e
nt ar
y
l
e
p
o
rt
é
p
a
r un
s
ili
c
ium pr
ése
n
t
s
u
r
l
a
c
h
a
in
e
l
a
t
é
r
a
l
e
.
P
o
ur illu
s
tr
e
r l
e
p
o
t
e
nti
e
l de cette tran
sfo
rmati
o
n
,
l
a sy
nth
èse to
t
a
l
e
d
e
l
a
Sce
l
é
t
é
n
o
n
e
,
un
a
l
ca
l
o
ïd
e
d
e
l
a fa
mill
e
d
es A
m
a
r
y
ll
idaceae
,
a
é
t
é
r
éa
li
sée
.
D
es
r
éac
ti
o
n
s
d
e cyc
l
oa
dditi
o
n
s
[
2+3
] d
ésa
r
o
m
a
ti
s
ant
es
d
e
ph
é
n
o
l
s e
t d
'a
r
y
l-
s
ul
fo
n
a
mid
es s
u
r
d
es
d
é
ri
vés
d
e
b
e
n
zè
n
es e
t d
e
n
a
phtal
è
n
es
n
o
n
-ac
ti
vés o
nt
é
t
é
d
éve
l
o
pp
ées g
r
âce
à
l
'
utili
sa
ti
o
n d
e
r
éac
ti
fs à
l
'
i
o
d
e
hyperv
a
lent.
Ce
tte r
é
a
c
ti
o
n p
asse
p
a
r un
e a
dditi
o
n nu
c
l
éo
phil
e
in
t
r
a
m
o
l
éc
ul
a
ir
e s
ur un int
e
rm
é
di
a
ire d
e ty
pe Wh
e
l
a
nd
gé
n
é
r
é
dur
a
nt l
'
oxy
d
a
ti
o
n
.
D
es
r
éact
i
o
n
s
d
e co
upl
age
bi-
a
r
y
liqu
e o
nt
éga
l
e
m
e
nt
é
t
é
mi
ses a
u p
o
int d
e
m
a
ni
è
r
e
indir
ec
t
e
,
p
a
r
tr
a
it
e
m
e
nt
e
n
co
ndi
t
i
o
n
s ac
id
es
d
es
c
o
mp
osés
d
e
c
y
cl
oa
dditi
o
n
s
,
m
a
i
s a
u
ss
i d
e
m
a
ni
è
r
e
dir
ec
t
e
p
a
r l
'
utili
sa
ti
o
n d
'ary
l-
s
ulf
a
mid
es
.
E
nfin
,
la
sy
nth
èse fo
rm
e
ll
e
d
e
l
a S
tr
yc
hnine
,
un
a
lcal
o
ïd
e co
nnu p
o
ur
ses
pr
o
pri
é
t
és
bi
o
l
og
iqu
es
,
a é
t
é
r
éa
li
sée à
p
a
rtir du
3
-( 4
-
h
y
dr
oxy
ph
é
n
y
l
)
pr
o
pi
o
n
a
t
e
d
e
m
ét
h
y
l
e e
n
9 é
t
a
p
es.
Ce
tt
e sy
nth
èse
impliqu
e
un
e oxy
d
a
ti
o
n d
ésa
rom
a
ti
sa
nt
e
à
l
'
i
o
d
e
h
y
p
e
rv
a
l
e
nt
,
un n
o
u
vea
u
pr
o
c
é
d
é
t
a
nd
e
m a
za
Micha
e
l-
é
th
e
r d
'é
nol ain
s
i qu
'
un
e
c
yc
li
sa
ti
o
n p
a
r un
co
upl
age
d
e
H
ec
k
e
t
un
e
i
so
m
é
ri
sat
i
o
n r
é
du
c
tri
ce
.
A
B
S
TRA
CT
N
ew ox
id
a
ti
o
n r
eac
ti
o
n
s o
f ph
e
n
o
l
s a
nd
a
r
y
l-
s
ulf
o
n
a
mid
es
m
e
di
a
t
e
d b
y
h
y
p
erva
l
e
nt i
o
din
e
r
eage
nt
s
h
ave
b
ee
n d
eve
l
o
p
e
d a
s we
il
as
th
e
ir
a
ppli
cat
i
o
n
s
in t
o
t
a
l
sy
nth
es
i
s of
n
a
tur
a
l
pr
o
duct
s.
T
he
ox
idati
ve
ip
so
-r
ea
rran
ge
m
e
nt m
e
di
a
t
e
d b
y a
h
y
p
e
rv
a
l
e
nt i
o
din
e
r
eage
nt
e
n
a
bl
es ra
pid
ge
n
e
r
a
ti
o
n
of a f
un
c
ti
o
n
a
li
ze
d di
e
n
o
n
e sys
t
e
m
co
nt
a
inin
g a
qu
ate
rn
a
r
y ca
rb
o
n
ce
n
ter
co
nn
ec
t
e
d t
o seve
r
a
!
sp
2ce
n
te
r
s. T
h
e
pr
ocess occ
ur
s
th
ro
u
g
h
t
h
e
tr
a
n
sfe
r
of a
n
ary
l
g
r
o
up
fr
o
m
a s
il
y
l
seg
m
e
nt pr
ese
nt
o
n th
e
l
a
t
e
r
a
l
c
h
a
in.
As a
n illu
st
r
a
ti
o
n
of
th
e
p
o
t
e
n
t
i
a
l
of
thi
s
tr
a
n
sfo
rm
a
ti
o
n
, t
h
e
t
o
t
a
l
sy
n
t
h
es
i
s of Sce
l
e
t
e
n
o
n
e, a s
m
a
ll
Amary
ll
idaceae
a
lk
a
l
o
id
,
i
s
d
esc
rib
e
d
.
New
d
ea
r
o
m
a
ti
z
in
g
[
2+3
]
cyc
l
oa
dditi
o
n r
eac
ti
o
n
s of
ph
e
n
o
l
s
o
r
a
r
y
l-
s
ul
fo
n
a
mid
es
a
nd
b
e
n
ze
n
e o
r n
a
phth
a
l
e
n
e
d
er
i
va
ti
ves
h
ave
b
ee
n d
eve
l
o
p
e
d thr
o
u
g
h th
e
u
se
of a
h
y
p
erva
l
e
nt
i
o
din
e
r
eage
nt.
T
hi
s
p
rocess occ
ur
s v
i
a a
n intr
a
m
o
l
ec
ul
a
r nu
c
l
eo
phili
c a
dditi
o
n t
o
th
e
Wh
e
l
a
nd
s
p
ec
i
es ge
n
e
r
a
t
e
d durin
g
th
e ox
id
a
ti
ve ac
ti
va
ti
o
n
. S
ub
se
qu
e
nt
t
r
ea
tm
e
nt und
e
r
a
cidi
c
c
o
nditi
o
n
s
r
e
adil
y
tr
a
n
sfo
rm
s
th
e
tri
cyc
li
c sys
t
e
m int
o a
bi
a
r
y
l
v
i
a a fo
rm
a
i
c
r
oss
-co
uplin
g
p
rocess
.
A
dir
ec
t
c
r
oss
-
co
uplin
g
m
e
th
o
d
o
l
ogy
h
as a
l
so
b
ee
n d
eve
l
o
p
e
d u
s
in
g a
r
y
l-s
ul
fa
mid
es
.
F
in
a
ll
y, a co
n
c
i
se
fo
rm
a
i
sy
nth
es
i
s of S
tr
yc
hnin
e
h
as
b
ee
n
ac
hi
eve
d
fro
m
ava
il
a
bl
e 3-(
4-H
y
dr
oxy
ph
e
n
y
l)pr
o
pi
o
ni
c ac
id m
e
th
y
l
este
r in
9 s
t
e
p
s. T
h
e sy
nth
es
i
s
inv
o
l
ves a
n
ox
id
a
ti
ve
dear
o
m
a
ti
za
ti
o
n m
e
di
a
t
e
d b
y a
hyp
e
r
va
l
e
nt i
o
din
e
r
eage
nt
,
a
n
ove
l
aza
Mi
c
h
ae
l-
e
th
e
r
-e
n
o
l
ta
nd
e
m pro
cess, a
h
ec
k t
y
p
e cyc
li
za
ti
o
n
a
nd
a
r
e
du
c
ti
ve
i
so
m
er
i
zat
i
o
n
.
INTRODUCTION
O.
1. Iode hypervalent
La
synthèse
totale de produits n
a
turel
s
bioactif
s occ
upe une plac
e
important
e e
n
sc
i
e
n
ce,
aussi
bi
e
n p
o
ur le
s
applications
pharmaceutiqu
es
que pour l
e
développement
d
e
n
o
u
ve
ll
es
méthodologies qu
'
elle
inspire. Dan
s
un
contexte
d
'é
conomie
d
es
r
esso
urc
es e
t d
'é
cologie
,
il
est essentiel
de développer de nouvelles
synthèses
plu
s
rapides
e
t plu
s efficaces
tout
e
n
évitant
le
s
rejets toxique
s.
Du fait qu
'
il
s
permett
e
nt d
e
rempl
ace
r l
'
utili
sa
ti
o
n
de
m
é
t
a
u
x
lourds
,
chers et
toxique
s
tels que l
e
Thallium (III)
,
l
e
M
e
rcur
e
(Il)
o
u
e
nc
o
r
e
l
e
Plomb (IV)
,
les réactifs
à
ba
se
d
'
iode h
y
pervalentjouent un r
ô
l
e
imp
o
rtant
e
n
sy
nth
èse'-
3.Géneralement
mon
ova
lent
e
t de de
g
r
é
d
'
oxydation -1
,
1
'
iode pr
ése
nt
e
de
s
d
eg
r
és
d
'
oxydation
supérieurs (III,
V
,
et
VII)
co
nnus
sous
le nom d
'
iodes hypervalent
s
(Schéma
1).
AcO OAc
~OH
d10A<
0
Il8
'o
'o
0=1-0
8)
ô
IlNa
0
0
0
DMP(V)
IBX (V)
Na10
4(VIl)
H
3CÎ ( 0 ,
1
_..OÎ(CH
3F
3CÎ(0,
1
_..0Î(CF
3H0
,
1
_....
0Ts
060
l
ô
0
60
l
ô
6
DIB
(Ill)
PIFA (III)
Réactif d
e
Koser (Ill)
Schéma
1: Réactifs
à
base d'iode hypervalent
Parmi les plus
utilisés
,
l
es
réactifs
à
base d
'
iode
(V)
permettent notamment de
s
oxydations
d
'
alcools
en
aldéhydes
o
u
cétones
en
co
nditions douces.
O
n
retrouve parmi
ces composés
,
l
e
périodinane de Dess-Martin (DMP)
et
1
'acide 2-iodoxybenzoïque
(lB
X)
.
Le
périodate de
sod
ium
,
réactif à
b
ase
d'iode (VII)
permet quant
à
lui de réa
li
ser de
s
coupures oxydantes de
diois vicinaux.
Enfin,
les réactifs
à
base d'iode hypervalents
(III) réagissent avec
de nombreux
composés
dans des
réactions
d
'
oxydations et sont égaiements
utilisés dans des réactions de
fonctionnalisation de
carbony
l
e et de réarrangements. Parmi
l
es
plus
connus, on
peut citer
l
e
diacétoxyiodobenzène (DIB)
,
le PIF
A ou encore le réactif de
Koser (Schéma 1
)
.
Les composés à base d'iode
(III) sont caractér
i
sés
par une
structure
bipyramide trigonale,
où
le
groupement ary
l
et
l
es
deux paires d'électrons libres
sont en
positions
équatoriales
.
Les
deux
li
gands sont eux e
n
positions apica
l
es et partagent une
li
aison
hypervalente
avec
l'iode.
En
revanche,
ceux à base d'iode
(V) possédent 4
1
igands et 2
1
iens hypervalents orthogonaux
(Schéma 2).
(III)
Bipyramide trigonale
(V)