Intérêts de la chronobiologie dans le traitement des cancers
Texte intégral
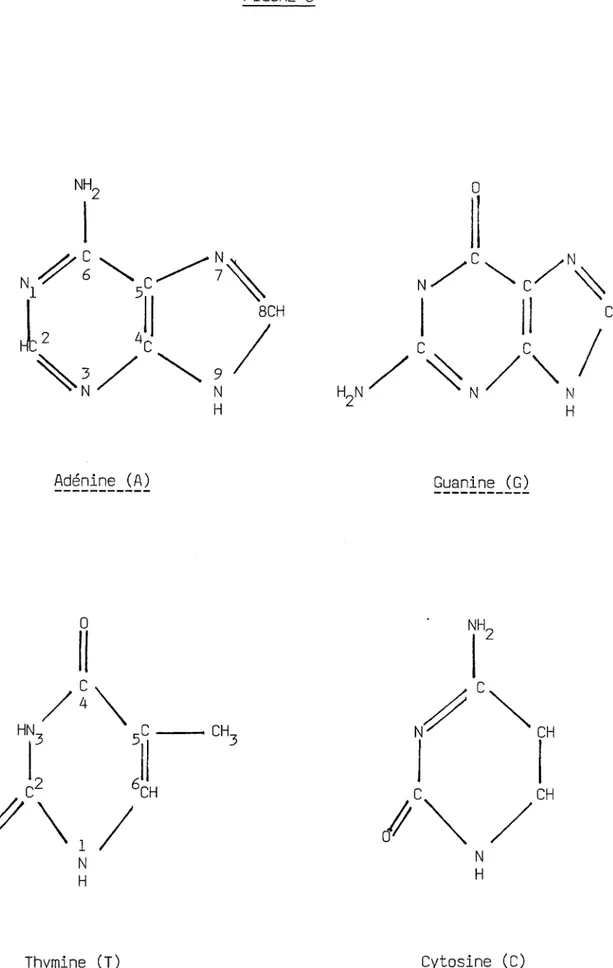
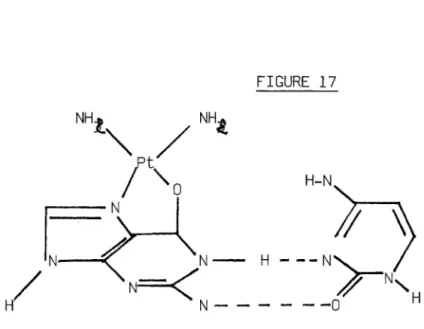
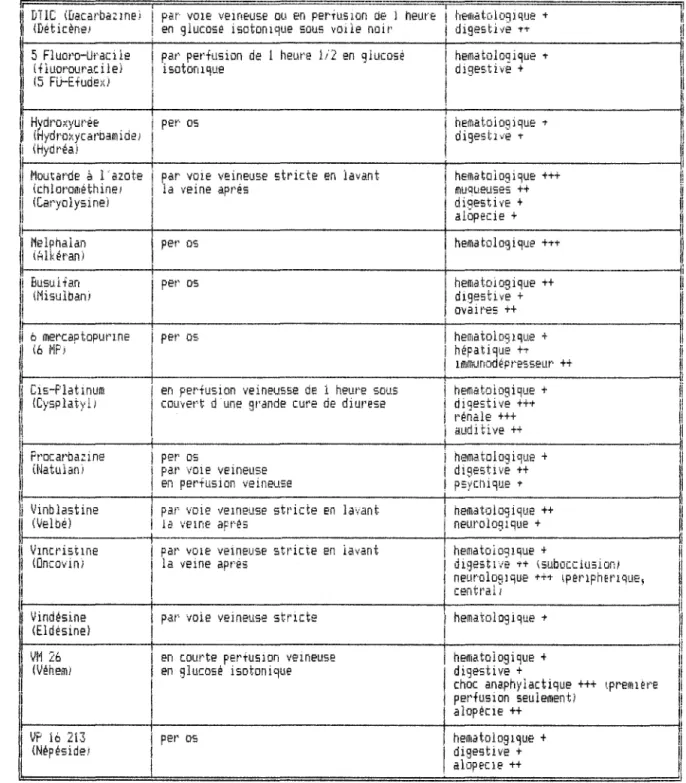
Figure

Documents relatifs
Ce poussin ne veut pas être en jaune comme tous les poussins, il veut être comme son ami Plioutche, plein de couleurs différentes en rayures. Il faut mettre toutes ces couleurs dans
Les conséquences du bris de l’alliance, par Israël Rappel des clauses de l’alliance (3 à 5). Un pays avec du lait et du miel en
Ayant débarqué des soutes à bagages cinq ou six caisses de marchandises, nous les avons vidées et disposées en cercle et, au fond de chacune d'elles, comme au
Je voudrais avoir le temps de redécouvrir avec bonheur le visage de tous ceux d'autrefois.. Ceux qui
Le soir même, vous racontez dans votre journal intime ce que vous avez découvert, les sentiments ressentis et ce que vous évoquent les secrets contenus dans cette malle...
Waldemar eut un sourire en voyant nos mines déconfites (3) et ses petites branches têtues qui restaient accrochées l’une à l’autre.. Non, nous ne
1- Ce premier triangle ABC a un angle obtus en A et l'angle en B est le double de l'angle en C. On construit le triangle isocèle de base OB avec le sommet D situé du même
Zig accompagne neuf randonneurs pour la traversée nocturne d'une vieille passerelle qui ne supporte pas plus de deux randonneurs à la fois.. Ils ne disposent que d'une seule lampe
