Université de Lille
Année Universitaire 2018/2019
Faculté de Pharmacie de Lille
THESE
POUR LE DIPLOME D'ETAT DE DOCTEUR EN PHARMACIE
Soutenue publiquement le 23.09.2019 Par M Floriant GOMES GONÇALVES
_____________________________ LE SYNDROME DES JAMBES SANS REPOS :
- PHYSIOPATHOLOGIE ET APPROCHES THÉRAPEUTIQUES
- ENQUÊTE OFFICINALE ET VIA INTERNET DE SA PRISE EN CHARGE DANS LES HAUTS-DE-FRANCE
_____________________________
Membres du jury :
Président : M. Thierry DINE, Professeur de Pharmacie clinique à la Faculté de Pharmacie de Lille, Praticien Hospitalier au GHLH
Directeur, conseiller de thèse : M. Kpakpaga Nicolas KAMBIA, Maître de Conférences en pharmacologie à la Faculté de Pharmacie de Lille
Université de Lille
Président : Jean-Christophe CAMART
Premier Vice-président : Damien CUNY
Vice-présidente Formation : Lynne FRANJIÉ
Vice-président Recherche : Lionel MONTAGNE
Vice-président Relations Internationales : François-Olivier SEYS
Directeur Général des Services : Pierre-Marie ROBERT
Directrice Générale des Services Adjointe : Marie-Dominique SAVINA
Faculté de Pharmacie
Doyen : Bertrand DÉCAUDIN
Vice-Doyen et Assesseur à la Recherche : Patricia MELNYK
Assesseur aux Relations Internationales : : Philippe CHAVATTE
Assesseur à la Vie de la Faculté et aux
Relations avec le Monde Professionnel : Thomas MORGENROTH
Assesseur à la Pédagogie : Benjamin BERTIN
Assesseur à la Scolarité : Christophe BOCHU
Responsable des Services : Cyrille PORTA
Faculté de Pharmacie de Lille
3, rue du Professeur Laguesse - B.P. 83 - 59006 LILLE CEDEX ( 03.20.96.40.40 - Ê : 03.20.96.43.64
Liste des Professeurs des Universités - Praticiens Hospitaliers
Civ. NOM Prénom Laboratoire
Mme ALLORGE Delphine Toxicologie
M. BROUSSEAU Thierry Biochimie
M. DÉCAUDIN Bertrand Pharmacie Galénique
M. DEPREUX Patrick ICPAL
M. DINE Thierry Pharmacie clinique
Mme DUPONT-PRADO Annabelle Hématologie
M. GRESSIER Bernard Pharmacologie
M. LUYCKX Michel Pharmacie clinique
M. ODOU Pascal Pharmacie Galénique
M. STAELS Bart Biologie Cellulaire
Liste des Professeurs des Universités
Civ. NOM Prénom Laboratoire
M. ALIOUAT El Moukhtar Parasitologie
Mme AZAROUAL Nathalie Physique
M. BERTHELOT Pascal Onco et Neurochimie
M. CAZIN Jean-Louis Pharmacologie – Pharmacie clinique
M. CHAVATTE Philippe ICPAL
M. COURTECUISSE Régis Sciences végétales et fongiques
M. CUNY Damien Sciences végétales et fongiques
Mme DELBAERE Stéphanie Physique
M. DEPREZ Benoît Lab. de Médicaments et Molécules
Mme DEPREZ Rebecca Lab. de Médicaments et Molécules
M. DUPONT Frédéric Sciences végétales et fongiques
M. DURIEZ Patrick Physiologie
M. GARÇON Guillaume Toxicologie
Mme GAYOT Anne Pharmacotechnie Industrielle
M. GOOSSENS Jean François Chimie Analytique
M. HENNEBELLE Thierry Pharmacognosie
M. LEMDANI Mohamed Biomathématiques
Mme LESTAVEL Sophie Biologie Cellulaire
M. LUC Gerald Physiologie
Mme MELNYK Patricia Onco et Neurochimie
M. MILLET Régis ICPAL
Mme MUHR – TAILLEUX Anne Biochimie
Mme PAUMELLE-LESTRELIN Réjane Biologie Cellulaire
Mme PERROY Anne Catherine Législation
Mme ROMOND Marie Bénédicte Bactériologie
Mme SAHPAZ Sevser Pharmacognosie
M. SERGHERAERT Eric Législation
Mme SIEPMANN Florence Pharmacotechnie Industrielle
M. SIEPMANN Juergen Pharmacotechnie Industrielle
M. WILLAND Nicolas Lab. de Médicaments et Molécules
Liste des Maîtres de Conférences - Praticiens Hospitaliers
Civ. NOM Prénom Laboratoire
Mme BALDUYCK Malika Biochimie
Mme GARAT Anne Toxicologie
Mme GOFFARD Anne Bactériologie
M. LANNOY Damien Pharmacie Galénique
Mme ODOU Marie Françoise Bactériologie
Liste des Maîtres de Conférences
Civ. NOM Prénom Laboratoire
Mme ALIOUAT Cécile Marie Parasitologie
M. ANTHERIEU Sébastien Toxicologie
Mme AUMERCIER Pierrette Biochimie
Mme BANTUBUNGI Kadiombo Biologie cellulaire
Mme BARTHELEMY Christine Pharmacie Galénique
Mme BEHRA Josette Bactériologie
M BELARBI Karim Pharmacologie
M. BERTHET Jérôme Physique
M. BERTIN Benjamin Immunologie
M. BLANCHEMAIN Nicolas Pharmacotechnie industrielle
M. BOCHU Christophe Physique
M. BORDAGE Simon Pharmacognosie
M. BOSC Damien Lab. de Médicaments et Molécules
M. BRIAND Olivier Biochimie
M. CARNOY Christophe Immunologie
Mme CARON Sandrine Biologie cellulaire
Mme CHABÉ Magali Parasitologie
Mme CHARTON Julie Lab. de Médicaments et Molécules
M CHEVALIER Dany Toxicologie
M. COCHELARD Dominique Biomathématiques
Mme DANEL Cécile Chimie Analytique
Mme DEMANCHE Christine Parasitologie
Mme DEMARQUILLY Catherine Biomathématiques
M. DHIFLI Wajdi Biomathématiques
Mme DUMONT Julie Biologie cellulaire
Mme DUTOUT-AGOURIDAS Laurence Onco et Neurochimie
M. EL BAKALI Jamal Onco et Neurochimie
Mme FLIPO Marion Lab. de Médicaments et Molécules
Mme FOULON Catherine Chimie Analytique
M. FURMAN Christophe ICPAL
Mme GENAY Stéphanie Pharmacie Galénique
M. GERVOIS Philippe Biochimie
Mme GOOSSENS Laurence ICPAL
Mme • GRAVE Béatrice Toxicologie
Mme GROSS Barbara Biochimie
M. HAMONIER Julien Biomathématiques
Mme HAMOUDI Chérifa Mounira Pharmacotechnie industrielle
Mme HANNOTHIAUX Marie-Hélène Toxicologie
Mme HELLEBOID Audrey Physiologie
M. HERMANN Emmanuel Immunologie
M. KAMBIA Kpakpaga Nicolas Pharmacologie
M. KARROUT Youness Pharmacotechnie Industrielle
Mme LALLOYER Fanny Biochimie
M. LEBEGUE Nicolas Onco et Neurochimie
Mme LECOEUR Marie Chimie Analytique
Mme LEHMANN Hélène Législation
Mme LELEU-CHAVAIN Natascha ICPAL
Mme LIPKA Emmanuelle Chimie Analytique
Mme MARTIN Françoise Physiologie
M. MOREAU Pierre Arthur Sciences végétales et fongiques
M. MORGENROTH Thomas Législation
Mme MUSCHERT Susanne Pharmacotechnie industrielle
Mme NIKASINOVIC Lydia Toxicologie
Mme PINÇON Claire Biomathématiques
M. PIVA Frank Biochimie
Mme PLATEL Anne Toxicologie
M. RAVAUX Pierre Biomathématiques
Mme RAVEZ Séverine Onco et Neurochimie
Mme RIVIERE Céline Pharmacognosie
Mme ROGER Nadine Immunologie
M. ROUMY Vincent Pharmacognosie
Mme SEBTI Yasmine Biochimie
Mme SINGER Elisabeth Bactériologie
Mme STANDAERT Annie Parasitologie
M. TAGZIRT Madjid Hématologie
M. VILLEMAGNE Baptiste Lab. de Médicaments et Molécules
M. WELTI Stéphane Sciences végétales et fongiques
M. YOUS Saïd Onco et Neurochimie
M. ZITOUNI Djamel Biomathématiques
Professeurs Certifiés
Civ. NOM Prénom Laboratoire
M. HUGES Dominique Anglais
Mlle FAUQUANT Soline Anglais
M. OSTYN Gaël Anglais
Professeur Associé - mi-temps
Civ. NOM Prénom Laboratoire
M. DAO PHAN Hai Pascal Lab. Médicaments et Molécules
Maîtres de Conférences ASSOCIES - mi-temps
Civ. NOM Prénom Laboratoire
M. BRICOTEAU Didier Biomathématiques
Mme CUCCHI Malgorzata Biomathématiques
M. FRIMAT Bruno Pharmacie Clinique
M. GILLOT François Droit et Economie pharmaceutique
M. MASCAUT Daniel Pharmacie Clinique
M. ZANETTI Sébastien Biomathématiques
M. BRICOTEAU Didier Biomathématiques
•
AHU
Civ. NOM Prénom Laboratoire
Mme DEMARET Julie Immunologie
Mme HENRY Héloïse Biopharmacie
Faculté de Pharmacie de Lille
3, rue du Professeur Laguesse - B.P. 83 - 59006 LILLE CEDEX Tel. : 03.20.96.40.40 - Télécopie : 03.20.96.43.64
http://pharmacie.univ-lille2.fr
L’Université n’entend donner aucune approbation aux opinions
émises dans les thèses ; celles-ci sont propres à leurs auteurs.
1
Remerciements
À mon Président de thèse, Monsieur Thierry DINE, de me faire l’honneur d’accepter la présidence de cette thèse. Cela a toujours été un réel plaisir de suivre vos enseignements durant mes études. Veuillez trouver ici l’expression de ma sincère reconnaissance.
À mon Directeur et conseiller de thèse, Monsieur Kpakpaga Nicolas KAMBIA, pour tout ce temps consacré à l’encadrement de mon travail. Merci d’avoir accepté de me suivre, merci pour vos nombreux conseils, votre rigueur et l’intérêt que vous avez porté à mon sujet. Veuillez trouver ici l’expression de ma sincère reconnaissance.
À Monsieur Christophe ENDERLE, merci de m’avoir encadré du premier au dernier stage dans votre officine, cela fût un honneur d’apprendre aux côtés d’un pharmacien titulaire aussi riche en connaissance et dévoué pour ses patients. Veuillez trouver ici mes remerciements les plus sincères.
À ma mère, sans qui rien n’aurait été possible. Merci d’avoir toujours cru en moi, depuis mes premiers pas jusqu’à ce jour. Je n’aurai jamais pu avoir une mère plus aimante et dévouée, j’espère pourvoir te rendre autant d’amour que tu ne m’en as apporté. Je t’aime.
À mon petit frère, l’homme que tu es devenu me remplit de fierté. Merci pour tous ces moments incroyables que nous avons vécus ensemble. Je serai toujours à tes côtés, je t’aime.
2
À ma grand-mère, tu as toujours cédé à mes nombreux caprices, merci pour tout l’amour que tu m’as apporté durant toutes ces années, merci pour ces merveilleux été en Bretagne avec pépère.
À Elodie, pour tout l’amour que tu me portes depuis plus de 7 ans maintenant. Nous voilà à présent dans notre maison, loin de notre première année de médecine, avec des projets plein la tête. Merci pour cette vie magnifique que l’on vit ensemble, je t’aime.
À mes beaux-parents et mes beaux-frères, pour tout l’amour que vous me portez. À mes cousins, pour tous ces moments passés ensemble et ce lien particulier qui ne cesse de nous unir.
À mes amis, collègues, pour votre présence.
3
Table des matières
Remerciements ... 1 Glossaire ... 6 Introduction ... 7 I. Le Syndromes des jambes sans repos ... 9 A. Histoire ... 9 B. Épidémiologie ... 11 1. Sexe ... 11 2. Age ... 13 3. Ethnie ... 13 4. Grossesse ... 15 5. Génétique ... 16 C. Mouvement périodique des jambes ... 16 D. Clinique et Diagnostic ... 17 1. Clinique ... 17 2. Critères de diagnostic ... 19 3. Échelle de sévérité ... 21 4. Diagnostic différentiel ... 26 E. Physiopathologie ... 27 1. La génétique ... 27 2. La dopamine ... 28 3. Le fer ... 34 4. Les opioïdes ... 35 F. Facteurs prédisposants/déclencheurs ... 36 1. Hygiène et mode de vie ... 36 2. Grossesse ... 37 3. Insuffisance rénale chronique ... 39 4. Population pédiatrique hyperactive ... 40 5. Patients atteints de la maladie de Parkinson ... 40 6. Médicaments ... 43
4 II. Approches thérapeutiques ... 44 A. Traitements non pharmacologiques ... 45 1. L’acupuncture ... 46 2. L’orthèse ... 47 3. La cryothérapie ... 48 4. La luminothérapie ... 48 5. Le « Relaxis pad » ... 49 B. Traitements pharmacologiques ... 51 1. Correction de la carence en fer ... 53 2. Les agents dopaminergiques ... 55 a. La L-Dopa ... 58 b. Les agonistes dopaminergiques ... 59 1) Ropinirole ... 59 2) Pramipexole ... 60 3) Rotigotine ... 61 3. Les anticonvulsivants ... 62 a. Gabapentine ... 63 b. Prégabaline ... 65 4. Comparaison entre les dopaminergiques et les anticonvulsivants ... 67 5. Les benzodiazépines ... 69 6. Opiacés ... 70 a. Oxycodone ... 71 b. Tramadol ... 73 c. Méthadone ... 76
III. Enquête officinale et via internet sur la prise en charge du syndrome des jambes sans repos ... 79 A. Objectifs ... 79 B. Matériel et méthode ... 79 1. Caractéristiques de l’étude ... 80 2. Population concernée ... 80 C. Résultats et discussion ... 80
5
1. Données démographiques et perception de la maladie, réponses aux questions de
l’enquête ... 80
2. Évaluation du score de sévérité selon l’échelle IRLS avant la mise en place d’un traitement ... 102
3. Évaluation du score de sévérité selon l’échelle IRLS après la mise en place d’un traitement ... 109 4. Comparaison des scores IRLS en fonction de différents paramètres ... 115 a. Scores IRLS en fonction de la tranche d’âge ... 115 b. Scores IRLS en fonction du sexe ... 115 c. Scores IRLS en fonction de la présence d’un historique familial ... 116 d. Scores IRLS en fonction de la molécule utilisée ... 116 D. Conclusion et perspectives ... 117 Annexe 1 : Questionnaire distribué aux patients ... 122 Bibliographie ... 130
6
Glossaire
AMM = Autorisation de mise sur le marché AVC = Accident vasculaire cérébrale
BPCO = Broncho-pneumopathie chronique obstructive CSST = Comité scientifique spécialisé temporaire EEG = Electroencéphalogramme
EMG = Electromyogramme EPO = Erythropoïétine
HAS = Haute autorité de santé HTA = Hypertension artérielle IRC = Insuffisance rénale chronique IRLS = International Restless Legs Scale
IRLSSG = International Restless Legs Syndrom Study Group IV = Intraveineux
MPJ = Mouvement périodique des jambes SJSR = Syndrome des jambes sans repos SMR = Service médical rendu
TDAH = Trouble déficitaire de l’attention avec hyperactivité TENS = Stimulateur électrique nerveux transcutanée
7
Introduction
Le Syndrome des Jambes sans repos (SJSR), connu également sous le nom d’impatiences musculaires ou plus récemment Maladie de Willis Ekbom, est un syndrome neurologique sensitivo-moteur, causant un large panel de symptômes ayant un impact direct sur la qualité de vie par ses perturbations causées lors des phases de sommeil ou d’immobilité, et touche de l’enfance jusqu’aux personnes âgées, à hauteur de 5 à 15% de la population mondiale. (1–3)
Les causes exactes sont encore méconnues ; ce qui fait que ce syndrome est souvent sous-diagnostiqué ou sur-diagnostiqué selon les médecins ; même si différentes pistes sont aujourd’hui fiables comme celle d’un déficit cérébral en fer ou encore une implication du système dopaminergique.
Le plus délicat dans cette maladie reste le diagnostic qui est basé sur des faits subjectifs et non établis par des marqueurs biologiques ou autres paramètres mesurables scientifiquement. D’autant plus que les symptômes sont également très difficiles à retranscrire aux médecins, et sont traduits selon les malades par des « brûlures, picotements, crampes, décharges électriques, vibrations, tensions etc. », autant de termes décrivant les symptômes de ce SJSR : paresthésies et dysesthésies des jambes le plus souvent, associées à des agitations motrices non volontaires.
Ces symptômes sont plutôt nocturnes que diurnes, et obligent les patients à bouger pour soulager leurs inconforts allant jusqu'à de fortes douleurs.
Nous verrons dans une première partie ; l’histoire du SJSR à travers diverses études épidémiologiques afin de voir quelles sont les personnes les plus susceptibles d’être
8
touchées, la façon de diagnostiquer les patients, et s’il y a des facteurs pouvant induire ou prédisposer à ce syndrome.
Puis dans une deuxième partie nous aborderons la prise en charge qui va de simples conseils hygiéno-diététiques jusqu’aux différents traitements médicamenteux.
Existe-t-il des médicaments spécifiques ou simplement symptomatiques ?
De même, quelles alternatives proposer aux patients pour éviter la prise de traitements pharmacologiques.
Enfin nous analyserons les résultats d’une enquête menée dans des pharmacies d’officines et diffusée sur internet, pour voir si les résultats obtenus convergent avec ceux des études scientifiques et pour essayer de répondre à diverses questions ; y a t-il vraiment une composante génétique ? Comment les patients se sentent-ils précisément et quel est l’impact réel sur leur vie quotidienne ? Une amélioration est-elle systématique lors de l’introduction d’une thérapeutique ?
9
I. Le Syndromes des jambes sans repos
A. Histoire
La première description provient du XVIIe siècle (1672 en latin, éditée en anglais en 1685) par le médecin anglais Sir Thomas Willis (1621-1675) qui décrivit ce syndrome comme « des sauts et contractures des tendons survenant la nuit, dans les bras et les jambes, causant une grande agitation et un sursaut des membres, ce qui cause au malade une insomnie, comme s’il était dans une place de torture ». (4)
Un siècle plus tard le médecin français, François Boissier de Sauvages de La Croix, décrit les mouvements anormaux en tant qu’impatiences des membres inférieurs qu’il dénomme « inquiétude des pieds ». (5)
C’est grâce à Karl-Axel Ekbom (1907-1977) que la description s’est précisée, notamment avec sa thèse en 1945 intitulée « Restless legs : a clinical study of a Hitherto Overlooked Disease in the legs characterized by peculiar paresthesia. » Y sont décrits les symptômes, comme le résume Bonduelle en 1952 : « paresthésies profondes localisées entre genou et cheville, symétriques, accompagnées d’agitations motrices invincibles des membres inférieurs, à rythme vespéral et nocturne et survenant dans le décubitus et la position assise ».
En 1943, F. Gerard Allison dans son écrit « obscure pains in the chest, back or limbs » nous offre également une description approchant au plus près des ressentiments de l’époque. Selon lui, le syndrome était une maladie mineure et commune dont il n’avait encore jamais vu de description, se produisant surtout la nuit et empêchant de dormir. Il note qu’il n’y a aucun rapport entre les sursauts brusques que l’on a en s’endormant. C’est une agitation inquiétante qui se manifeste dans
10
l’une ou les deux jambes, qui n’est pas une douleur mais quelque chose de distinct et de désagréable. (6)
Il n’y a pas d’irritation de la peau, c’est plutôt une combinaison, entre des mouvements volontaires et des secousses involontaires, qui empêchent le membre de trouver le repos. Selon lui les massages n’ont aucun effet, la seule façon de calmer ce désagrément est de se lever et de marcher.
Il pose l’hypothèse d’une cause vasculaire suite à l’observation qu’une amélioration était possible lors de la supplémentation en nitroglycérine.
Une autre théorie apparaît en 1953 selon Nils Brage Nordlander dans laquelle il associe le syndrome à une carence martiale, il pose cette hypothèse en voyant des patients anémiés guérir après avoir reçu une perfusion de fer. (7)
C’est enfin en 1982 que l’efficacité de la L-DOPA sur le syndrome est démontrée pour la première fois par S. Akpinar en Turquie pendant que d’autres classent ce syndrome dans les troubles périodiques du sommeil. (8)
Les agents dopaminergiques deviennent alors le traitement de référence de ce syndrome. (8,9)
Autrefois nommé syndrome des jambes sans repos, c’est en 2011 que la décision a été prise suite à un congrès à Québec de l’appeler la maladie de Willis-Ekbom (MWE). En effet, le terme de « jambes » sans repos n’était plus significatif puisque d’autres parties du corps, notamment les bras, peuvent être touchées.
Notons que le syndrome des jambes sans repos était méconnu au XIXe et XXe siècle du fait de son examen clinique trop banal, et de l’absence d’étiologie connue. De même à cette époque, ce syndrome était classé dans les « névroses » car les médecins ne connaissaient aucun remède et le qualifiaient donc d’incurable. Certains d’entre eux n’hésitaient pas à parler de manifestations hystériques. (10,11)
11
Cette absence d’informations était surtout causée par la difficulté des patients à exprimer leurs ressentiments. À cela s’ajoutaient des plaintes très variables selon les patients, rendant à l’époque très complexe la compréhension du syndrome.
B. Épidémiologie
Une étude française INSTANT portant sur 10 263 adultes français confirme une prévalence du SJSR de 8,5% et estime un âge moyen de la maladie de 48 ans. Les femmes sont plus touchées que les hommes : 10,8% de femmes touchées contre 5,8% d’hommes.
16,8% des patients présentent des symptômes sévères et 4,4% des symptômes très sévères.
Une histoire familiale est retrouvée dans 41% des cas.
Les enfants aussi semblent être touchés : 1,9% chez les 8-11ans ; 2% chez les 12-17ans. (2,12)
1. Sexe
Il apparaît que les femmes sont deux fois plus touchées : 9 à 14,2% chez les femmes contre 5,4 à 9,4% chez les hommes. (13)
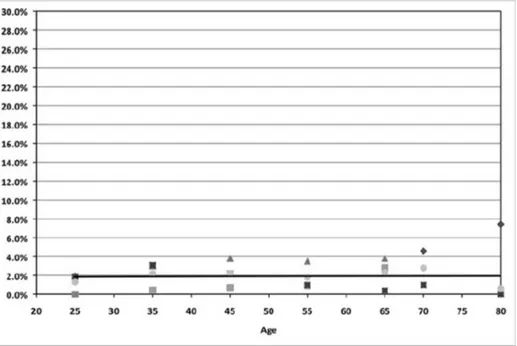
Les deux diagrammes ci-après résultent de douze études qui ont inclus d’abord 23 282 hommes puis 26 150 femmes, tous âgés de plus de 18 ans.
Ces études ont été conduites chez des adultes d’Amérique du Nord et d’Europe pour lesquels les critères de l’international restless legs syndrom study group (IRLSSG) sont utilisés. (Voir chapitre critère de diagnostic)
On peut voir un ratio de 2 pour les femmes avec une tendance de 9,5-10% contre 5% pour les hommes.
12
Figure 1 : Prévalence du syndrome des jambes sans repos chez les hommes nord-américains et européens (13)
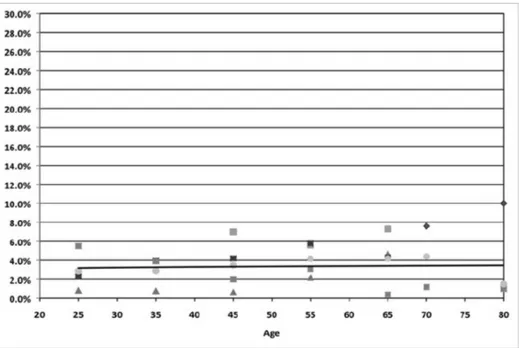
Figure 2 : Prévalence du syndrome des jambes sans repos chez les femmes nord-américaines et européennes (13)
13
NB : pour ces deux diagrammes ci-dessus, les différents points à chaque classe d’âge représentent les différentes études, donc 12 points par classe d’âge.
2. Age
Une étude montre que l’on peut retrouver ce syndrome dans 3 classes d’âges distinctes :
- Les moins de 45 ans pour lesquels on observe un pic du syndrome entre 20 et 40 ans avec une évolution plutôt lente de la maladie, et souvent d’origine familiale. - Les plus de 45 ans pour lesquels on observe une progression rapide de la maladie et souvent liée à des comorbidités comme un déficit en fer par exemple.
- Et la population pédiatrique : sur 10 000 familles américaines et anglaises, il y a des cas de maladie chez les 8-11ans représentants 1,9% de la population pédiatrique et 2% chez les 12-17 ans (14).
Il apparaît également que la prévalence du syndrome augmente avec l’âge et cela se confirme dans les pays américains et européens, mais pas dans les pays asiatiques où le taux de prévalence est très faible (13).
Ce syndrome peut apparaître à n’importe quel âge mais les études sur l’âge sont moins concluantes que celles sur le sexe par exemple, on sait néanmoins que la plupart des individus touchés ont plus de 40 ans (13).
3. Ethnie
En France, l’assurance maladie compte 8,5% de français atteints. (15)
Si nous regardons au-delà de notre pays, la plupart des études effectuées dans la population caucasienne donnent une prévalence de 5 à 15% de la population mondiale, mais les données sont encore trop faibles pour pouvoir évaluer la
14
prévalence ethnique car les études sont assez fragmentées, bien que nous sachions tout de même que les pays d’Asie ont un taux beaucoup plus faible que les autres régions du monde. (14)
Les deux diagrammes ci-après montrent la prévalence en fonction de l’âge dans la population asiatique en se basant sur les critères IRLSSG.
Le premier résulte de 5 études portant sur 8 081 hommes asiatiques majeurs, le deuxième de 6 études portant sur 11 253 femmes asiatiques majeures.
On observe que les populations asiatiques ont une prévalence très faible : inférieure à 4% tout sexe confondu. (13)
Figure 3 : Prévalence du syndrome des jambes sans repos chez les hommes asiatiques (13). Les 5 points différents correspondent aux 5 études différentes.
15
Figure 4 : Prévalence du syndrome des jambes sans repos chez les femmes asiatiques (13). Les 6 points différents correspondent aux 6 études différentes.
4. Grossesse
Le SJSR touche 19,5% des femmes enceintes, cette valeur augmente au fur et à mesure des trimestres de la grossesse avec une valeur de 15% de femmes touchées dès le 1er trimestre, jusque 23% au dernier.
Il se développe tout de même le plus souvent lors du dernier trimestre et disparaît naturellement 1 mois après l’accouchement. (13)
Une méta-analyse plus récente annonce un taux de 21% de femmes enceintes touchées avec des prévalences en fonction des 1er, 2e et 3e trimestre de grossesse respectivement de 8%, 16% et 22% (16,17).
16 5. Génétique
En ce qui concerne le caractère héréditaire, une étude récente a montré une histoire familiale chez 40 et 65% des individus atteints. (10)
Un ensemble d’études ont donné des valeurs plus précises allant de 28,3% de patients ayant une composante familiale en Suisse à 40,9% en France, et dans un même temps ont évalué le taux d’hérédité chez les jumeaux à hauteur de 83,3% (13).
Mais ces valeurs sont assez variables et les résultats des études épidémiologiques sont à prendre avec du recul car ils mélangent souvent des résultats d’enquêtes de SJSR primaires et secondaires, où l’inclusion n’est pas toujours bien détaillée.
C. Mouvement périodique des jambes
Environ 80% des patients qui souffrent du SJSR présentent des mouvements périodiques des jambes (MPJ) et cela crée une confusion pour le diagnostic du syndrome (2,18).
Les MPJ sont souvent non perçus par le patient et sont des mouvements anormaux, observables donc enregistrables et objectifs contrairement aux mouvements et symptômes du SJSR.
Certaines études montrent même par EEG (électroencéphalogramme) et EMG (électromyogramme) que les MPJ sont accompagnés d’une élévation de la pression systolique et d’une tachycardie puis d’une bradycardie qui pourraient être à terme un facteur de risque cardiovasculaire (2).
On estime qu’environ 6% de la population générale présentent des MPJ sans différences de sexes mais qui augmentent avec l’âge, et que 30% de ces patients sont atteints du SJSR (2).
17
Ce sont des mouvements répétés des membres inférieurs lors du sommeil, comme des extensions d’hallux ou des flexions de pied et/ou de genou.
Ces MPJ sont diagnostiqués par EMG et peuvent également toucher les membres supérieurs.
Chaque mouvement à une durée de 0,5 à 10 secondes et fait partie d’une série d’au moins 4 mouvements consécutifs séparés de 5 à 90 secondes.
Les MPJ sont plus nombreux en début de nuit lors de la phase de sommeil léger, et ne sont considérés comme significatifs qu’à partir de 15 MPJ/heure. Ils ne sont traités que s’ils sont sources d’inconfort et après avoir exclu tous facteurs déclencheurs (par exemple : apnée du sommeil) (2).
D. Clinique et Diagnostic
1. Clinique
La clinique est la seule source de diagnostic et cela fait toute la spécificité de ce syndrome : besoin impérieux de bouger les membres, accompagné ou non de sensations désagréables à savoir « électricité, démangeaison, tension, étau ».
Cela débute ou s’aggrave lors d’inactivité et s’améliore ou disparaît lors du mouvement.
Parmi les explications des patients nous pouvons donner deux manifestations spécifiques à savoir des paresthésies et dysesthésies des jambes, qui surviennent préférentiellement le soir au repos, et qui sont soulagées par le mouvement des jambes tel que la marche.
18
Les patients tentent de décrire leurs symptômes par les termes suivants : « sensation de brûlure, de picotements, d’aiguilles ou de fourmis dans les membres, de crampes intenses, et une obligation de bouger ».
Ils évoquent surtout le fait que ces douleurs dans les jambes ne les quittent jamais et que cela cause une source de fatigue plus ou moins intense selon la sévérité de la maladie pour le patient mais aussi à son/sa conjoint(e), ce qui explique la composante psychologique et socio-professionnelle.
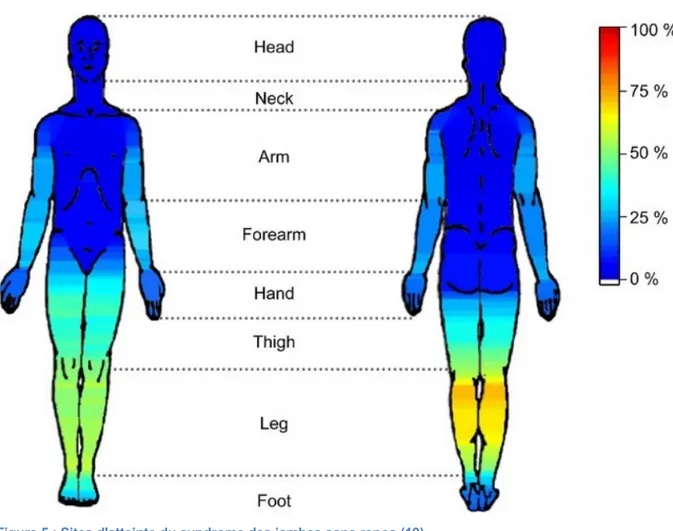
Même si la symptomatologie prédomine dans les jambes et de façon bilatérale, on retrouve des impatiences au niveau des membres supérieurs dans 50% des cas et une latéralisation de l’intensité dans 42% des cas. (19)
19
L’aspect vespéral de ce syndrome ajoute des difficultés d’endormissement, provoque des réveils nocturnes et des insomnies. Cela est problématique car la fatigue est un facteur d’augmentation de la sévérité du syndrome.
On peut classer deux formes cliniques selon l’âge de début des symptômes :
- Une forme à début précoce (avant 45 ans) qui est plutôt idiopathique et à forte composante familiale. Les symptômes sont souvent modérés, le rôle du fer y est jugé mineur.
- Une forme à début tardif (après 45 ans) d’évolution plus rapide et souvent en lien avec une forme secondaire du syndrome. Les symptômes sont généralement plus sévères (7).
2. Critères de diagnostic
Le diagnostic du SJSR est quelque chose de subjectif et ne répond pas à un test objectif ou à une valeur d’un marqueur biologique spécifique. Il se fait à partir d’un interrogatoire et il n’y a pas de nécessité d’explorations complémentaires.
Notons d’abord que chez l’enfant le diagnostic est très difficile car il y a des confusions avec les douleurs articulaires et/ou musculaires liées à la croissance, ou encore avec l’hyperactivité, mais dans tous les cas la clinique reste la même que chez l’adulte.
Un des obstacles à ce diagnostic est la confusion avec des MPJ nocturnes.
C’est pourquoi avant de poser le diagnostic il faut impérativement exclure toutes les causes qui induisent des symptômes semblables (qui crée des SJSR secondaires) comme les œdèmes des jambes, les crampes ou myalgies, les douleurs articulaires,
20
les polyneuropathies, l’arthrose, les stases veineuses ou autres désordres veinotoniques.
L’International Restless Legs Syndrome Study Group (IRLSSG) a défini en 2012 les 5 critères dits « obligatoires » ou « essentiels » qui doivent tous être remplis pour poser le diagnostic d’un SJSR :
« - Le besoin impérieux de bouger les jambes, souvent accompagné ou causé par des sensations inconfortables et désagréables dans les jambes.
- Le besoin impérieux de bouger, ou les sensations désagréables, débutent ou s’aggravent durant les périodes de repos ou d’inactivité.
- Le besoin impérieux de bouger, ou les sensations désagréables, sont soulagées partiellement ou totalement par le mouvement.
- Le besoin impérieux de bouger, ou les sensations désagréables, s’aggravent le soir ou la nuit, ou ne surviennent que le soir ou la nuit.
- Les symptômes ne sont pas uniquement attribuables à une autre condition telle que des crampes, inconfort positionnel ou arthrite. » (7,20)
À cela peut s’ajouter des critères supplémentaires tels que des antécédents familiaux, une réponse positive à un traitement par dopamine, un bilan clinique. (21)
Quand il y a une suspicion de forme secondaire, une résistance aux agonistes dopaminergiques (traitement de référence vu par la suite) ou un interrogatoire difficile (enfant, patient dément), on peut pratiquer plus d’examens tels que :
- Un bilan médicamenteux pour rechercher une cause iatrogène, - Un examen neurologique,
- Une NFS (numération formule sanguine), - La Ferritinémie, créatininémie, glycémie à jeun, - Un EMG, Doppler
21
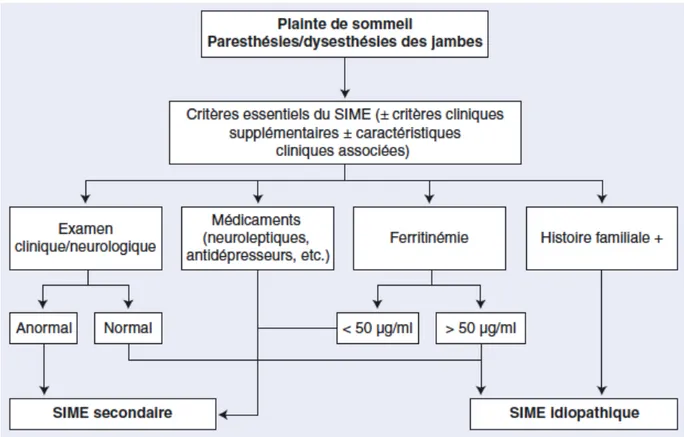
Figure 6 : Arbre décisionnel pour le diagnostic d'un syndrome des jambes sans repos (2)
3. Échelle de sévérité
L’échelle de mesure de la sévérité est définie par the « International Restless Legs Scale » (IRLS) comprenant 10 questions de 5 items chacun donnant un score de 0 à 4. (Tableau 1 ci-après) (22)
En additionnant chaque score, on obtient un score total sur 40 points donnant une indication sur la sévérité du syndrome. Plus le score est élevé, plus le syndrome est qualifié de sévère (14) :
- Score de 1 à 10 : faible - Score de 11 à 20 : modéré - Score de 21 à 30 : sévère - Score de 31 à 40 : très sévère
22
L’évaluation de la sévérité est très importante pour déterminer s’il y a besoin de mettre en place un traitement pharmacologique et pour savoir quelle classe thérapeutique mettre en route.
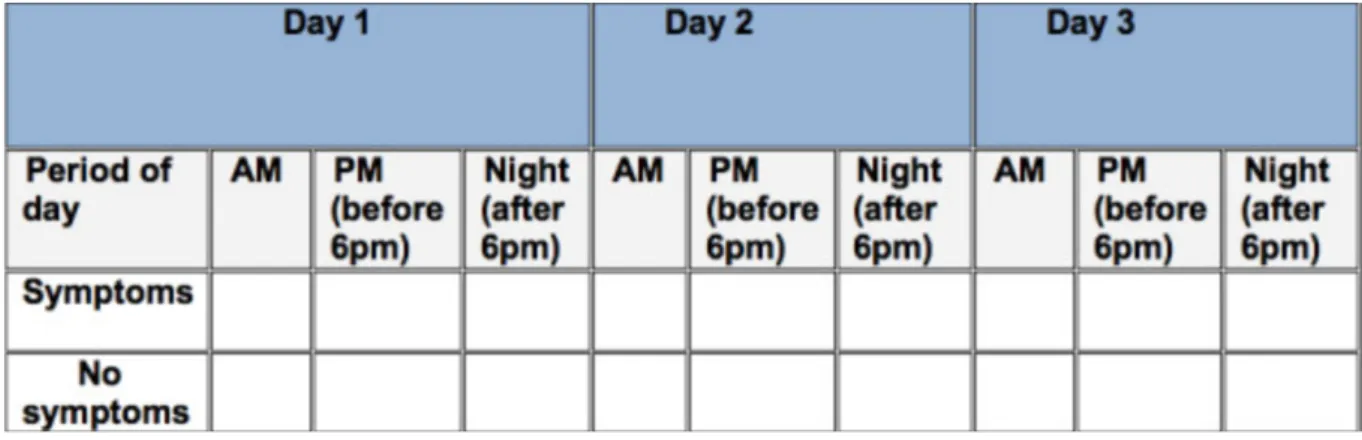
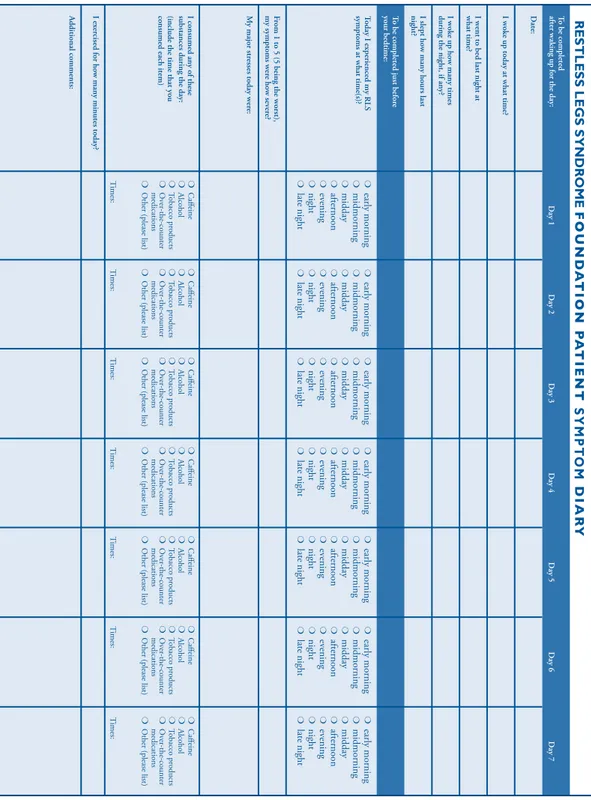
Des fondations et institutions ont également créé ce qu’on peut nommer des aides aux suivis, qui ressemblent aux carnets de suivi de la glycémie, de l’INR ou de la tension artérielle, mais adaptées au SJSR. (Tableaux 2, 3 et 4 ci-après)
Le patient note jour après jour le ressenti de ses symptômes sur la journée s’il en a, à quel moment et à quelle intensité, s’il a pris des produits susceptibles d’aggraver ses douleurs tels quel l’alcool, la caféine ou des médicaments divers.
Le patient pourra le montrer à son médecin (neurologue, généraliste) lors de ses consultations, ce qui permettra à ce dernier d’avoir une vue plus détaillée sur les journées du patient et pourra au mieux adapter ses conseils d’hygiène de vie, de diététique et le traitement.
23
Tableau 2 : Échelle de sévérité du syndrome des jambes sans repos (23)
In the past week…In the past week…
(1) Overall, how would you rate the RLS discomfort in your legs or arms?(6) How severe was your RLS as a whole?_ (4) Very severe_ (3) Severe_ (4) Very severe _ (3) Severe _ (2) Moderate_ (2) Moderate _ (1) Mild_ (1) Mild _ (0) None _ (0) None
In the past week…In the past week…
(2) Overall, how would you rate the need to move around because of your RLS symptoms? (7) How often did you get RLS symptoms? _ (4) Very severe_ (4) Very often (6 to 7 days in 1 week) _ (3) Severe_ (3) Often (4 to 5 days in 1 week) _ (2) Moderate_ (2) Sometimes (2 to 3 days in 1 week) _ (1) Mild_ (1) Occasionally (1 day in 1 week) _ (0) None_ (0) Never
In the past week…In the past week…
(3) Overall, how much relief of your RLS arm or leg discomfort did you get from moving around?_ (4) No relief _ (3) Mild relief _ (2) Moderate relief (8) When you had RLS symptoms, how severe were they on average? _ (4) Very severe (8 hours or more per 24 hour)_ (3) Severe (3 to 8 hours per 24 hour)_ (2) Moderate (1 to 3 hours per 24 hour) _ (1) Either complete or almost complete relief _ (1) Mild (less than 1 hour per 24 hour) _ (0) No RLS symptoms to be relieved _ (0) None
In the past week…In the past week…
(4) How severe was your sleep disturbance due to your RLS symptoms?(9) Overall, how severe was the impact of your RLS symptoms on your ability to carry out your daily affairs, for example carrying out a satisfactory family, home, social, school or work life? _ (4) Very severe_ (4) Very severe _ (3) Severe_ (3) Severe _ (2) Moderate_ (2) Moderate _ (1) Mild_ (1) Mild _ (0) None_ (0) None
In the past week…In the past week…
(5) How severe was your tiredness or sleepiness during the day due to your RLS symptoms? (10) How severe was your mood disturbance due to your RLS symptoms - for example _ (4) Very severe_ (3) Severe_ (2) Moderateangry, depressed, sad, anxious or irritable?_ (4) Very severe_ (3) Severe_ (2) Moderate _ (1) Mild_ (1) Mild _ (0) None _ (0) None 1. Answers for this IRLS are scored from 4 for the first (top) answer (usually ‘very severe’) to 0 for the last answer (usually none). All items are scored. The sum of the item scores serves as the scale score. The International Restless Legs Syndrome Study Group holds the copyright for this scale.
Sum of scores = Restless Legs Syndrome Rating Scale
Have the patient rate his/her symptoms for the following ten questions. The patient and not the examiner should make the ratings, but the examiner should be available to clarify any misunderstandings the patient may have about the questions. The examiner should mark the patient's answers on the form.
24
Tableau 3 : Questionnaire d’évaluation et de suivi des symptômes du syndrome des jambes sans repos (25)
25
Tableau 4 : Guide d'évaluation de la sévérité du syndrome des jambes sans repos (25)
ear ly m orn in g m id m orn in g m id da y aft ern oo n eve nin g nig ht late n igh t ear ly m orn in g m id m orn in g m id da y aft ern oo n eve nin g nig ht late n igh t ear ly m orn in g m id m orn in g m id da y aft ern oo n eve nin g nig ht late n igh t ear ly m orn in g m id m orn in g m id da y aft ern oo n eve nin g nig ht late n igh t ear ly m orn in g m id m orn in g m id da y aft ern oo n eve nin g nig ht late n igh t ear ly m orn in g m id m orn in g m id da y aft ern oo n eve nin g nig ht late n igh t ear ly m orn in g m id m orn in g m id da y aft ern oo n eve nin g nig ht late n igh t C aff ein e Alc oh ol To ba cco pr od uc ts O ver -th e-c ou nte r m ed ica tio ns O th er ( ple ase lis t) Tim es: C aff ein e Alc oh ol To ba cco pr od uc ts O ver -th e-c ou nte r m ed ica tio ns O th er ( ple ase lis t) Tim es: C aff ein e Alc oh ol To ba cco pr od uc ts O ver -th e-c ou nte r m ed ica tio ns O th er ( ple ase lis t) Tim es: C aff ein e Alc oh ol To ba cco pr od uc ts O ver -th e-c ou nte r m ed ica tio ns O th er ( ple ase lis t) Tim es: C aff ein e Alc oh ol To ba cco pr od uc ts O ver -th e-c ou nte r m ed ica tio ns O th er ( ple ase lis t) Tim es: C aff ein e Alc oh ol To ba cco pr od uc ts O ver -th e-c ou nte r m ed ica tio ns O th er ( ple ase lis t) Tim es: C aff ein e Alc oh ol To ba cco pr od uc ts O ver -th e-c ou nte r m ed ica tio ns O th er ( ple ase lis t) Tim es: To b e c om ple ted aft er w ak in g u p f or th e d ay : D ate : I w ok e u p t od ay at w ha t t im e? I w en t t o b ed la st n ig ht at w ha t t im e? I w ok e u p h ow m an y t im es du rin g t he n ig ht, if an y? I s lep t h ow m an y h ou rs las t nig ht? To b e c om ple ted ju st b efo re yo ur b ed tim e: To da y I ex pe rie nc ed m y R LS sy m pto m s a t w ha t t im e(s )? Fr om 1 to 5 (5 b ein g t he w or st) , m y s ym pto m s w ere h ow se ve re? I c on su m ed an y o f t he se su bs tan ce s d ur in g t he d ay : (in clu de th e t im e t ha t y ou co ns um ed ea ch ite m ) I e xe rci sed fo r h ow m an y m in ute s t od ay ? A dd itio na l c om m en ts: M y m ajo r s tre sse s t od ay w ere : D ay 1 D ay 2 D ay 3 D ay 4 D ay 5 D ay 6 D ay 7
26 4. Diagnostic différentiel
Il faut savoir distinguer le SJSR avec des dysesthésies et paresthésies causées par d’autres pathologies comme une polyneuropathie, des douleurs articulaires ou musculaires, une artérite, une insuffisance veineuse, des crampes nocturnes, un inconfort positionnel, un syndrome des jambes douloureuses et de mouvements des orteils (painful legs and moving toes), de l’anxiété etc. (26)
Parmi les éléments qui permettent de différencier et d’isoler un SJSR, nous pouvons noter le caractère circadien des symptômes sensori-moteurs du syndrome qui prédomine le soir et la nuit ainsi que le soulagement des douleurs par le mouvement, ce qui constitue une grande différence avec des douleurs vasculaires ou articulaires par exemple (3,13).
Ainsi, nous pouvons principalement distinguer :
- Les neuropathies périphériques qui n’ont pas d’aspect circadien et ne montrent pas d’amélioration de la symptomatologie par le mouvement.
- Les akathisies qui n’ont pas d’aspect circadien, ne se manifestent pas sous forme d’impatience, ne cèdent pas à l’activité physique, et sont souvent liées à la prise de neuroleptiques.
- Les problèmes vasculaires : tels que les artérites oblitérantes des membres inférieurs (AOMI) ou varices par exemple, les symptômes augmentent avec l’activité physique et s’atténuent au repos.
- Les crampes nocturnes qui sont unilatérales, focalisées, apparaissent de manière soudaine et sont soulagées par une extension des muscles concernés.
27
- Un syndrome des jambes douloureuses et de mouvements des orteils où il y a une indifférence à la mobilité sans prédominance vespérale.
E. Physiopathologie
1. La génétique
Le SJSR idiopathique est retrouvé dans 28,3% des cas selon une étude espagnole, 40,9% selon une étude française et jusque 77,1% selon une étude canadienne. (3) Le caractère héréditaire suit un mode de transmission autosomique dominant, et les formes familiales sont plus précoces que les formes sporadiques (27).
Une première étude franco-canadienne a mis en évidence un locus sur le chromosome 12q (RLS1) ayant une transmission autosomique récessive.
D’autres études européennes et nord-américaines se sont basées sur un modèle de transmission dominant et ont mis en évidence des loci localisés sur 14q (RLS2), 9p (RLS3) ainsi que 2q et 20p (RLS4 et 5). (27,28)
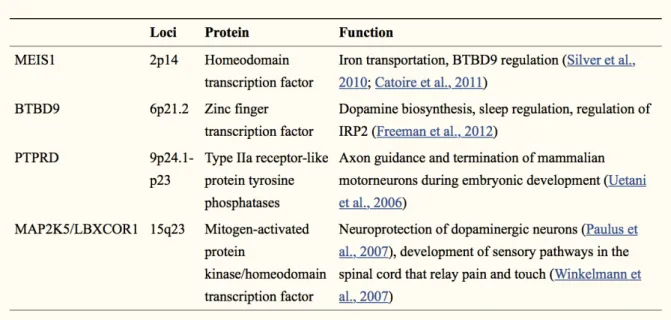
Si l’on regarde les gènes de plus près, ces études montrent qu’il existe 5 régions génomiques qui ont un risque de porter un allèle facteur de risque du syndrome : MEIS1, BTBD9, PTPRD, MAP2k/SKOR1 et TOX3/BC034767 ainsi qu’une région inter génique sur le chromosome 2. (27,28)
La plupart de ces variations ont un lien avec le SJSR et les MPJ et surtout un allèle à risque du SJSR sur le BTBD9, qui est particulièrement associé à une augmentation des mouvements périodiques involontaires et à un déficit périphérique en fer. (27,28)
28
Tableau 5 : Liste des principaux polymorphismes génétiques associés au syndrome des jambes sans repos (3)
2. La dopamine
Un large panel d’études pharmacologiques met en évidence le rôle de la dopamine dans ce syndrome, en effet on observe un dysfonctionnement du système dopaminergique chez les patients atteints du syndrome, une amélioration des symptômes chez ceux qui reçoivent une dose (même faible) d’agent dopaminergique, ainsi qu’une aggravation des symptômes chez ceux qui reçoivent des antagonistes dopaminergiques ; malheureusement à ce jour rien n’est clair à ce sujet.
Cependant, on sait que le fer est impliqué dans ce système car il est co-facteur de l’enzyme tyrosine hydroxylase qui métabolise la levodopa en dopamine.
29
Une autre théorie implique le système sympathique qui est stimulé de façon plus importante chez les patients atteints du SJSR. Ainsi, la vasoconstriction entraîne une hypoxie périphérique qui induit des douleurs et la nécessité de bouger pour mieux oxygéner les tissus.
L’ajout de dopamine joue un rôle de vasodilatation et améliore donc les symptômes. A ce jour, les études sont malheureusement divergentes mais montrent dans l’ensemble des choses communes, à savoir l’implication d’un transporteur de dopamine, un déficit en récepteur D2 striatal (par tomographie par émission de positons TEP), une perte neuronale ou encore une lésion anatomique. (27)
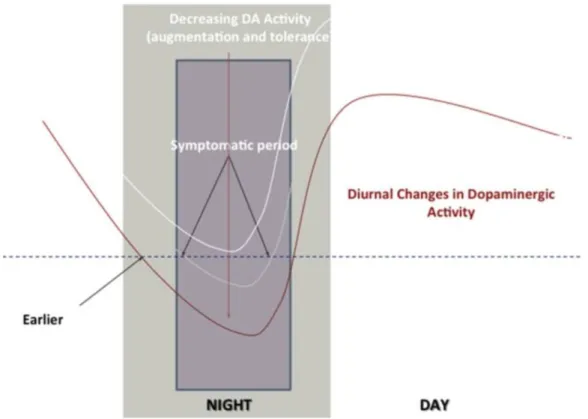
S’il on observe l’aspect circadien de l’activité dopaminergique, on voit clairement qu’il y a une diminution le soir et la nuit et une augmentation le matin, cela expliquerait l’arrivée des symptômes en début de soirée. (Figure 7 ci-après)
Même si une petite dose de dopamine permet de corriger cette baisse de dopamine en soirée, cela s’avère plus complexe.
Une stimulation par la dopamine va activer un rétrocontrôle ou down-régulation qui va induire une baisse des récepteurs dopaminergiques, ce qui va reproduire les effets de la pathologie présente ou en aggraver les symptômes.
L’ajustement du traitement entraîne donc la nécessité d’augmenter encore la stimulation de dopamine et donc d’ajouter des doses plus élevées.
Ce phénomène appelé l’augmentation, est dans le cas du SJSR semblable au phénomène de tolérance. En effet l’augmentation progressive des doses va conduire à une aggravation progressive de la pathologie. (27)
Il est alors préconisé de traiter par un agoniste dopaminergique à faible dose en utilisant une forme à libération prolongée (limitant l’effet de pic).
30
Figure 7 : Phénomène d’augmentation en fonction du rythme circadien de la dopamine (27)
Sur le schéma ci-dessus nous pouvons observer le phénomène d’augmentation : - La ligne pointillée indique le niveau critique du signal post-synaptique de la dopamine, en dessous duquel les symptômes apparaissent.
- La ligne blanche (claire) correspond au SJSR avant traitement avec des symptômes la nuit.
- La ligne blanche (foncée) correspond au traitement avec succès, il n’y a alors pas de symptômes.
- La ligne rouge représente l’ajustement du traitement afin de répondre au phénomène d’augmentation, c’est à dire que l’on a augmenté la dose afin de pouvoir combattre ce phénomène et donc d’éviter que les symptômes ne réapparaissent. Le principal problème est que les symptômes deviennent alors plus précoces, durables (potentiellement sur la journée) et sévères. (27)
31
Dans une étude pour laquelle nous rappelons que la concentration plasmatique normale de dopamine est de l’ordre de 15-30pg/ml, nous étudierons les récepteurs dopaminergiques D2 sur les cellules immunitaires lymphocytaires et monocytaires (WBC= White Blood Cells) afin de savoir si ces derniers peuvent être mis en cause dans la maladie ou non.
L’étude s’intéresse à 3 groupes : - Un groupe de patients non traités - Un groupe de patients traités - Un groupe témoin
32
Le résultat est que le taux d’expression en récepteurs dopaminergiques dans les cellules immunitaires des 3 groupes est différent. En effet, on observe sur la figure 8 ci-après des taux d’expressions de récepteurs significativement plus bas chez les patients traités ou non traités que dans le groupe témoin et cela pour les lymphocytes tout comme les monocytes.
Figure 8 : Pourcentage d'expression de récepteurs dopaminergiques en fonction des groupes tests sur les cellules lymphocytaires (A) et monocytaires (C) (29)
33
Étudions à présent la régulation positive des récepteurs dopaminergiques en fonction des taux en dopamine :
Sur la figure 9 ci-dessous nous pouvons suivre le pourcentage d’expression des récepteurs en dopamine dans les lymphocytes et monocytes en fonction des variations en concentration de dopamine.
On peut voir que l’expression des récepteurs est insensible aux variations de la concentration en dopamine pour des taux de 0,001 ; 0,01 et 0,1 μM et ce pour les deux types de cellules alors qu’elle est sensible pour des valeurs supérieures à 0,1 et jusque 10μM sur les lymphocytes uniquement.
Figure 9 : Pourcentage d'expression de récepteurs en dopamine en fonction des variations de concentrations en dopamine sur les cellules lymphocytaires et monocytaires. (29)
Conclusions de cette étude :
On peut affirmer qu’il y a bien chez les personnes atteintes du SJSR une baisse des récepteurs dopaminergiques et que ces derniers peuvent également rester insensibles aux traitements dopaminergiques.
On pourrait alors se servir de ces récepteurs comme des bio-marqueurs du SJSR. (30)
34 3. Le fer
Le SJSR est défini depuis les études de Ekbom et Nordlander par un déficit périphérique en fer (vu dans la partie historique), qui lorsqu’il augmente, accroît également la sévérité du syndrome, toute condition qui provoque un déficit en fer peut alors induire un SJSR comme par exemple la grossesse ou encore une insuffisance rénale.
Cela a été prouvé par le fait qu’un ajout massif de fer dans l’organisme améliorait considérablement les symptômes, mais on s’aperçut ensuite pour beaucoup de patients, un taux normal de ferritine était retrouvé (14,27,31).
La physiopathologie apparaît donc moins périphérique mais plutôt située dans le système nerveux central.
Des études ont montré en effet que chez des patients atteints du SJSR, le taux de fer périphérique était normal, alors que le taux de ferritine cérébrospinal était plus bas que la normale. (32)
Grâce à l’IRM on peut effectivement voir une réduction du fer cérébral, plus précisément dans la substance noire, le putamen, le noyau caudé et des études plus récentes avec une meilleure sensibilité ont même montré une baisse de fer dans le thalamus. (32)
Donc le déficit en fer touche aussi bien des régions riches en fer comme la substance noire que pauvre en fer comme le thalamus.
Les conséquences de ce déficit en fer sont à la fois l’hypoxie et la perte de myéline. En effet, le fer est impliqué dans le mécanisme de transport de l’oxygène, sa carence entraîne donc une hypoxie, retrouvée surtout dans les membres inférieurs.
Puisque la synthèse de myéline est fer-dépendante, cela engendre donc un déficit en myéline et donc une moins bonne transmission de l’influx nerveux. De plus, on sait grâce à des études sur les animaux qu’un déficit en fer au niveau
35
cérébral implique une baisse de myéline mais aussi de protéines, lipides et de cholestérols tous importants pour la création et le maintien de la structure des cellules et du transport des informations. (27)
La concentration sanguine en fer suit également un rythme circadien avec une baisse en fin de journée de 50 à 60%. Le moment où la concentration en fer est la plus basse correspond bien avec le moment où les symptômes sont le plus élevés. (32)
Il y a plus de 50 ans, Ekbom notait déjà une prévalence du SJSR de 24% chez les patients anémiques et exprimait alors que tout évènement conduisant à une baisse en fer systémique (multiples dons du sang, ménorragie, gastrectomie) pouvait majorer un risque de SJSR ou en exacerber les symptômes. (2)
4. Les opioïdes
Une fois encore rien n’est certain concernant l’hypothèse de l’implication du système opioïdique dans le SJSR mais on sait que les opioïdes sont un traitement efficace du SJSR et que l’ajout de la naloxone (inhibiteur des récepteurs aux opiacés) induit l’apparition des symptômes.
Il y a probablement une altération du traitement central de la douleur qui implique le système opioïde endogène. Des études ont montré que les régions cérébrales impliquées dans la gravité des symptômes du SJSR sont similaires à celles impliquées dans la douleur chronique, elles ont montré par PET à la diprénorphine (radio-ligand des récepteurs opiacés) que plus le SJSR est sévère, plus il y a libération d’opioïdes endogènes (33,34).
36
F. Facteurs prédisposants/déclencheurs
1. Hygiène et mode de vie
Plusieurs causes sont souvent retrouvées dans les descriptions d’habitudes de vie des patients. Beaucoup d’entre eux recensent une intensité plus élevée des symptômes dans la soirée ou encore une crise qui dure plus longtemps la nuit selon qu’ils ont consommé ou non des substances potentiellement aggravantes à savoir la caféine, la nicotine ou l’alcool.
Ils se plaignent également d’une augmentation des douleurs lorsqu’ils ont mangé un repas trop copieux et gras le soir.
Une étude a donc cherché à savoir si ces facteurs étaient bien déclencheurs ou aggravants d’un SJSR. Un facteur supplémentaire a été étudié dans cette étude, le don du sang (qui peut causer évidemment une baisse du taux de fer).
Sur 973 participants (262 atteints d’un SJSR et 711 sujets sains), il n’y a que le facteur « don du sang » qui s’est révélé significatif et cela augmente avec le nombre de don.
Il n’y a pas eu de rapport évident entre le syndrome et le tabac, ni l’alcool. (35)
Concernant la diététique, voyons de plus près si le poids peut-être un facteur de risque ou non grâce à une méta-analyse qui recense un total de 197 204 participants. (36)
On y démontre une association positive entre obésité et SJSR avec un odds ratio de 1.44.
De même, les personnes en surpoids sont à risque aussi avec un odds ratio de 1.29. On note un risque plus important chez les femmes obèses que chez les hommes obèses (odds ratio 1.42 VS 1.19) (36).
37
Pour aller plus loin on s’est aussi intéressé à la population vivant en altitude suite à des hypothèses de relation entre cette condition et le syndrome, grâce à une étude menée sur une population indienne (région Himalayenne) de 1 689 personnes réparties entre 3 seuils d’altitudes différents : 400m ; 1900-2000m ; 3200m.
Les sujets sont âgés de 18 à 84 ans avec un âge moyen de 35.2 ans, et 55,2% des participants sont des femmes.
Le diagnostic de SJSR est posé selon les critères IRLSSG en mesurant la saturation en oxygène grâce à un oxymètre de pouls.
On observe un SJSR chez 9,4% des habitants avec une prévalence plus forte chez les femmes : 13,6% VS 4,1% chez les hommes.
On note surtout une prévalence plus élevée (5 fois plus) en haute altitude : 12,2% et 11,8% à 2000m et 3200m VS 2,5% à 400m. (37)
Donc la baisse d’oxygène se montre alors comme facteur de risque pour ce syndrome.
2. Grossesse
La principale cause de dyskinésie durant la grossesse est attribuée au SJSR, et on estime entre 11 à 27% le nombre de femmes enceintes qui ont des symptômes attribuables au syndrome selon une étude américaine, surtout au dernier trimestre. Ces troubles s’estompent après l’accouchement dans la majeure partie des cas. (32)
Durant la grossesse, l’incidence d’un déficit en fer augmente de façon significative. L’étiologie du SJSR durant la grossesse est corrélée avec une insuffisance en folates et en fer. En effet, les besoins en nutriments augmentent de façon significative : une augmentation de 3 à 4 fois sa valeur pour les besoins en fer et de 8 à 10 fois sa valeur pour ceux en folates. La figure 10 ci-après nous montre bien qu’un taux faible en folates est retrouvé chez les femmes atteintes alors que ce taux est plus haut chez les femmes non atteintes.
38
Figure 10 : Évolution de la concentration en folates dans le sérum de femmes enceintes atteintes et non atteintes du syndrome des jambes sans repos, de la préconception jusqu'à 1 mois après accouchement. (32)
Cette hypothèse se confirme par une autre étude qui compare les femmes enceintes qui ont un SJSR et supplémentées en folates contre des femmes enceintes qui ont un SJSR non supplémentées en folates. On observe alors une prévalence du SJSR de 9% chez les femmes supplémentées VS 80% chez les non supplémentées. (38)
Une autre étude menée sur 500 femmes à deux stades de leur grossesse (33-34e semaine de gestation et 4e semaine après l’accouchement) montre que la prévalence du SJSR est de 19,5% à la 33-34e semaine de gestation contre 0,6% 4 semaines après l’accouchement. (13)
Cela montre bien que ce syndrome (déclaré lors de la grossesse) disparaît dans la plupart des cas après l’accouchement.
39
On a également cherché à savoir si le syndrome gestationnel est un facteur de risque d’un SJSR chronique. Pour cela, une étude conduite auprès de 207 femmes ayant accouché 6,5 ans auparavant, montre que celles qui ont développé un SJSR gestationnel durant la grossesse avaient 4 fois plus de risque de développer un SJSR par la suite par rapport aux femmes n’ayant pas eu de SJSR gestationnel. Ces femmes ont également beaucoup plus de risque de développer un nouveau SJSR lors d’une prochaine grossesse : 58% VS 3% (13,16).
3. Insuffisance rénale chronique
On observe que chez les patients en phase terminale de la maladie rénale, 62% d’entre eux se plaignent de SJSR, le risque de développer ce syndrome diminue après une transplantation de rein. On ne note cependant pas de lien entre le taux d’urée et ce syndrome. L’apparition du SJSR dépend plutôt de la durée et du nombre de dialyse. (32)
L’évidence d’une relation entre l’insuffisance rénale et le SJSR est due au déficit en fer par le fait que le rein fonctionne moins bien et produit moins d’érythropoïétine (EPO) ce qui engendre une anémie.
Des traitements par EPO permettent une baisse des MPJ et une amélioration de la qualité du sommeil chez les patients atteints. (32)
Une étude réalisée sur 237 patients dialysés de façon chronique (âge moyen 59,8 ans ; durée moyenne de début des dialyses 5,4 ans), montre la présence du SJSR (selon les critères IRLSSG) à hauteur de 18,6%. (38)
40 4. Population pédiatrique hyperactive
Les enfants qui présentent des déficits de l’attention avec hyperactivité présentent un risque plus élevé de SJSR que les enfants non affectés.
Une étude réalisée auprès de 886 enfants âgés de 2 à 14 ans montre que les symptômes de la maladie sont plus élevés chez les enfants hyperactifs par rapport aux autres enfants. (32)
Comme pour les femmes enceintes ou les insuffisants rénaux, ces enfants ont un taux de ferritine plus bas que la normale.
Dans une autre étude portant sur les capacités de stockage du fer, on a observé que la ferritine à une valeur de 23+/-13ng/ml chez les enfants qui présentent des troubles de l’attention contre 44+/-22ng/ml chez les autres enfants non affectés, soit une baisse de 50%. (31)
5. Patients atteints de la maladie de Parkinson
La maladie de Parkinson est causée par un désordre dopaminergique également retrouvé dans le SJSR. C’est pourquoi il se pose alors la question d’un lien entre ces deux pathologies.
Pour répondre à cette question une étude comparative a été menée chez des patients atteints de la maladie de Parkinson (n= 187) ainsi que chez des sujets témoins (n=172) afin de voir s’il existe une prévalence plus élevée ou non chez ces patients
Les résultats de cette étude montrent une prévalence du SJSR significativement plus élevée (environ 3 fois plus) chez les patients atteints de la maladie de Parkinson 9,6% VS 2,9% chez les sujets témoins. (39)
41
Cependant, beaucoup d’autres études faites à ce sujet ont eu des résultats très différents et contradictoires avec l’hypothèse d’un lien, allant de la prévalence nulle jusqu’à 50% comme le montre tableau 7 ci-dessous.
Tableau 7 : Liste d’études portant sur la prévalence du syndrome des jambes sans repos dans la population atteinte de la maladie de Parkinson VS témoin. (40)
42
En effet, chez les patients parkinsoniens on sait à présent que le SJSR apparaît chez 18,75% des malades, soit 2 fois plus que dans la population générale (diagnostic fait sur la base des critères IRLSSG). Il apparaît que la sévérité du syndrome est proportionnelle à la sévérité de la maladie de Parkinson. Une étude l’a démontrée sur un groupe de 48 patients parkinsoniens non diabétiques, sans insuffisance rénale, sans anémie et sans artérite afin d’exclure des facteurs pouvant prédisposer un SJSR. (41)
Cependant, il existe des limites à ces études notamment la confusion entre les symptômes de ces deux pathologies. En effet, elles ont en commun des troubles moteurs et le SJSR peut être confondu avec les akathisies de la maladie de Parkinson par exemple.
De plus, les résultats hétérogènes sont à associer à des méthodologies différentes selon les études avec des critères d’inclusion et d’exclusion pas toujours identiques, des comorbidités associées selon certains groupes ou encore des groupes avec et sans traitements.
Une des différences majeures entre ces deux pathologies est la concentration en fer dans la substance noire : elle est augmentée chez les patients atteints de la maladie de Parkinson à l’origine d’un stress oxydatif qui conduit à une dégénérescence dopaminergique alors que dans le SJSR elle est diminuée. Le lien entre ces deux pathologies semble donc venir de la dopamine même si aujourd’hui nous n’avons pas assez d’études pour le confirmer. (42)
En conclusion, on peut dire que la thérapie dopaminergique chez les patients atteints de la maladie de Parkinson a probablement un rôle à jouer dans le développement du SJSR, que ce syndrome serait plutôt une manifestation précoce de la maladie de Parkinson qu’un facteur de risque, et qu’il y a bien un mécanisme dopaminergique qui lie ces deux maladies sans pour autant savoir l’expliquer de nos jours. (40)
43 6. Médicaments
Beaucoup de médicaments peuvent engendrer ou augmenter la symptomatologie d’un SJSR, particulièrement ceux qui ont un effet antagoniste de la dopamine. C’est le cas de certains antiémétiques et neuroleptiques.
Selon des expérimentations plus récentes, certains antidépresseurs sont également en cause, tout comme des antihistaminiques présents dans de nombreux médicaments que l’on peut même avoir sans ordonnances (contre le rhume, le mal des transports, les allergies etc…) (2,43).
Les antidépresseurs de 2e génération tels que la fluoxetine, la paroxetine, le citalopram, la sertraline, l’escitalopram, la venlafaxine, la duloxetine et la mirtazapine ont été étudiés dans 4 cabinets de neurologie lors de leur mise en place chez des patients atteints du SJSR.
Les résultats montrent que 9% d’entre eux ont subi une aggravation du syndrome suite à l’installation du traitement (dès les premiers jours), et cela d’autant plus avec la mirtazapine 28%. (44)
Notons l’exemple d’un cas clinique d’une patiente mise sous escitalopram suite à une dépression, qui montre une apparition rapide et brutale du syndrome et nettement amélioré suite à l’arrêt de ce traitement, à nouveau réapparut suite à la réintroduction de ce dernier pour finalement disparaître une semaine après l’arrêt définitif. (45)
Aux États-Unis, un antidépresseur est cependant à part : le bupropion qui n’a pas d’effet d’aggravation du SJSR et tolère bien les agonistes dopaminergiques, il pourrait alors être un antidépresseur de choix si tel en était le besoin (14,46,47) (notons qu’en France le bupropion n’est indiqué que pour le sevrage tabagique).
44
II. Approches thérapeutiques
Les traitements ont uniquement un rôle symptomatique et non curatif, ils sont prescrits dans le but d’améliorer la qualité de vie et de diminuer l’impact des symptômes sur celle-ci.
Une fois le diagnostic du syndrome posé :
- Il faut dans un premier temps expliquer au patient le caractère chronique de cette maladie, avec des périodes d’améliorations et d’exacerbations de la symptomatologie, qu’il pourra identifier et faire le lien avec des évènements de sa journée (stress intense par exemple pour l’exacerbation, pratique sportive pour l’amélioration).
- Il faut informer également le patient que son traitement, s’il est nécessaire, sera très probablement sujet à des adaptations et/ou modifications.
- Il faut d’abord éliminer de façon certaine toute cause pouvant déclencher un SJSR et évaluer la sévérité du syndrome avant d’entreprendre une initiation de traitement.
- Il faut vérifier le taux de ferritine, et réaliser une enquête médicamenteuse afin de voir si le patient prend un traitement à risque tel que les antagonistes dopaminergiques, les neuroleptiques, les antidépresseurs etc. (48)
- Il faut évaluer la sévérité du syndrome, car c’est l’impact de la clinique sur les états de veille et de sommeil qui dicte la décision d’instaurer ou non un traitement.